Ā
- Tratamiento de la presión intracraneal (PIC)
- Tratamiento con barbitúricos
- Tratamiento de segunda línea de la hipertensión intracraneana
- Tratamiento médico del traumatismo encefalocraneal (TEC) en sala o piso de neurocirugía
- Seguimiento del traumatismo encefalocraneal (TEC) por consulta externa
- Alimentación de los pacientes con traumatismo encefalocraneal (TEC)
- Tratamiento quirúrgico del traumatismo encefalocraneal (TEC)
- Agujeros de trepanación exploratorios
- Tratamiento médico quirúrgico de las fracturas de cráneo
- Operaciones en las fracturas cerradas del cráneo
- Operaciones en los hematomas intracraneanos
- Hematoma epidural
- Hematoma subdural
- Consideraciones sobre el tratamiento del hematoma subdural crónico
- Higroma subdural. Hematoma intracerebral
- Operaciones en el traumatismo encefalocraneal (TEC) abierto
- Hemostasis en la ruptura de los senos de la duramadre
Tratamiento de la presión intracraneal (PIC).
Esta sección describe un protocolo general para tratar la hipertensión intracraneal comprobada o, a veces, la sospecha clínica.
Por lo general, se siguen las pautas propuestas en el artículo “Guidelines for the Management of Severe Head Injury” publicadas en el Journal of Neurotrauma. Se recomienda al lector recurrir, si le es posible, a ese documento a fin de que comprenda el proceso que se utilizó para crear esas pautas y entienda las diferencias que existen entre los estándares, las pautas y las opciones que se definen en esa publicación. En los cuadros números 25 y 26 referidos a continuación se resume el protocolo.
Ā
Cuadro número 25. Resumen de medidas generales para controlar la hipertensión intracraneal.
Objetivos: mantener la presión intracraneal (PIC) < 20 mmHg y la presión de perfusión cerebral (PPC) > 60 mmHg.
PASOS – JUSTIFICACIÓN - MEDIDAS GENERALES
- Elevar la cabecera de 30 a 45║: Reduce la presión intracraneal (PIC) por que aumenta el drenaje venoso, reduce la presión carotídea media. No hay cambio claro en flujo sanguíneo cerebral
- Mantener el cuello recto y no ajustar demasiado el tubo de traqueostomía, si llega a utilizarse: La compresión de las venas yugulares aumenta la presión intracraneal (PIC)
- Evitar que aparezca hipotensión, tensión arterial sistólica menor de 90 mm Hg. Normalizar el volumen intravascular. Administrar vasopresores si es necesario.
- Corregir la hipertensión si está presente: Nitroprusiato si no hay taquicardia.
- Betabloqueantes si hay taquicardia, como propanolol, atenolol, labetalol, esmolol. No sobrecorregir a hipotensión
- Evitar que aparezca hipoxia, pO2 menor de 60 mm Hg, mantener la vías respiratorias permeables y oxigenación suficiente. La hipoxia puede agregar lesión isquémica cerebral
- Administrar oxígeno hasta llegar a la normocapnia, pCO2 entre 30 y 40 mm Hg. No instituir hiperventilación preventiva
- Sedación suave de 30 a 60 miligramos de codeína intramuscular cada 4 horas según necesidad. Igual a la sedación fuerte
- TAC de cráneo sin contraste para verificar la causa de la hipertensión. Para descartar una afección que pueda corregirse quirúrgicamente.
Cuadro número 26. Resumen de las medidas especificas para controlar la hipertensión intracraneal.
PASOS – JUSTIFICACIÓN - MEDIDAS ESPECIFICAS (si persiste la hipertensión, instituir las siguientes medidas en el orden propuesto)
- Sedación fuerte de 1 a 2 mililitros de fentanilo o de 2 a 4 miligramos de morfina vía intravenosa (iv) cada 1 hora o bloqueo neuromuscular de 8 10 miligramos de vecuronio vía intravenosa (iv) o ambas medidas. Reduce el aumento del tono simpático y la hipertensión arterial (HTA) provocada por los movimientos, tensa la musculatura abdominal.
- Drenar de 3 a 5 mililitros de líquido cefalorraquídeo (LCR) si hay colocado un catéter intraventricular. Reduce el volumen intracraneal.
- De 0.25 a 1 gramos por kilogramo de manitol, luego 0.25 gramos / kilogramo cada 6 horas; aumentar la dosis si persiste la hipertensión y la osmolaridad sérica es de 320 (no realizar este paso si hay hipovolemia o hipotensión). Aumenta el volumen plasmático y la tonicidad sérica, lo cual extrae líquido del cerebro. Puede mejorar las propiedades reológicas de la sangre.
- Hiperventilar hasta que la pCO2 alcance 30-35 mm Hg. Reduce la pCO2, disminuye el flujo sanguíneo cerebral, reduce la presión intracraneal
- Si persiste la hipertensión, obtener una tomografía axial computerizada (TAC) de cráneo sin contraste y un electroencefalograma. Continuar con el tratamiento de segunda línea
A medida que disminuya la hipertensión se debe ir suspendiendo el tratamiento gradualmente.
Si persiste la hipertensión y, sobre todo, si se produce un aumento inexplicable abrupto, es muy conveniente repetir un TAC de cráneo a fin de descartar que la causa sea una afección que pueda corregirse quirúrgicamente: un coágulo (hemorragia subdural, epidural o intraparenquimatosa) o hidrocefalia.
El electroencefalograma se indica para descartar un estado de mal epiléptico subclínico, que es una causa posible aunque infrecuente de hipertensión intracraneal.
Las dosis a las que se refiere este protocolo corresponden a un adulto promedio, salvo que se especifique en miligramos/Kg. El tratamiento puede iniciarse antes de insertar un monitor si se verifica deterioro neurológico agudo o aparecen signos clínicos de hipertensión intracraneal, pero para mantener el tratamiento es necesario tener pruebas de que persiste la hipertensión intracraneal.
En los casos resistentes, cabe intentar los tratamientos de segunda línea.
El cuadro 27 enumera las medidas adicionales que pueden emplearse para tratar una crisis aguda de hipertensión intracraneana.
Cuadro número 27. Medidas adicionales para tratar una crisis aguda de hipertensión intracraneana.
PASOS – JUSTIFICACIÓN - MEDIDAS ADICIONALES (verificar las vías respiratorias, la posición entre otros aspectos de las medidas generales) para los casos resistentes o abruptos, puede ser conveniente obtener un TAC de cráneo sin contraste
- El paciente debe estar sedado y bajo efecto de bloqueantes neuromusculares como se planteó en las medidas especificas. Reduce el aumento del tono simpático y la hipertensión arterial (HTA) provocada por los movimientos, tensa la musculatura abdominal
- Drenar de 3 a 5 ml de líquido cefalorraquídeo (LCR) si hay colocado un catéter intraventricular. Reduce el volumen intracraneal
- 1 gramo por kilogramo de manitol en bolo vía intravenosa (iv). Aumenta el volumen plasmático y la tonicidad sérica, lo cual extrae líquido del cerebro. Puede mejorar las propiedades reológicas de la sangre, aumenta el flujo sanguíneo cerebral, disminuye la presión intracraneal (PIC), aumenta la osmolaridad sérica y disminuye el agua cerebral.
- Hiperventilar con ambú, mantener la pCO2 mayor de 25 mm Hg. Reduce la pCO2, disminuye el flujo sanguíneo cerebral, reduce la presión intracraneal. Precaución: puesto que reduce el flujo, no debe utilizarse más que algunos minutos.
- Pentobarbital 100 miligramos en infusión vía intravenosa (iv) lenta; o tiopental 2.5 miligramos /kilogramo vía intravenosa (iv) durante 10 minutos. Tiene efecto sedante, disminuye la presión intracraneal (PIC). También es un depresor miocárdico, disminuye la presión arterial media, trata las convulsiones, puede ser neuroprotector.
El uso del manitol está contraindicado si el paciente esta hipotenso, hipovolémico o si la osmolaridad sérica es mayor de 320 mOsm/l.
En algunos países la disponibilidad del pentobarbital ha disminuido y puede llegar a ser necesario sustituirlo por otros sedantes.
Protocolo de tratamiento de la presión intracraneal (PIC).
Los objetivos del tratamiento son: Mantener la PIC < 20 mmHg, evita que las mesetas comprometan el flujo sanguíneo cerebral y provoquen isquemia y muerte cerebrales.
Mantener la presión de perfusión cerebral (PPC) > 60 mmHg, evitar la hipotensión. El principal objetivo consiste en reducir la presión intracraneal (PIC), que se logra manteniendo una presión arterial media suficiente que asegure que la presión de perfusión cerebral sea constantemente > 60 mmHg.
Tratamiento quirúrgico.
Todo hematoma epidural o subdural de diámetro máximo superior a 1 cm debe ser evacuado quirúrgicamente a fin de eliminar su influencia sobre la hipertensión endocraneana. Los pacientes que presenten contusiones hemorrágicas y un deterioro neurológico progresivo pueden ser candidatos para una intervención en la que se extirpe la parte del tejido cerebral dañado.
Cuidados generales.
Los objetivos principales son prevenir la aparición de la hipoxia (pO2 < 60 mmHg) y de la hipotensión (tensión arterial sistólica < 90 mmHg).
Medidas terapéuticas específicas.
Prevención de las hemorragias gástricas de las úlceras por corticoides (si se emplean) y de las úlceras de Cushing (son frecuentes en los traumatismos encefalocraneales (TEC) graves con hipertensión intracraneana, asociados a hipergastrinemia) a través del aumento del PH gástrico con el uso de un antiácido o antihistamínico H2 o ambos, como la ranitidina 50miligramos vía intravenosa (iv) cada 8 horas. No administrar cimetidina si el paciente está recibiendo fenitoína. Otro medicamento indicado es el sucralfato.
Tratamiento intensivo de la fiebre, ya que es un estímulo potente que aumenta el flujo sanguíneo cerebral, lo que eleva la presión intracraneal (PIC) y, también puede acentuar las ondas en meseta. Hay que mantener una normotermia corporal con antipiréticos, algunos han empleado mantas enfriadoras, bolsas de hielos en la cabeza, abdomen y extremidades u otros medios.
Colocar una vía arterial para controlar la tensión arterial y obtener gasometrías frecuentes.
Colocar una vía para medir la presión venosa central o presión pulmonar arterial si son necesarias dosis altas de manitol. (Para mantener el paciente en euvolemia).
Los líquidos intravenosos de elección utilizados en los traumatismos encefalocraneales (TEC) son las soluciones isotónicas como la solución fisiológica + 20 mEq CLK /l. No administrar soluciones hipotónicas como la solución Ringer Lactato, ya que puede disminuir la distensibilidad cerebral.
El volumen hídrico adecuado es importante para proporcionar una reanimación hídrica suficiente, para que no haya hipotensión.
La normalización del volumen hídrico no es nocivo para la presión intracraneal (PIC), si bien la restricción de líquidos reduce la cantidad de manitol que es necesaria para disminuir la presión intracraneal (PIC), en la actualidad se considera obsoleto dejar que los pacientes se deshidraten, si es necesario utilizar manitol el paciente debe estar euvolémico, se debe tener precaución cuando se restringen los líquidos tras una hemorragia subaracnoidea (HSA) ya que puede aparecer un síndrome cerebral perdedor de sal.
Si hay traumatismos de otros órganos, alguna víscera perforada, el volumen de líquidos que se debe administrar quedará determinado por ese traumatismo.
Los vasopresores como la dopamina son preferibles a la infusión intravenosa.
Medidas para disminuir la presión intracraneal (PIC).
Medidas generales.
- La posición de la cabeza del paciente en el lecho. Es importante mantener la cabeza más elevada que el cuerpo (posición Fowler) y evitar rotaciones extremas de la misma, para facilitar el drenaje venoso y reducir la presión intracraneal (PIC).
Elevar la cabecera 30 a 45 ║, mantener la cabeza centrada en la línea media, a fin de evitar de que se formen acodamientos de las yugulares con la consiguiente isquemia cerebral.
- La sedación debe ser suave de 30 a 60 miligramos de codeína intramuscular cada 4 horas según necesidad, o 1 o 2 miligramos de lorazepan (Trapax) vía intravenosa (iv) cada 4 a 6 horas según necesidad.
- Prevenir la hipotensión (tensión arterial sistólica < 90 mmHg), normalizar la volemia intravascular, administrar tratamiento de apoyo con vasopresores.
4. Corregir la hipertensión arterial (HTA), sobre todo en los casos de hemorragia intracerebral, el objetivo debe ser la tensión arterial habitual o por lo menos mantener la presión sistólica inferior a 160 mm Hg, con nitroprusiato si no hay taquicardia y, en los pacientes con taquicardia se utilizan betabloqueadores. El aumento de la presión arterial eleva la penetración de proteínas y líquido al cerebro con una barrera hematoencefálica alterada, también la hipertensión debe evitarse, para no comprometer la presión de perfusión cerebral.
5. Prevenir la hiperglicemia, agrava el edema cerebral de aparición frecuente en los pacientes con TEC. La hiperglicemia puede verse agravada en la diabetes mellitus y por el uso de corticoides.
6. Intubar a los pacientes que tienen un puntaje en la escala de Glasgow para coma (EGC) igual o menor de 8 puntos o que presentan disnea, en estos casos administrar lidocaína vía intravenosa (iv) primero.
7. No hiperventilar, mantener la pO2 en el margen normal inferior de la eucapnia de 35 mmHg.
Medidas para reducir la hipertensión intracraneana comprobada.
En primer lugar, es necesario verificar que se hayan tomado las medidas generales mencionadas, Seguir los siguientes pasos si persiste la hipertensión intracraneal.
La sedación fuerte o bloqueo neuromuscular cuando sea necesario o ambos, estas medidas también son de ayuda para tratar la hipertensión (HTA), por ejemplo, cuando el paciente está agitado o cuando se produce un aumento abrupto de la presión intracraneal (PIC) tras ciertas maniobras, como al mover al paciente desde la camilla hasta el tomógrafo. Como precaución, cuando el paciente está muy sedado o bloqueado, no resulta posible controlar el estado neurológico por lo tanto es preciso monitorear la presión intracraneal (PIC).
Si la presión intracraneal (PIC) es significativamente elevada mayor de 40 torr por 15 minutos o más y/o la presión cerebral es menor de 50 torr, deben emplearse barbitúricos como el pentobarbital en el tratamiento. La presión de perfusión cerebral (PPC) se obtiene restando a la presión sanguínea media la PIC (PPC= PSM - PIC).
Es normal cuando es mayor de 50 mm de agua. La presión sanguínea media es igual a la presión diastólica más un tercio de la presión diferencial por ejemplo para una tensión arterial de 120 y 80 mm Hg, la presión sistólica media (PSM) va a ser igual 80 más (40 /3).
Si no hay posibilidad de la medición continua de la presión intracraneal (PIC) puede valorarse la conveniencia del tratamiento descrito en los puntos anteriores: en los pacientes que mantengan crisis tónicas de rigidez tipo decorticación o descerebración o se mantengan flácidos.
Si el cráneo queda abierto por craniectomía descompresiva extensa pueden ocurrir desplazamientos del contenido intracraneal con 15 o menos torr de presión intracraneal (PIC) y la palpación del área quirúrgica nos da una mejor información que la medición mecánica de la PIC.
Pentobarbital de 3 a 5 miligramos por kilo como dosis inicial de carga y continuar con 100 a 200 miligramos vía intravenosa (iv) cada 30 a 60 minutos, por 72 horas para mantener un nivel en sangre de 2.5 a 3,5 miligramos%.
Otro método utilizado es dosis de carga de 10 miligramos por kilo de peso hora durante 4 horas consecutivas. Después mantener infusión continúa de 1.6 miligramos kilogramo hora.
El tratamiento con barbitúricos se suspende cuando se normaliza la respuesta de la presión de volumen intracraneal, elevación de menos de 3 mmHg de la presión intracraneal (PIC) al inyectar 1ml de suero fisiológico por catéter ventricular, cuando la PIC es menor de 15 mm de Hg por 72 horas, cuando la presión arterial sistémica es menor de 160 mmHg sin necesidad de terapia vasodilatadora.
La acción beneficiosa de los barbitúricos para reducir la mortalidad, al menos en dosis muy elevadas, no es aceptada en la actualidad de forma unánime.
La acción de los barbitúricos para disminuir la presión intracraneal (PIC) ha sido argumentada de forma experimental y también clínica, por algunos autores, quienes sostienen que los barbitúricos actúan por su efecto constrictivo sobre los vasos cerebrales, provocando una reducción de la formación de edema al elevar el tono vascular y reducir la presión hidrostática en el área lesionada, así como disminuir la presión arterial sistémica, estabilización de la presión de perfusión cerebral y disminución del metabolismo cerebral.
Además de disminuir el consumo de oxígeno por el cerebro entre un 53 a un 55%, limita la fuga de potasio celular, la salida de radicales libres que afectan los lípidos de la membrana celular y protege la microcirculación al reducir la peroxidación de ácidos grasos libres.
La acción de los barbitúricos permite, en muchos pacientes reducir las dosis de deshidratantes para el control de la presión intracraneal (PIC). La protección del sistema nervioso central (SNC) es mayor cuando se emplea una dosis inicial directa, seguida de una infusión continua para efecto farmacológico estable.
Otros métodos de empleo de los barbitúricos cuando no puede medirse la presión intracraneal (PIC) y no hay pentobarbital (acción corta) son, emplear tiopental (acción ultracorta) o el fenobarbital (acción larga) en dosis suficiente para deprimir o aplanar el electroencefalograma (EEG) entre 2 a 5 Hz.
Después se continúa con dosis fraccionadas y control de electroencefalograma y se mantiene de 3 a 6 días, se retira gradualmente y se suprime cuando, clínicamente, no hay hipertensión intracraneal.
El empleo del tiopental afecta menos la estabilidad cardiopulmonar que otros anestésicos y brinda mayor protección contra el infarto cerebral, por penetrar más fácilmente al sistema nervioso central (SNC) que el pentobarbital, a niveles plasmáticos similares.
En pacientes cuya respiración no está controlada pueden usarse dosis medias de tiopental, 500 miligramos directo vía intravenosa.
En los pacientes con una presión intracraneal (PIC) significativamente elevada, mayor de 40 torr o con presión de perfusión cerebral (PPC) menor de 50 mmHg, con respiración controlada, algunos autores recomiendan dosis muy altas, entre 20 a 50 miligramos por kilo como dosis inicial de carga, directo en vena durante una hora, en inyecciones fraccionadas de 50 a 100miligramos y después continuar con 100 a 200 miligramos vía intravenosa cada 30 a 60 minutos o con una dilución equivalente en venoclisis.
Recomendamos si no es posible realizar TAC evolutivos o medición constante de la presión intracraneal (PIC), sólo es recomendable el empleo de barbitúricos en dosis altas, en pacientes en que se descarto, por otros medios, un hematoma intracraneal.
Para instituir una sedación profunda se recomienda intubar a fin de prevenir una depresión respiratoria, un aumento de la pCO2 y un aumento de la presión intracraneal (PIC), por ejemplo emplear uno de los siguientes fármacos: fentanilo 1 o 2 ml vía intravenosa. cada 1 hora, morfina 2 a 4 miligramos vía intravenosa (iv) cada 1 hora, goteo de propofol, pentobarbital en dosis bajas, en adultos 100 miligramos vía intravenosa (iv) cada 4 horas; en niños 2 a 5 miligramos /Kg vía intravenosa (iv) cada 4 horas.
El propofol o Diprivan se administra para sedación de la siguiente forma, comenzar con 5 a 10 ug/Kg/ minuto. Aumentar en 5 a 10 ug/Kg/ minuto cada 5 o 10 minutos, según la sedación deseada, hasta un máximo de 50 ug / Kg /minuto Su presentación es de 500 miligramos suspendidos en frasco de 50 ml de emulsión lipídica.
Tanto el frasco como los catéteres deben cambiarse después de 12 horas de uso porque el fármaco no contiene agentes bacteriostáticos.
Para el bloqueo neuromuscular es obligatorio intubar, se utilizan de 8 a 10 miligramos de vecuronio vía intravenosa (iv) cada 2 o 3 horas.
Otra medida importante es el drenaje de líquido cefalorraquídeo (LCR) si se está utilizando un catéter intraventricular para medir la presión intracraneal (PIC), se drenan de 3 a 5 ml de LCR con la cámara cuentagotas ubicada a 10 cm del conducto auditivo externo: El efecto es inmediato por la extracción del líquido cefalorraquídeo (LCR), porque se reduce el volumen intracraneano y, posiblemente, porque permite que el líquido del edema drene hacia los ventrículos, esta última consideración está muy discutida.
Se debe tener en cuenta el uso de los deshidratantes cerebrales u osmoterapia, cuando hay signos de hipertensión intracraneana. El manitol se administra en bolo vía intravenosa (iv) de 0,25 a 1 gramo / Kg durante menos de 20 minutos seguido de un bolo vía intravenosa (iv) de 0,25 g/ Kg durante más de 20 minutos cada 6 horas según necesidad para lograr una presión intracraneal (PIC) > 20.
Es posible alternar este fármaco con la furosemida o Lasix que se administra en una dosis de 10 a 20 miligramos vía intravenosa (iv) cada 6 horas según necesidad para que la PIC < 20; en niños 1 miligramo/Kg vía intravenosa (iv), la dosis máxima es de 6 miligramos, cada 6 horas para lograr una presión intracraneal (PIC) >20.
Mantener al paciente en estado euvolémico ligeramente hipervolémico. Si persiste la hipertensión y la osmolaridad sérica es < 320 mOsm/l, aumentar la dosis del manitol hasta 1 g / Kg y disminuir el intervalo de dosificación cada 4 horas. Interrumpir la osmoterapia si la osmolaridad sérica es > 320 mOsm/l, una mayor tonicidad no contribuye en nada y pone en riesgo la función renal. También se debe interrumpir la osmoterapia si la tensión arterial sistólica < 100 mmHg.
La hiperventilación para llegar a una pCO2 = 30 – 35 mm Hg, no emplear como prevención, no instituir la hiperventilación intensiva (pCO2 menor o igual de 25 mm Hg) en ningún momento. Sólo debe utilizarse durante períodos cortos si aparece deterioro neurológico agudo o, como tratamiento prolongado si se comprueba hipertensión intracraneal resistente a la sedación, al bloqueo neuromuscular, al drenaje del líquido cefalorraquídeo (LCR) y a la osmoterapia. Si es posible, no hiperventilar durante las primeras 24 horas después del traumatismo encefalocraneal (TEC).
En algunos países se emplea si la presión intracraneal (PIC) es mayor de 15 torr, para lograr una PaCO2 de 30 torr o un valor menor y una PaO2 de 70 torr o mayor, con respirador volumétrico y relajantes musculares si es necesario. La ventilación controlada se descontinúa cuando la presión intracraneal (PIC) es normal. Si no hay contraindicaciones médicas de otro tipo.
Los corticoides: se han utilizado para disminuir la hipertensión intracraneal postraumática sobre todo los glucocorticoides.
Actualmente no se recomienda administrarlos en el tratamiento de los que sufrieron un traumatismo encefalocraneal (TEC), excepto en los pacientes en los que se verifique una disminución de las hormonas suprarrenales endógenas. Si bien los glucocorticoides reducen el edema cerebral vasógeno como el que rodea a los tumores cerebrales y pueden ser eficaces para controlar la presión intracraneal (PIC) en los casos de pseudotumor cerebral, tienen poco efecto sobre el edema cerebral citotóxico, que es el tipo de edema más frecuente tras un traumatismo encefalocraneal (TEC).
Los corticoides pueden tener efectos colaterales o complicaciones importantes: coagulopatías, hiperglicemia que tiene un efecto nocivo cuando hay edema cerebral y además el aumento de la incidencia de infecciones a causa de la inmunodepresión que ocasiona.
La dexametasona ha sido la más empleada, puede provocar las complicaciones mencionadas y sólo actúa con eficiencia si se comienza su uso en las primeras 6 horas después del traumatismo y en dosis masiva, 48 a 100 miligramos vía intravenosa (iv) de inicio y después 24 a 48 miligramos vía intravenosa (iv) o vía intramuscular (im) por 5 a 8 días.
La metilprednisolona se utiliza de la siguiente forma, 40 miligramos cada 6 horas o a razón de 30 miligramos por kilogramo en dosis única.
Otros esteroides parecen tener poco o ningún efecto sobre la presión intracraneal (PIC) postraumática.
Se está estudiando el empleo de corticoides no glucocorticoideos como por ejemplo (21 – aminoesteroides), también denominados lanzaroides.
Tratamiento barbitúrico de dosis altas.
En teoría, el efecto beneficio de los barbitúricos deviene de que provocan vasoconstricción de las zonas normales, derivan sangre hacia el tejido cerebral isquémico, disminuyen la demanda metabólica de oxígeno y, como consecuencia, decrece el flujo cerebral, provocan la captación de radicales libres, reducen el calcio intracelular y estabilizan los lisosomas.
No cabe duda de que los barbitúricos bajan la presión intracraneal (PIC), incluso en los casos en que otros tratamientos no fueron efectivos, pero, en cuanto a la evolución clínica, hay discordancia, algunos estudios demostraron que tienen beneficios pero otros dan cuenta de efectos nocivos. Los pacientes que respondieron a este tratamiento tuvieron una mortalidad más baja, de un (33%), que quienes no obtuvieron ningún beneficio en lo que respecta a la presión intracraneal (PIC) (75%).
El factor limitante para instituir este tratamiento es, por lo general, la hipotensión, por que los barbitúricos provocan una reducción del tono simpático, que causa vasodilatación periférica, y una leve depresión miocárdica directa. La hipotensión afecta a un 50% de los pacientes aunque la volemia sea suficiente y se halla empleado dopamina.
El tratamiento con barbitúricos imposibilita el examen neurológico, por lo que es necesario monitorear la presión intracraneal (PIC) para evaluar el estado del paciente.
Comparación entre el coma barbitúrico y el tratamiento de dosis altas.
Si se administran barbitúricos hasta que se observe en el electroencefalograma una depresión de la actividad eléctrica con supresión de salvas, el paciente ha entrado en un verdadero coma barbitúrico, que lleva a una reducción casi total de la demanda metabólica de oxígeno y del flujo sanguíneo cerebral. Aún así, la mayoría de los regímenes deberían recibir la denominación técnica de tratamiento endovenoso de dosis altas por que tienen como objetivo llegar a concentraciones séricas especificas de los barbitúricos por ejemplo de 3 a 4 miligramos/% en el caso del pentobarbital, aunque casi no haya relación entre la concentración sérica, el beneficio terapéutico y las complicaciones sistémicas.
Medidas adyuvantes a la administración de barbitúricos en dosis altas son: cabe utilizar un catéter Swan-Ganz para medir la presión pulmonar arterial durante la primera hora de dosis de carga.
Colocar una sonda nasogástrica para aspirar el contenido intestinal ya que las dosis altas de barbitúricos provocan un íleo paralítico; puede ser conveniente hiperalimentar al paciente por vía intravenosa durante el tratamiento con barbitúricos.
Indicaciones de los barbitúricos
El empleo de barbitúricos debe quedar reservado para las situaciones en las que no sea posible bajar la presión intracraneal (PIC) utilizando las medidas que ya se describieron, ya que existen datos que demuestran que el tratamiento preventivo con barbitúricos no mejora la evolución clínica y, además, está asociado a efectos colaterales graves, sobre todo hipotensión, que puede a su vez provocar deterioro neurológico.
Elección de los barbitúricos
Si bien se han estudiado varios barbitúricos, no se dispone de información suficiente que avale recomendar uno en lugar de otro. El pentobarbital es el más estudiado, pero su disponibilidad a disminuido en algunos países como es el caso de los EE.UU, y puede llegar a ser necesario reemplazarlo con otro sedantes.
Otros agentes que no han sido tan estudiados como el pentobarbital son el tiopental, el fenobarbital, el propofol y el etomidato, que no es un barbitúrico sino un hipnótico de acción corta que tiene efectos similares a los de la GABA: deprime la actividad eléctrica de las neuronas, lo que a su vez reduce el metabolismo neuronal hasta un 50%. Además, inhibe la liberación de los neurotransmisores excitadores.
El pentobarbital tiene un inicio de acción rápido (el efecto máximo se registra tras 15 minutos), una duración corta de 3 a 4 horas y una vida media de 15 a 48 horas.
Protocolo para el tratamiento de adultos con pentobarbital.
Existen varios protocolos. Aquí se describe uno simple tomado de un estudio clínico aleatorizado.
- Dosis de carga: 10 miligramos/ Kg de pentobarbital vía intravenosa (iv) durante 30 minutos. Luego, 5 miligramos / Kg cada hora por 3 dosis.
- Mantenimiento: 1 miligramo/Kg /hora.
Protocolo más complejo:
Dosis de carga: 10 miligramos/Kg de pentobarbital vía intravenosa (iv) durante 4 horas de la siguiente manera:
La primera hora: 2,5 miligramos/ Kg en bolo vía intravenosa (iv) lento cada 15 minutos por 4 dosis (total 10 miligramos/Kg la primera hora); controlar la tensión arterial.
Las siguientes tres horas: 10 miligramos / Kg en infusión continua (colocar 2500 miligramos de pentobarbital en 250 ml de líquido vía intravenosa (iv) adecuado, infundir a Kg ml/ h por 3 horas
Ā(Kg = peso del paciente en kilogramos).
Mantenimiento: 1,5 miligramos/ Kg / h en infusión (colocar 250 miligramos en 250 ml de líquido vía intravenosa (iv) e infundir a 1,5 por Kg ml/ h).
Verificar la concentración del fármaco en suero 1 hora después de completar la dosis de carga: generalmente debe ser de 3,5 - 5,0 miligramos%.
Verificar la concentración sérica diariamente mientras dure el tratamiento.
Si la concentración llega a ser mayor de 5 miligramos% y la presión intracraneal (PIC) está en un valor aceptable, se debe reducir la dosis.
Registrar los potenciales evocados de tallo cerebral (PEAT) iniciales al comienzo del tratamiento. Pueden no obtenerse si existen justificativos clínicos. Repetir el registro si la concentración de pentobarbital supera los 6 miligramos%. Si se deterioran los PEAT, se debe reducir la dosis (precaución: un hemotímpano puede interferir en el registro de los potenciales evocados de tallo cerebral (PEAT).
Objetivo: presión intracraneal (PIC) menor de 24 mm Hg y concentración de fenobarbital de 3 a 5 miligramos% cabe suspender el pentobarbital por ineficacia si la presión intracraneal (PIC) se mantiene en valores mayores de 24 mm Hg a pesar de que la concentración del fármaco haya sido la adecuada durante 24 horas.
Si la PIC es menor de 20 mm Hg, continua con el tratamiento durante 48 horas y luego disminuir la dosis gradualmente. Si aumenta la presión intracraneal (PIC), volver al estadio anterior hasta que disminuya.
La función neurológica normal se recupera aproximadamente dos días después de suspender el tratamiento.
La concentración del pentobarbital debe ser menor de 10 μg/ml para poder efectuar un examen de muerte cerebral que sea válido.
En el cuadro 28 se expresan los efectos de la concentración del pentobarbital sobre el sistema nervioso central.
Cuadro número 28. Efectos de la concentración del pentobarbital sobre el sistema nervioso central (SNC).
Grados de depresión del SNC - miligramos% - μg/ml.
Concentración válida para efectuar examen de muerte cerebral: Menor o igual a 1 - Menor o igual a 10
Sedación: relajado, el paciente se despierta fácilmente: 0,05 – 0,3 - 0,5 – 3
Sedación intensa: dificultad para despertarlo, depresión respiratoria: 2 - 20
Coma (generalmente, supresión de salvas en el electroencefalograma (EEG)): 5 - 50
Según las publicaciones, estos valores provienen de pacientes sensibles al fármaco; existe gran variabilidad entre los pacientes y es probable que quienes toleran el fármaco no lleguen a estar sedados ni siquiera con concentraciones de 100 ug/ ml.
Tiopental.
Este fármaco puede ser de utilidad cuando se necesita un barbitúrico de acción rápida por ejemplo, en el quirófano o cuando no se disponga de dosis suficientes de pentobarbital. Puede utilizarse de la siguiente forma (no se ha estudiado el tiopental para esta indicación, pero en teoría es similar al pentobarbital).
La dosis de carga: 5 miligramos/kilogramo (margen de 3 a 5) de tiopental vía intravenosa (iv) durante 10 minutos. Luego, infusión continúa de 5 miligramos/kilogramo/h (margen de 3 a 5) durante 24 horas.
Puede llegar a ser necesario administrar otro bolo de 2.5 miligramos/ kilogramo para bajar la presión intracraneal (PIC). Después de 24 horas, se saturan las grasas, por lo que se debe reducir la infusión a 2.5 miligramos / kilogramo/ hora. Ajustar la dosis para bajar la presión intracraneal (PIC) o monitorear con electroencefalograma (EEG) hasta obtener el silencio bioeléctrico. La concentración terapéutica en suero es de 6 a 8.5 miligramos /dl.
Si bien no se ha estudiado este fármaco para el tratamiento de la presión intracraneal (PIC), se ha sugerido un protocolo de sedación: comenzar con 5 a 10 ug/kilogramo/minuto; aumentar de 5 a 10 ug/kilogramo/minuto cada 5 o 10 minutos, según sea necesario, hasta que baje la presión intracraneal (PIC).
Se ha utilizado el propofol como tratamiento neuroprotector durante la operación de los aneurismas intracraneales con dosis de hasta 170 ug/kilogramo/minuto. También puede provocar hipotensión.
Tratamiento de segunda línea de la hipertensión intracraneana.
Si la hipertensión intracraneana persiste a pesar de haber instituido las medidas ya descritas, y, sobre todo, si se produce un repunte de la presión intracraneal (PIC) después de haber sido controlada, es sumamente recomendable repetir una tomografía axial computerizada (TAC) de cráneo a fin de descartar que la causa de la hipertensión sea una afección quirúrgica antes de comenzar cualquier tratamiento de segunda línea, que, aunque eficaces, plantean riesgos significativos como por ejemplo, los barbitúricos en dosis altas, o sus efectos no están comprobados en cuanto al beneficio que proporcionan a la evolución clínica. Así mismo, también es conveniente realizar un electroencefalograma para descartar un estado de mal epiléptico que no genere signos clínicos evidentes.
Uso de barbitúricos en dosis altas: se inicia el tratamiento si la presión intracraneal (PIC) se mantiene mayor de 20 a 25 mm Hg.
La hiperventilación: Sirve para lograr la hipocapnia hasta que la pCO2 sea igual a 25 o 30 mm Hg (torr). Se recomienda controlar la saturación yugular de la oxihemoglobina (SjO2), la diferencia del contenido de oxígeno arteriovenoso cerebral (AvdO2) y el flujo sanguíneo cerebral.
La hiperventilación ha sido un método efectivo para reducir rápidamente el volumen sanguíneo cerebral y la presión intracraneal. Es discutido la efectividad de la hiperventilación prolongada. Ya que pasado cierto tiempo el pH del líquido cefalorraquídeo (LCR) se normaliza y atenúa la constricción cerebrovascular inducida por la hiperventilación. Además si se mantienen durante muchos días grados extremos de hipocapnia, la reducción del volumen sanguíneo y el flujo sanguíneo cerebral provocan isquemia e infarto cerebral. Es aceptable aún por algunos el tratamiento con hiperventilación durante 2 a 4 días como tratamiento de segunda línea.
Hipotermia: es preciso verificar que los pacientes no tengan disminución del índice cardiaco, trombocitopenia, depuración elevada de creatinina ni pancreatitis. Durante un tiempo se preconizó el empleo de cascos de enfriamiento o mantas especiales para alcanzar temperaturas de 32║C, durante unos 15 días en pacientes menores de 30 años, con crisis de rigidez tipo descerebración. Se aduce que este tratamiento disminuye el tono muscular, la presión intracraneal y las secreciones respiratorias: actualmente, no se acepta por las complicaciones cardiovasculares que puede provocar y su interferencia con la utilización de barbitúricos. Sin embargo, se insiste en mantener la normotermia corporal.
Craniectomía descompresiva: se reseca una porción de la calota y zonas extensas de tejido cerebral contuso y hemorrágico (hace lugar de inmediato y elimina zonas donde la barrera hematoencefálica está alterada). Este procedimiento es controvertido, porque puede incluso propiciar la formación de edema. Si hay contusión del polo temporal, cabe realizar una lobectomía de no más de 4 o 5 centímetros del lado dominante y de 6 o 7 centímetros en el caso de que sea la lesión del lado no dominante, dado que una lobectomía total es demasiado agresiva, o una lobectomía del lóbulo frontal, si la contusión es frontal. Aún así, los resultados de estos procedimientos no han confirmado las expectativas.
Se reporta además el tratamiento antihipertensivo
Medidas adyuvantes.
La lidocaína: 1,5 miligramos/ Kg al menos 1 minuto antes de intubar o aspirar, debe controlarse que no aparezca hipotensión y se debe reducir la dosis si llegara a ocurrir. Detiene el aumento de la presión intracraneal (PIC), la taquicardia y la hipertensión arterial (HTA) sistémica, estos datos corresponden a pacientes que tenían un tumor cerebral y que fueron entubados con anestesia superficial de barbitúricos y monóxido de dinitrógeno (N2O); no se ha comprobado que pueda extrapolar a los traumatizados.
Respiración asistida de alta frecuencia: evaluar si son necesario niveles altos de presión espiratoria final positiva (PEFP). Los pacientes que tienen distensibilidad pulmonar reducida, por edema pulmonar, trasmiten más la PEFP a través de los pulmones hacia los vasos torácicos, lo que puede aumentar la presión intracraneal (PIC). Los niveles de presión espiratoria final positiva (PEFP) hasta 10 centímetros de agua no provocan aumento de la PIC de importancia clínica. No se recomienda llegar a niveles más altos de presión espiratoria final positiva (PEFP) mayor de 15 a 20 centímetros de agua. Asimismo, es preciso tener en cuenta que un descenso brusco de la presión espiratoria final positiva (PEFP) puede causar un aumento abrupto de la volemia, que puede agravar el edema cerebral y provocar un aumento de la presión intracraneal (PIC).
Descripción de algunas medidas terapéuticas.
Elevación de la cabecera.
Algunos datos antiguos obtenidos de estudios realizados con perros indican que mantener la cabecera entre 30║ y 45║ hace que se compensen los siguientes dos efectos: la reducción de la presión intracraneal (PIC), porque aumenta el drenaje venoso y promueve el desplazamiento del líquido cefalorraquídeo (LCR) desde el compartimiento intracraneal hacia el raquídeo, y la reducción de la presión de perfusión cerebral, porque se reduce la presión arterial media de las arterias carótidas.
Algunos datos más recientes indican que, si bien elevar la cabecera a 30║ reduce la presión carotídea media, también disminuye la PIC, por lo que el flujo sanguíneo cerebral no se ve alterado. El efecto tras elevar la cabecera es inmediato.
Hiperventilación.
La hiperventilación disminuye la presión intracraneal (PIC) porque al bajar la pCO2, determina una vasoconstricción cerebral que reduce el volumen sanguíneo cerebral (intracraneal) como la vasoconstricción reduce el flujo sanguíneo del cerebro, existe el riesgo de provocar isquemia focalizada en zonas que conserven la autorregulación cerebral por el fenómeno del robo inverso. No obstante, no siempre se produce isquemia porque también puede aumentar la fracción de extracción de oxígeno.
La hiperventilación, en una época fue considerada una medida de defensa de primera línea contra la hipertensión intracraneal, ahora es considerada un método que debe emplearse con moderación y sólo en situaciones especificas.
La hiperventilación preventiva se asocia en la actualidad a una peor evolución. Cuando se indica, sólo se debe tener como propósito que la pCO2 llegue a ser de 30 a 35 mm Hg.
El flujo sanguíneo cerebral de los TEC graves ya de por sí está reducido a la mitad de lo normal durante las primeras 24 horas. Según una publicación, la hiperventilación con pCO2 igual a 30 mm Hg instituida dentro de las 8 a 14 horas de ocurrido el traumatismo encefalocraneal (TEC) grave no influyó en el metabolismo cerebral general, pero no se estudió la probabilidad de que produjese cambios focales.
Cuando se habla de la hiperventilación preventiva, se está haciendo referencia a su uso en casos que no presentan signos de hipertensión intracraneana y en los casos en que no se ha comprobado el fracaso de las otras medidas mediante el monitoreo de la presión intracraneal (PIC).
La hiperventilación que lleva la pCO2 a menos de 30 mm Hg reduce aún más el flujo sanguíneo cerebral, pero no necesariamente reduce la presión intracraneal (PIC) y, además, puede alterar la autorregulación cerebral. Si se la controla cuidadosamente, puede ser útil en muchas ocasiones.
En el cuadro 29 mostramos un resumen de los márgenes de la pCO2 y las recomendaciones respecto de este tema.
Cuadro número 29. Resumen de los valores recomendados de pCO2 tras un traumatismo encefalocraneal (TEC).
PCO2 (mm Hg) - Descripción
35-40: Normocapnia, uso de rutina
30-35: Hiperventilación, no como método preventivo. Usar sólo en un período breve si se observa deterioro neurológico (signos clínicos de hipertensión intracraneal) o en un período prolongado si se comprueba que la hipertensión no responde a otras medidas
25-30: Hiperventilación acentuada. Tratamiento de segunda línea. Sólo debe utilizarse cuando fracasan las otras medidas para bajar l hipertensión. Se recomienda monitoreo para descartar isquemia cerebral.
< 25: Hiperventilación intensiva. No se ha comprobado su beneficio. Grandes probabilidades de que provoque isquemia.
En la mayoría de los pacientes, la reducción de la pCO2 de 35 a 29 mm Hg disminuye la presión intracraneal (PIC) en 25 a 30%. El inicio del efecto ocurre tras 30 segundos y el efecto máximo se registra a los 8 minutos. La duración de esta acción puede ser muy corta, entre 15 y 20 minutos. Dentro de la hora, la acción puede quedar truncada según una publicación sobre estos pacientes que tenían tumores cerebrales, después de la cual resulta difícil retornar a la normocapnia sin que se produzca un rebote de la presión intracraneal (PIC). Por ese motivo, la hiperventilación se debe retirar lentamente.
Indicaciones de la hiperventilación.
Por períodos breves (minutos) en las siguientes circunstancias: antes de insertar un monitor de la presión intracraneal (PIC) si hay signos clínicos de hipertensión intracraneana. Tras la inserción de un monitor si se observa una aumento abrupto de la PIC o se produce deterioro neurológico. Puede ser utilizada mientras se realiza la evaluación prequirúrgica de un paciente que tiene una lesión tratable como es el caso de un hematoma intracraneal tardío.
Por períodos prolongados, cuando se comprobó que la hipertensión intracraneal no responde a la sedación, ni al bloqueo neuromuscular, ni al drenaje de líquido cefalorraquídeo (LCR) si está disponible, ni a los diuréticos osmóticos.
Puede ser apropiada para tratar la hipertensión intracraneana que es consecuencia preponderante de hiperemia.
Precauciones en el empleo de la hiperventilación.
- Evitar la hiperventilación durante los primeros 5 días después del traumatismo encefalocraneal (TEC), sobre todo, durante las primeras 24 horas.
- No se debe emplear como método preventivo.
- Si se comprobó que la hipertensión intracraneal no responde a ninguna otra medida, se debe hiperventilar cuidando que la pCO2 sea de 30 a 35 mm Hg.
- Si resulta necesario hiperventilar por un período prolongado con una pCO2 que llegue a 25 o 35 mm Hg, es conveniente verificar la saturación yugular de la oxihemoglobina, la diferencia del contenido de oxígeno arteriovenoso cerebral o el flujo sanguíneo cerebral a fin de detectar la isquemia cerebral.
- La pCO2 nunca debe estar por debajo de los 25 mm Hg.
Tratamiento médico en piso o sala de neurocirugía.
A los pacientes con traumatismo encefalocraneal (TEC) o sus secuelas, cuya envergadura no permita el tratamiento ambulatorio, pero que no presentan complicaciones con peligro inminente tal, que requieran cuidados intensivos como contusión cerebral no severa, fracturas craneales, hemorragia subaracnoidea postraumática, convulsiones postraumáticas, agitación psicomotora, excitación, infecciones del sistema nervioso central (SNC), infarto, espasmo u oclusión vascular cerebral postraumática.
En la contusión cerebral no severa, se realiza la prevención del síndrome de insuficiencia respiratoria agudo, uso de deshidratantes cerebrales, prevención del déficit nutricional, cuidados generales de enfermería, antibióticos si infecciones y analgésicos.
En las fracturas craneales lineales, reposo, analgésicos, observación para detectar signos de déficit o irritación del sistema nervioso central (SNC), antibióticos en caso de otorragia o heridas.
En la hemorragias subaracnoideas postraumáticas luego de realizado una tomografía axial computerizada (TAC) y fondo de ojo, algunos plantean que se puede realizar punción lumbar, acostado en decúbito lateral, y se realiza drenaje lento de 10 a 20 ml de líquido cefalorraquídeo (LCR). Puede repetirse si persiste la cefalea. No debe realizarse si se sospecha presión intracraneal (PIC) muy alta, por el peligro de enclavamiento. En mi experiencia personal prefiero en estos casos no realizar punción lumbar. Además debe realizarse tratamiento contra el edema cerebral con deshidratantes.
Las convulsiones postraumáticas se controlan con diazepan 10 miligramos intravenoso lento o fenobarbital 100 a 200 miligramos intravenoso durante la crisis y continuar por vía oral 100 a 400 miligramos por día, la fenitoína sódica 125 miligramos cada 8 horas intravenoso, o 100 miligramos cada 8 horas por vía oral, en niños a razón de 6 a 10 miligramos por kilogramo de peso día.
Si no se controlan las convulsiones trasladar el paciente a UCI, para tratamiento con tiopental o pentobarbital y realizar control respiratorio.
La agitación psicomotora o excitación, después de descartar como posibles causas, la elevación de la presión intracraneal, embolismo graso, globo vesical u otra causa de dolor, se inicia la sedación con diazepan 10 miligramos o fenobarbital 100 a 200g intravenoso o intramuscular.
En las infecciones del sistema nervioso central (SNC) se inicia el tratamiento antibiótico, se ha usado mucho la tríada de antibióticos compuesta por penicilina, cloranfenicol y sulfamidas.
En el caso de infarto, espasmo u oclusión vascular cerebral postraumática, se inicia tratamiento con dextrán en solución al 20%, 500 ml intravenoso en una hora y continuar con 500ml cada 12 horas durante 3 días y tratamiento del edema cerebral.
El embolismo graso debe sospecharse en pacientes con fracturas de huesos largos o grandes contusiones de tejidos blandos que presentan agitación psicomotora, trastornos respiratorios como la polipnea, taquicardia, en los cuales se buscaran, corpúsculos grasos en la orina, biopsia del coágulo para buscar corpúsculos grasos. En caso positivo, se solicitará traslado a la UCI para tratamiento con anticoagulantes, corticoides y cuidados respiratorios.
Tratamiento médico y seguimiento del traumatismo encefalocraneal (TEC) por consulta externa.
Generalmente el seguimiento por consulta externa de neurocirugía se realiza en pacientes sintomáticos, por las secuelas de los traumatismos encefalocraneales (TEC), hasta mejorar, recuperar o estabilizar el cuadro clínico o por las posibles complicaciones que puedan aparecer durante un periodo de tiempo determinado, una vez realizado el control y comprobado que el paciente ha evolucionado de forma aceptable y está libre de riesgos o complicaciones, es posible valorar el alta y concluirlo por neurocirugía.
A los pacientes que presenten secuelas crónicas y permanentes, se remitirán a su área de atención en salud donde residan, donde tendrán un seguimiento por el médico general, con el cuadro clínico estabilizado.
En caso necesario por sus discapacidades, se remitirá a un centro especializado en rehabilitación y valoración fisioterapeuta, indicando terapias físicas, del lenguaje, ocupacional, integrales, según sea el caso. Asimismo será valorado por medicina laboral en un tiempo oportuno para definir su situación laboral según su grado de discapacidad parcial, total, temporal o permanente.
Fundamentación farmacológica del porque se han empleado en el tratamiento de los TEC graves los barbitúricos y antiagregantes plaquetarios.
Hace algunos años, varios autores preconizaron tratamientos basados en la oxigenación temprana, la combinación de deshidratantes cerebrales, el uso de antiagregantes plaquetarios y el empleo en distintas dosis de barbitúricos, en los pacientes con traumatismos encefalocraneales (TEC) graves e hipertensión endocraneana aguda.
La isquemia por hipertensión endocraneana aguda o por lesión vascular, puede provocar la liberación de catecolaminas, ácido araquidónico, tromboxano (TXA) y ADP, estas sustancias activan las plaquetas y pueden provocar obstrucción vascular por agregación plaquetaria.
Después de un traumatismo encefalocraneal (TEC), en ocasiones se producen alteraciones de la circulación cerebral, relacionables con coagulación intravascular diseminada y con disminución de la deformabilidad de los eritrocitos, es decir, de su capacidad para adaptarse al diámetro de los capilares cerebrales, con importante compromiso de la perfusión sanguínea cerebral.
Estas complicaciones, que posiblemente ocurren con más frecuencia que las ocasiones en que son diagnosticadas y tratadas, en pacientes con traumatismo encefalocraneal (TEC) o hematomas intracraneales, pudieran aliviarse con los efectos de la hemodilución, antitrombótico y desagregante del dextrano y otros medicamentos.
Hace más de 35 años la investigación de los lípidos llevo al descubrimiento de las prostaglandinas. Estos derivados de los ácidos grasos, se dividen en grupos de compuestos con importante actividad biológica, algunos con acción fisiológica y farmacológica sobre la circulación cerebrovascular, la función hipotalámica, la neurotransmisión y la actividad nociceptiva.
Mientras que otros compuestos mediadores y moduladores (neurotransmisores) como la acetilcolina, la norepinefrina y la dopamina, se mantienen preformados y almacenados dentro de las células, las prostaglandinas se sintetizan y liberan en respuesta a varios estímulos activadores.
La cantidad y tipo de prostaglandinas sintetizadas, depende de varios factores, entre los que se encuentra el tipo de estímulo (trauma, isquemia, catecolaminas).
En el ser humano, las prostaglandinas se biosintetizan, principalmente, a partir de dos precursores que se encuentran en las células, que son el ácido eicosatrienoico para las series de prostaglandinas monosaturadas y el ácido araquidónico o ácido eicosatetraenoico, de mayor interés para nuestro tema, por ser el precursor de la serie 2 de las prostaglandinas bi- insaturadas.
El ácido araquidónico puede ingerirse preformado en los alimentos, o derivarse del ácido linoleico, este último se encuentra en las carnes y aceites vegetales.
Los ácidos grasos de la dieta, se unen a la albúmina y se incorporan como los componentes de los fosfolípidos y ésteres del colesterol dentro de la membrana celular y de estructuras subcelulares.
En respuesta a estímulos mecánicos, químicos u hormonales, se activa la enzima fosfolipasa, que libera al ácido araquidónico de los fosfolípidos celulares. La oxidación del ácido araquidónico por la ciclooxigenasa, crea los intermediarios endoperóxidos cíclicos PGG2 y PGH2, que tienen efectos vasculares potentes y pueden, por si mismos, causar agregación plaquetaria, a pesar de su corta vida media de aproximadamente 5 minutos.
En el tejido cerebral, cardíaco en los fibroblastos pulmonares, bazo, leucocitos polimorfonucleares y en las plaquetas, el endoperóxido cíclico PGG2, puede ser convertido en tromboxano (TX A2), mediante la enzima tromboxano sintetasa. El principal metabolito producido por las plaquetas, es el TXA2.
Por otro lado, el endotelio vascular, el tejido cardíaco y otros pueden convertir el endoperóxido cíclico PGG2 en PG12 (prostaciclina), mediante la prostaciclina sintetasa. Las arterias y arteriolas intracraneales sintetizan cantidades importantes de prostaciclinas.
El tromboxano (TXA2) y la prostaciclina (PG12), tienen acciones opuestas en relación a la circulación cerebral.
El balance entre dos prostaglandinas con acción antagonista, determina la fisiología vascular resultante.
El tromboxano, es el más potente constrictor de arterias sintetizado por el organismo y es, además, promotor de la agregación plaquetaria.
En respuesta a la disrupción de endotelio vascular o de otros estímulos humorales, las plaquetas interactúan con el colágeno subendotelial, para liberar adenosindifosfato (ADP) y activar la ruta biosintética del ácido araquidónico, para producir TXA2. El TXA2 y el ADP promueven la agregación plaquetaria y la contracción de la musculatura de la capa media vascular.
La prostaciclina PG12, relaja la musculatura lisa vascular y es el más potente inhibidor endógeno de la agregación plaquetaria.
La prostaciclina puede producir desagregación plaquetaria en el ser humano y vasodilatación, enrojecimiento facial, elevación de la temperatura de la piel y dispersión de agregados plaquetarios circulantes cuando se infunde de forma intravenosa.
Se investiga el empleo de inhibidores de algunas de las etapas de la cadena metabólica del ácido araquidónico, para definir las funciones de las prostaglandinas como mediadores y para determinar sus posibilidades farmacológicas, en la terapéutica de varias enfermedades neurológicas, entre las que se encuentran algunas complicaciones de los traumatismos encefalocraneales (TEC), así como, también, el vasoespasmo secundario a las hemorragias subaracnoideas, las cefaleas migrañosas, los accidentes vasculares encefálicos, los traumas raquimedulares y otras.
Los corticoides, son capaces de limitar la liberación del ácido araquidónico, por inhibición de la enzima fosfolipasa. Pero esta inhibición, requiere la síntesis de una proteína específica, que es producida por las células del endotelio vascular, pero no por las plaquetas. Por lo tanto, los corticoesteroides pueden interferir la producción de la prostaciclina (PG12), pero no la de tromboxano (TXA2).
La enzima fosfolipasa, puede también ser inhibida por la indometacina, la cloropromacina y por anestésicos locales al parecer, por interferencia en las uniones con el calcio e interactuando con los fosfolípidos, para prevenir la acción hidrolítica de la enzima.
Los barbitúricos parecen tener acción inhibidora tanto sobre los radicales libres que afectan los fosfolípidos de la membrana celular, como sobre la peroxidación de los ácidos grasos libres por la enzima ciclooxigenasa.
La aspirina y otras drogas antiinflamatorias como la indometacina y el ibuprofeno, también inhiben la enzima ciclooxigenasa.
La aspirina puede bloquear la producción del tromboxano por el tiempo de vida de las plaquetas sobre las que actúan al impedirles, de forma irreversible, su posibilidad de sintetizar proteínas.
Mientras que las células endoteliales recuperan su capacidad de síntesis de la enzima ciclooxigenasa para producir prostaciclina, antes de 36 horas.
Por supuesto, contrariamente a los barbitúricos pueden existir ciertas limitaciones para el empleo de la aspirina, en algunos pacientes con determinados traumatismos o hematomas intracraneales, por el peligro de los sangramientos.
El dipiridamol, parece tener una débil acción vasodilatadora y modifica e inhibe la capacidad de las plaquetas para adherirse al endotelio dañado, pero estructuralmente intacto, al mantener el AMP (adenosinmonofosfato) en su forma cíclica, estimulando su producción enzimática y reduciendo su degradación.
Cuando los niveles de AMP cíclico descienden, se liberan iones de calcio, que activan las plaquetas, pierden su forma discoide, desarrollan seudópodos y pueden adherirse a las paredes de los vasos.
La dosis recomendada es de 100 miligramos por día, por vía oral ó 10 miligramos por día vía intravenosa, no provoca alteraciones de los mecanismos hemostáticos, durante o después de la cirugía, ya que cuando el endotelio está lacerado, libera endoperóxido que garantiza los niveles de tromboxano.
Hoy en día, existen drogas con capacidad selectiva de inhibición de la enzima tromboxano sintetasa, como el imidazol.
También se han empleado prostaglandinas exógenas en estudios clínicos, que confirman su influencia en la fisiología del flujo sanguíneo cerebral, en sentido positivo o negativo, según su efecto vasodilatador (PGE1; PG12) o vasoconstrictor (TXA2, PGF2); así como respuestas contrapuestas al mismo medicamento, en dependencia de la dosis empleada, lo que puede representar acción sobre dos diferentes receptores.
Las combinaciones de inhibidores, pueden tener efectos favorables en algunas complicaciones o consecuencias de la isquemia cerebral.
Con estos elementos como consideración, en los pacientes en que se sospecha una elevación importante de la presión intracraneal (PIC) o isquemia cerebral por medición mecánica o por evidencias clínicas y después de descartar por tomografía computarizada u otros medios la presencia de colecciones intracraneales con efecto de masa, recomendamos el empleo de tiopental de dosis bajas y de antiagregantes plaquetarios como adición a los procedimientos anteriormente descritos, el uso de deshidratantes cerebrales y mantener la normotermia corporal, mantener la presión sistólica inferior a 160 mm de Hg y el monitorage continuo de la presión intracraneal (PIC).
Tiopental: de 3 a 6 miligramos por kilogramo de peso en bolo (por anestesista) y continuar con 1 g disuelto en dextrosa al 5% en infusión intravenosa cada 12 horas.
Dextrano en solución al 20% 500 ml. vía intravenosa en 1 hora y continuar con 250 ml cada 6 horas, durante 3 o más días.
Tratamiento de la agitación psicomotora.
Después de descartar como posibles causas una elevación de la presión intracraneal; embolismo graso; retención urinaria con globo vesical u otra causa de dolor: sedación con Diazepam 10 miligramos vía intravenosa (iv), o fenobarbital 100-200 miligramos vía intravenosa (iv) o vía intramuscular (im), o el midazolan (dormicun) en dosis bajas 1 miligramo vía intravenosa (iv) se debe administrar lentamente.
Profilaxis en los encefalocraneales (TEC).
La prevención del traumatismo encefalocraneal (TEC) debe estar centrada en su mayor parte en evitar los accidentes de tránsito y sus causas. En este sentido, todos los esfuerzos deberían estar dirigidos a educar correctamente a la población sobre los efectos devastadores del TEC tanto en el ámbito personal como familiar y social. El control estricto por parte de las autoridades competentes de los límites de velocidad, de las tasas de alcoholemia de los conductores y del uso adecuado de las medidas obligatorias de seguridad (cinturones, airbags y cascos en los motoristas) han demostrado ser eficaces al reducir tanto el número como la gravedad de los encefalocraneales (TEC).
ALIMENTACIÓN DE LOS PACIENTES CON TRAUMATISMO ENCEFALOCRANEAL (TEC).
Se recomienda en el proceso de alimentación de los pacientes con encefalocraneales (TEC) graves que hacia el 7mo día de la injuria traumática, se debe haber restituido lo siguiente (por vía entérica o parenteral): los pacientes no paralizados: 140% del gasto energético basal y en los pacientes paralizados el 100% del gasto energético basal, proporcional más del 15% de las calorías como proteínas, la restitución debe comenzar dentro de las primeras 72 horas desde el traumatismo a fin de cumplir con lo recomendado anteriormente.
Si bien la restitución calórica es similar, sea que se emplee la vía entérica o la parenteral, se prefiere la hiperalimentación endovenosa si se desea un mayor aporte de nitrógeno o si hay alteraciones del vaciado gástrico.
Justificación.
Necesidades calóricas: los pacientes comatosos que han sufrido un traumatismo encefalocraneal (TEC) tienen un gasto metabólico que supera al normal en 140% con un margen entre 120 y 250%. Los bloqueantes musculares o los barbitúricos reducen este exceso en la mayoría de los casos aún 100 o 120% de lo normal, pero en algunos se sigue registrando un exceso de un 20 a un 30%.
Las necesidades de energía suben durante las primeras dos semanas posteriores a la injuria, pero se desconoce cuánto tiempo persiste ese aumento. El índice de mortalidad se reduce en quienes, hacia el 7mo día, ya están recibiendo restitución calórica completa. Puesto que generalmente alcanzar este nivel nutricional le lleva dos o tres días, sea que se emplee la vía parenteral o la entérica para acelerar el proceso, se recomienda comenzar con la alimentación 72 horas después del traumatismo.
No se hallaron diferencias significativas en la albúmina sérica, adelgazamiento, balance nitrogenado, incidencia de infecciones y evolución clínica entre la nutrición entérica y la parenteral.
Para calcular el gasto energético basal (GEB), también denominado requerimiento energético basal, se puede emplear la ecuación de Harris – Benedict, que aparece a continuación, en las que P corresponde al peso en kilogramos, A corresponde a la altura en centímetros y E corresponde a la edad en años.
- Varones: gasto energético basal (GEB) = 66,47 + 13,75 x P + 5,0 x A – 6.76 x E.
- Mujeres: gasto energético basal (GEB) = 65,51 + 9,56 x P + 1,85 x A – 468 x E.
- Lactantes: gasto energético basal (GEB) = 22,1 +31,05 x P +1,16 x A.
Nutrición por sonda nasogástrica.
Las soluciones isotónicas como son el Osmolite y el Isocal deben administrarse sin diluir (20) comenzado a 30 ml por hora. Se debe verificar el residuo gástrico cada 4 horas y detener la alimentación si supera 125 ml en un adulto. Se aumenta la velocidad en 15 o 25 ml por hora cada 12 o 24 horas según lo tolere el paciente hasta llegar a la deseada. Como se ha expuesto previamente, no se recomienda diluir estas soluciones porque pueden lentificar el vaciado gástrico pero, si por algún motivo resulta necesaria la dilución, debe emplearse solución fisiológica para reducir el aporte de agua pura.
Precauciones: la nutrición por sonda nasogástrica puede interferir en la absorción de la fenitoína. En los traumatizados, es frecuente observar un retraso del vaciado gástrico, por el contrario, algunos pacientes pueden presentar aumento transitorio del vaciado y, al igual que en el coma barbitúrico, puede ser necesario administrar hiperalimentación endovenosa hasta que la vía entérica pueda volver a utilizarse. Otros han descrito un mejor tolerancia al nutrición mediante yeyunostomía. En nuestro medio es utilizada con éxito.
Balance nitrogenado: como cálculo estimado, por cada gramo de nitrógeno eliminado principalmente en la orina pero también en la materia fecal, se catabolizan 6,25 miligramos de proteínas. Se recomienda restituir al menos 15% de las calorías como proteínas. Es posible calcular el porcentaje de calorías consumidas (PCC) a partir de las proteínas utilizando la siguiente ecuación, en el que la N corresponde al nitrógeno en gramos y GEB corresponde al gasto energético basal.
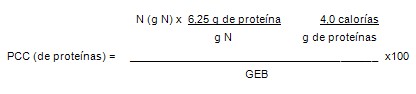
Por lo tanto, para administrar el porcentaje de calorías consumidas (proteínas) = al 15% una vez que se conoce el gasto energético basal (GEB) se emplea la siguiente ecuación. Algunas preparaciones para la vía entérica utilizada en los EEUU son el magnatal (porcentaje de calorías consumidas = 14%) y traumacal (porcentaje de calorías consumidas = 22%).
N (g) = 0,006 x GEB.
Prevención del déficit nutricional.
La dieta se prepara para pasarla por una sonda nasogástrica o por vía intravenosa, con los siguientes elementos.
- Calorías, 40 por kilogramo de peso corporal, puede elevarse hasta 80 calorías por kilogramo de peso corporal en caso de hipoxia, hipovolemia, infección o dolor intenso.
- Proteínas, 2 gramos por kilogramo de peso corporal.
- Vitaminas, en forma de jugos naturales de frutas, tabletas de polivitaminas o por vía intravenosa.
En pacientes que no puedan alimentarse por vía oral, pasada una semana es recomendable realizar gastrotomía para garantizar una alimentación sólida y balanceada con el apoyo de la nutricionista.
TRATAMIENTO QUIRÚRGICO DEL TRAUMATISMO ENCEFALOCRANEANO.
Dentro del tratamiento quirúrgico del traumatismo encefalocraneal (TEC) existen operaciones diagnósticas y operaciones más específicas como tratamiento, pues ya tienen un diagnóstico preciso, generalmente por una tomografía axial computerizada (TAC) de cráneo, y que requieren de una cirugía urgente.
Operaciones diagnósticas.
Una craneotomía o trépanos exploratorios, en los pacientes en que sospeche colección intracraneal que provoque hipertensión endocraneana, compresión cerebral, con signos de herniación cerebral y que, por motivos de tiempo, condiciones del paciente o posibilidades técnicas, no pueda ser sometido a exámenes especiales de certeza diagnóstica. Generalmente se realizarán agujeros de trépanos en regiones temporal, frontal y parietal en el mismo lado de la midriasis, si hay anisocoria contralateral a la hemiplejía, si la hay o no, en su defecto, se deben realizar, en la zona del traumatismo directo o fractura. Después, siempre debe realizarse uno o dos agujeros de trépano contralateralmente.
Operaciones como tratamiento.
En los pacientes que lo requieran, que tienen un diagnóstico con indicación de cirugía craneoencefálica, ya sea clínico o por estudios especiales (tomografía axial computerizada (TAC) de cráneo, resonancia magnética nuclear (RMN), RX de cráneo, angiografía cerebral).
La efectividad del tratamiento quirúrgico en el pronóstico de los pacientes depende, en primer lugar, de que se realice, inmediatamente después del diagnóstico precoz, la evacuación del hematoma u otras masas que provoquen aumento de la presión intracraneal (PIC), o desplazamiento de las estructuras de la línea media mayor de 5mm. En pacientes con áreas de necrosis, contusión hemorrágica y edema, principalmente en las puntas de los lóbulos frontales y temporales, está indicada la descompresión interna, exéresis generosa de las áreas lesionadas y cierre de la duramadre.
En otros pacientes, en quien no se encuentran áreas definidas de lesión importante ni masas intracraneales anormales, pero si visualmente un aumento de presión intracraneal (PIC) y compresión de encéfalo por la duramadre y el cráneo, puede ser útil en algunos casos que no han mejorado con el tratamiento médico y la terapia neurointensiva, la descompresión externa, craniectomía descompresiva amplia y apertura de la duramadre.
Lo relativo a la técnica quirúrgica de estos pacientes lo abordaremos más adelante.
Otros procederes de diagnóstico y tratamiento requeridos se realizaran preferiblemente en la Unidad de Cuidados Intensivos como colocar catéteres venosos y arteriales profundos para control del volumen circulatorio y medir la presión venosa central, intubación endotraqueal, asistencia o control ventilatorio, colocar dispositivos para la medición continua de la presión intracraneal (PIC).
Agujeros de trepanación exploratorios.
En los pacientes que sufrieron un traumatismo, la tríada clínica compuesta por (1) alteración del estado mental, (2) dilación pupilar unilateral y arreflexia pupilar, y (3) hemiparesia contralateral generalmente es producto de una hernia uncal transtentorial que comprime el sector superior del tronco encefálico que, en la mayoría de los casos, se debe a su vez a un hematoma intracraneal extraxial.
El pronóstico de los pacientes que tienen una hernia traumática es poco auspicioso, pero si se realiza una descompresión precoz, es posible mejorar el pronóstico, que incluso es mucho mejor cuanto más rápidamente se efectúa la descompresión.
Cuando hay sospechas fundadas de que la causa de la descompensación es un hematoma, puede plantearse la necesidad de efectuar agujeros de trepanación exploratorios.
Los agujeros de trepanación son, ante todo, una herramienta de diagnóstico, ya que la mayoría de los hematomas agudos son demasiado sólidos para que sea posible extirparlos a través de ellos. Aún así, si el agujero muestra la existencia de un hematoma, es posible realizar una descompresión mínima, y luego llevar a cabo una craneotomía incorporando el agujero o los agujeros ya realizados. De todos modos, en el mejor de los casos se logra una recuperación satisfactoria que solo llega al 20%.
Gracias a la amplia disponibilidad actual de la tomografía axial computerizada (TAC), es infrecuente que sea necesario abrir agujeros de trepanación exploratorios.
Indicaciones.
1. Criterios clínicos: deterioro del estado neurológico. Indicaciones para realizar los agujeros en la sala de urgencia (infrecuentes): casos de pacientes que se están muriendo a causa de una hernia transtentorial rápida o de compresión del tronco encefálico que no mejoran ni se estabilizan con el manitol e hiperventilación.
Indicadores de la presencia de una hernia transtentorial o de compresión del tronco encefálico:
- Caída abrupta en el puntaje de la escala de Glasgow para coma (EGC).
- Una pupila que se dilata y deja de responder a la luz.
- Parálisis o descerebración (generalmente, contralateral a la dilatada y arreactiva).
- Situaciones recomendadas en las que deben aplicarse los criterios anteriores:
- Cuando hay pruebas de que los pacientes que tenían un estado neurológico estable se deterioraron como ya se ha descrito.
- En los pacientes alertas que sufren el mismo proceso cuando son trasladados y el personal médico o paramédico tiene pruebas que atestiguan esos cambios.
2.- Otros criterios
Algunos pacientes que deban ser operados de urgencia por traumatismos sistémicos (por ejemplo, lavado peritoneal positivo + inestabilidad hemodinámica) cuando no hay tiempo de obtener una tomografía axial computerizada (TAC) de cerebro.
Tratamiento.
Es controvertido el uso de los agujeros de trepanación como tratamiento. Las consideraciones expuestas a continuación sólo son pautas generales:
1.ĀĀĀĀ Si el paciente cumple con los criterios ya descritos (operación de urgencia a causa de traumatismos sistémicos o deterioro que no mejora con manitol ni hiperventilación) y no es posible realizar una tomografía axial computerizada (TAC) e interpretarla de inmediato, el tratamiento no debe retrasarse para obtener la tomografía axial computerizada (TAC).
A.ĀĀĀ En general, si el quirófano está disponible de inmediato, es preferible abrir los agujeros de trepanación allí (porque se dispone del equipo necesario para realizar una craneotomía, tanto la iluminación como la esterilidad son mejores, está disponible una enfermera asistente entrenada, entre otros), sobre todo en los adultos (> 30 años) que no hayan sido víctima de un accidente de tránsito. Así, es probable que sea más rápido el diagnóstico y tratamiento de los hematomas extraxiales en los casos de hernia, aunque no se ha comprobado que exista ninguna diferencia fehaciente en la evolución posterior.
B.ĀĀĀ Si se prevé que el quirófano no va estar disponible inmediatamente, puede decidirse realizar los agujeros de trepanación de urgencia en la sala de emergencias misma.
2.ĀĀĀĀ La realización de los agujeros de trepanación se describe en la sección técnica.
Posición del paciente.
Se gira la cabeza del paciente de forma tal que el lado que se va a explorar quede hacia arriba y se le coloca una almohadilla bajo el hombro. Se utiliza fijación del cráneo de tres puntos si existe la sospecha de que pueda haber un aneurisma o una malformación arteriovenosa (para poder utilizar retractores autoestáticos y obtener inmovilidad del campo quirúrgico) o si es necesario estabilizar la columna (por ejemplo, en los casos de fracturas cervicales inestables). De lo contrario, es suficiente con colocar un sostén en herradura, que ahorra tiempo y permite un acceso rápido al lado contralateral si llega a ser necesario.
Elección del lado donde abrir el primer agujero de trepanación.
Es recomendable comenzar con un agujero temporal (ver más adelante)
- Del lado homolateral a la pupila dilatada y arreactiva. De este modo, el lado será correcto en más del 85% de las lesiones ocupantes epidurales y otras lesiones extraxiales.
- Si ambas pupilas están dilatadas, utilizar el lado de la pupila que se dilató en primer lugar (si se tiene conocimiento).
- Si las pupilas están iguales, o si se desconoce cuál se dilató primero, es conveniente hacer el agujero del lado donde es evidente el traumatismo externo.
- Si no hay signos localizadores, se lo debe realizar del lado izquierdo (a fin de evaluar y descomprimir el hemisferio que se cree es el dominante)
Abordaje.
Los agujeros de trepanación se realizan a lo largo de un trayecto que los conecte a fin de poder formar un “colgajo para evacuar un hematoma” si llega a ser necesario realizar una craneotomía.
La denominación “colgajo por hematoma traumático“ se debe a que proporciona acceso amplio a casi toda la convexidad cerebral, lo cual permite evacuar por completo los coágulos hemáticos y detener gran parte de la hemorragia si persiste.
En primer lugar, se traza el colgajo con un marcador cutáneo:
1.ĀĀĀĀ Se comienza en el arco cigomático a menos de 1 cm anterior al trago (así, no se corre el riesgo de dañar el ramo del nervio facial que inerva el músculo frontal ni la rama anterior de la arteria temporal superficial).
2.ĀĀĀĀ Se sigue hacia arriba y luego se hace una curva hacia atrás a la altura del vértice superior del pabellón auricular.
3.ĀĀĀĀ A 4 - 6 cm detrás de la oreja se sigue hacia arriba.
4.ĀĀĀĀ A 1 - 2 cm de la línea media (seno longitudinal superior) se hace una curva hacia delante y se termina detrás del nacimiento del cabello.
Técnica quirúrgica.
Ubicación de los agujeros de trepanación.
1.ĀĀĀĀ Primer agujero de trepanación (temporal) sobre la fosa craneal media, justo por encima del arco cigomático. Este agujero proporciona acceso a la fosa media (que es el lugar donde es más frecuente que se forme un hematoma epidural y, por lo general, permite acceder a los hematomas subdurales de la convexidad, así como a la arteria meníngea media de la región pterional).
2.ĀĀĀĀ De no hallar un hematoma epidural, se abre la duramadre si ésta presenta una coloración azulada (signo que sugiere la presencia de un hematoma subdural). O si existe una sospecha fundada de que en ese lado hay una lesión ocupante.
3.ĀĀĀĀ Si la exploración es completamente negativa, se realiza otro agujero temporal del lado contralateral.
4.ĀĀĀĀ Si éste también es negativo, es necesario completar con otros orificios como se hizo en el hemisferio contralateral si no es posible realizar una tomografía axial computerizada (TAC) en ese momento.
5.ĀĀĀĀ Primero se completa con un agujero frontal.
6.ĀĀĀĀ Después, se efectúa un agujero parietal y, por último, en la fosa posterior.
En un estudio realizado en 100 pacientes que habían sufrido traumatismo y que, como consecuencia, presentaron hernia transtentorial o comprensión del tallo cerebral, los agujeros de trepanación bilaterales temporales, frontales y parietales, todos realizados en el quirófano, fueron positivos en el 56% de los casos.
Los índices son menores entre los menores de 30 años y quienes tenían una malformación arteriovenosa (MAV) en comparación con los efectuados por caídas o golpizas.
Los hematomas subdurales son las lesiones ocupantes extraxiales más frecuentes (son únicos y unilaterales en el 70%, bilaterales en el 11% y están asociados a hematomas epidurales o intracerebrales en un 10% de los pacientes).
En los casos de exploraciones positivas, el primer orificio estuvo del lado correcto en el 86% de las veces cuando se lo realizó siguiendo las recomendaciones anteriores. Seis pacientes tenían hematomas extraxiales importantes que no fueron descubiertos mediante agujeros de trepanación (probablemente porque la exploración fue incompleta). Sólo 3 pacientes tuvieron los signos neurológicos descritos como consecuencia de hematomas intraparenquimatosos.
La evolución clínica en un tiempo promedio de seguimiento de 11 meses con un margen entre el primer mes y 37 meses se comporto de la siguiente forma.
Fallecieron 70 de los 100 pacientes: No fue posible atribuir ningún tipo de morbimortalidad a los agujeros de trepanación. En 4 pacientes que tuvieron una buena evolución y en 4 que presentaron una incapacidad moderada fue positiva la exploración mediante agujeros de trepanación.
Tratamiento médico quirúrgico de las fracturas de cráneo.
Las fracturas hundidas de cráneo tienen criterios que indican elevarlas que son: que sean mayor de 8 a 10 mm el hundimiento o mayor el grosor que el cráneo, que tenga un déficit vinculado al cerebro subyacente, que tenga pérdida de líquido cefalorraquídeo (LCR) por laceración dural o que sea una fractura abierta y hundida, una fractura abierta es una fractura compuesta.
No se ha demostrado que elevar una fractura hundida de cráneo reduzca la aparición posterior de convulsiones postraumáticas, que probablemente estén más relacionadas con el traumatismo encefalocraneal (TEC) inicial, con excepción de los siguientes casos: puede ser peligroso elevar las fracturas hundidas cuando están superpuestos o se comprimen algunos de los senos durales, o si el paciente tiene un estado neurológico indemne y no hay indicaciones de efectuar una intervención, como por ejemplo, cuando hay una pérdida del líquido cefalorraquídeo (LCR) que exige tratamiento quirúrgico. Si no es así, conviene instituir tratamiento conservador inicial.
En el tratamiento de las fracturas de la base del cráneo si es necesario utilizar una sonda nasogástrica, este proceder debe ser con precaución: ya que se corre el riesgo de pasar la sonda nasogástrica hacia dentro de cráneo, lo cual está asociado a una evolución fatal en el 65 a 70% de los casos. Entre las causas posibles cabe mencionar que: la lámina cribosa puede ser delgada por causas congénitas o por sinusitis crónica o esta lesionada a causa de una fractura frontal de la base del cráneo o de una fractura conminuta.
Las contraindicaciones sugeridas para la colocación a ciegas de una sonda nasogástrica, son entre otras, la sospecha de que hay una fractura fronto-orbitaria, la presencia o los antecedentes de rinorraquia y la meningitis en curso acompañada de sinusitis crónica.
La antibioticoterapia preventiva.
Es controvertido el uso de antibióticos como tratamiento preventivo de rutina, aunque se halle una fístula de líquido cefalorraquídeo (LCR). Aún así, la mayoría de los otorrinolaringólogos recomiendan tratar las fracturas que comprometen lo senos nasales como si se tratara de fracturas contaminadas administrando antibióticos de amplio espectro como por ejemplo la ciprofloxacina durante 7 a 10 días.
En los pacientes con fracturas de la base del cráneo, en la mayoría de los casos, no es necesario tratar la fractura en si, pero puede llegar a ser necesario tratar algunas afecciones que se asocian a estas fracturas, como son los aneurismas traumáticos, las fístulas carótido - cavernosas postraumáticas y las fístulas de LCR.
En casos de rinorraquia persistente, puede ser necesario un tratamiento quirúrgico.
Las meningoencefalitis o los abscesos cerebrales: pueden aparecer cuando la fractura de la base se extiende hacia los senos aéreos frontales o mastoideos, aunque no haya pérdida de líquido cefalorraquídeo (LCR).
Pueden aparecer años después de ocurrida la fractura, deformidades estéticas y parálisis facial postraumática como consecuencia de las fracturas del peñasco.
Cuando aparece una parálisis facial postraumática unilateral o bilateral el tratamiento puede verse complicado por la presencia de traumatismos múltiples entre ellos el traumatismo encefalocraneal (TEC) severo en cuyo caso es necesario intubar al paciente, lo que no permite definir con certeza el momento en que se inicio la parálisis.
Independiente de cuando se haya iniciado la parálisis facial postraumática muchos utilizan los glucocorticoides, pero resta demostrar su eficacia.
En estos casos se debe realizar una interconsulta con un otorrinolaringólogo.
Cuando ocurre una instalación de inicio de una parálisis facial periférica unilateral: la electromiografía facial también denominada electroneurografía, tarda al menos 72 horas en mostrar alteraciones.
En general se recomienda realizar un seguimiento clínico, ya que estos pacientes pueden ser sometidos a una descompresión quirúrgica del séptimo par craneal si los corticoides no generan mejoría. El momento indicado para operar está muy discutido, pero no suele realizarse como tratamiento de urgencia.
Cuando ocurre una instalación tardía de una parálisis facial periférica: si en las electroneurografías seriadas se detecta deterioro nervioso a pesar de que el paciente este recibiendo glucocorticoides y la actividad cae a menos del 10% del lado contralateral, cabe considerar el tratamiento mediante descompresión quirúrgica, que actualmente es controvertido, pero se considera que mejora la recuperación entre un 40% hasta un 75% de los casos.
En el caso de la aparición de un neumoencéfalo postraumático por una fractura craneal hay que tener en cuenta que cuando se debe a microorganismos productores de gases, se inicia primero el tratamiento de la infección y luego se encara el neumoencéfalo.
El tratamiento del neumoencéfalo simple de causas no infecciosas depende de si existe la sospecha o no de que haya una pérdida de líquido cefalorraquídeo (LCR). Si no hay pérdida de LCR, el aire se reabsorbe espontáneamente con el paso del tiempo y, si el efecto de masa no es acentuado, es acertado seguir el caso mediante observación.
Si existe la sospecha de que hay una pérdida de líquido cefalorraquídeo (LCR), el tratamiento es el mismo que se instituye ante cualquier fístula de LCR.
Los neumoencéfalos tensionales persistentes deben ser evacuados como una urgencia, similar a la de un hematoma intracraneal. La mejoría puede ser rápida y asombrosa cuando se libera el aire bajo presión. Las opciones de tratamiento consisten en realizar nuevos agujeros de trepanación o insertar una aguja de punción lumbar a través de uno realizado anteriormente por una craneotomía.
En el tratamiento de las fístulas de líquido cefalorraquídeo (LCR) postraumáticas, en la etapa aguda del traumatismo encefalocraneal (TEC) se justifica realizar observación del paciente, ya que en la mayor parte de los casos se detiene espontáneamente.
La profilaxis antibiótica es polémica. No se hallaron diferencias en la incidencia o la morbilidad de las meningitis entre los pacientes sometidos a tratamientos y aquellos que no recibieron ninguna terapia. Además, el riesgo de seleccionar cepas resistentes parece real y, por lo tanto, suele evitarse la antibioticoterapia.
El tratamiento consiste en tomar medidas para bajar la presión intracraneal (PIC), reposo absoluto, evitar el estreñimiento utilizando laxantes, aconsejarle al paciente que no se suene la nariz ni estornude, administrar acetazolamida 250 miligramos por vía oral 4 veces al día para disminuir la producción de líquido cefalorraquídeo (LCR) y la restricción leve de líquidos.
Si persiste la filtración en primer lugar descartar la hidrocefalia obstructiva por tomografía axial computerizada (TAC) o resonancia magnética nuclear (RMN), realizar una punción lumbar diaria o dos veces al día si es preciso para reducir la presión hasta igualarla a la presión atmosférica o hasta que el paciente manifieste cefalea, o bien colocar un drenaje lumbar continuo utilizando un catéter percutáneo. Mantener la cabecera de la cama elevada a 10 o 15 ║ y la cámara cuentagotas a nivel de los hombros la cual se deberá bajar si persiste la filtración. Este procedimiento requiere internación en la UCI.
Si el paciente se deteriora con el drenaje colocado, detener el drenaje inmediatamente, ubicar al paciente en posición horizontal plana sobre la cama o con una leve inclinación de Trendelemburg, iniciar oxigenación con oxígeno al 100%, obtener una tomografía axial computerizada (TAC) o una radiografía de cráneo con equipos portátil para descartar un neumoencéfalo tensional causado por la entrada de aire.
Operaciones en las fracturas cerradas del cráneo.
Indicaciones y contraindicaciones.
En las fracturas cerradas del cráneo, es decir, cuando estas no se acompañan de las heridas de las partes blandas epicraneanas, la intervención quirúrgica está indicada si existe fractura deprimida.
El grado de hundimiento debe precisarse por el examen radiográfico y sobre todo por vistas tangenciales al foco de la fractura.
La operación debe practicarse lo más precoz posible si lo permite el estado general del paciente. En casos de fracturas lineales o múltiples, sin datos radiológicos de hundimiento, la operación no está indicada, salvo en los casos, por cierto pocos frecuentes, en los que aparecen signos de irritación cortical (crisis epilépticas focales) ya que en tales casos, pequeños fragmentos de lámina interna no son visibles en las radiografías, los cuales pueden lesionar la duramadre y la corteza cerebral.
El tratamiento quirúrgico se debe posponer cuando el estado del paciente es muy grave, ya sea por shock o por lesiones severas del encéfalo (estupor, coma, trastornos bulbares, hipotensión arterial). En tales casos deben tomarse todas las medidas necesarias para sacar el paciente de dicho estado y una vez obtenida una recuperación aceptable, proceder a la operación; a sí mismo, en casos de politraumatizados con lesiones en el resto del organismo, que necesiten un tratamiento quirúrgico inmediato, debemos posponer la operación del cráneo.
Si existen signos clínicos que sugieren la existencia de un hematoma, la operación debe practicarse inmediatamente sin tener en cuenta el estado del paciente y esta debe ser dirigida a la evacuación de dicha colección sanguínea que es la que pone en peligro la vida del paciente.
En el caso de las fracturas craneanas pediátricas, en los quistes leptomeníngeos postraumáticos el tratamiento es quirúrgico, y es obligatorio hacer un cierre de la duramadre. Puesto que el defecto dural tiene mayores dimensiones que el óseo, puede ser beneficioso realizar una craneotomía alrededor del lugar fracturado, reparar el defecto dural y reemplazar el hueso.
Es preciso controlar la evolución de las fracturas en pseudocrecimiento mediante radiografías y operarlas sólo si persiste la expansión después de varios meses o si aparece una lesión subgaleal.
En las fracturas en pelotas de ping-pong no es necesario instituir ningún tratamiento cuando estas se producen en la región temporoparietal, siempre que no haya una lesión cerebral subyacente, ya que la deformidad generalmente se corrige cuando crece el cráneo. Las lesiones situadas en la zona frontal pueden corregirse por razones estéticas, efectuando una pequeña incisión lineal detrás de la inserción del cabello, abriendo un agujero de trepanación adyacente al hundimiento y empujándolo hacia fuera con un disector de Penfield.
Técnica quirúrgica.
Los objetivos de la operación son:
1.ĀĀĀĀ levantar los fragmentos óseos.
2.ĀĀĀĀ evacuar los hematomas y tejidos necróticos intracraneanos.
3.ĀĀĀĀ Restituir la integridad anatómica del cráneo en todos sus planos.
Desde el punto de vista de la técnica operatoria la intervención se puede realizar utilizando 3 métodos:
En el primer método se practica una craneotomía osteoplastia. Este es el método elegido cuando se trata de un foco de hundimiento, sin líneas de fracturas radiadas, ya que esto permite circunscribirlo dentro de un colgajo osteoplástico.
Con este fin se practica una incisión de partes blandas epicraneanas en forma de herradura, como en las craneotomías osteoplásticas habituales, y se libera la superficie ósea en forma semicircular dejando un pie de músculo temporal. En dicha liberación se debe examinar cuidadosamente el hueso en busca de fracturas lineales que no hayan sido evidenciadas radiológicamente y una vez cerciorados de que no existe, podemos proceder a practicar la trepanación. Si es posible se deja el periostio intacto, sobre los fragmentos.
Debemos señalar que en esta craneotomía el pie del colgajo óseo debe ser lo más estrecho posible a fin de facilitar su levantamiento, ya que una maniobra brusca o forzada puede añadir una fractura del colgajo, en tanto que un levantamiento cuidadoso nos permite ir examinando la superficie cerebral subyacente y sus relaciones con los fragmentos.
Una vez levantado el colgajo, si la duramadre tiene un aspecto normal, late bien, el cirujano puede comenzar a trabajar sobre el colgajo osteomuscular al que están fijados los fragmentos. Cuando estos son pequeños se extraen; los grandes se colocan en su lugar a nivel del hueso y se fijan. No se pueden dar normas rígidas para esta reconstrucción, pues dependerá de la disposición de las fracturas, pero el hecho de estar ya separados del encéfalo, nos permite aplicar mayor fuerza y valernos de maniobras variables. Después, examinamos atentamente la superficie de la duramadre en cuanto a su aspecto, color y latidos, y si éstos son normales, la herida se cierra por planos.
Si la duramadre está tensa, no late, o tiene una coloración azulada, se debe sospechar un hematoma subdural y su abertura es obligatoria.
Cuando las fracturas cerradas se acompañan de heridas de la duramadre y del cerebro lo cual se constata en el momento del levantamiento del colgajo óseo, se extraen cuidadosamente los fragmentos incrustados en la masa encefálica, y se lava o se aspira el tejido necrótico existente. En tales casos, para explorar bien la superficie cortical subyacente, el defecto de la duramadre se amplía mediante incisiones en forma estrellada, se observa atentamente el área cerebral expuesta y se extraen delicadamente las esquirlas óseas, de modo de no causar más daño encefálico.
Lavamos con solución isotónica los detritos de tejido; si es necesario, provocamos una hipertensión intracraneana artificial por medio de compresión yugular bilateral, que facilita la salida de pequeños coágulos, esquirlas o tejido necrótico a la superficie.
Una vez realizada una buena limpieza de la herida, con una completa hemostasis, ésta se cierra por planos: duramadre, periostio y partes blandas.
Si existe edema cerebral que provoque prolapso de masa encefálica a través de la abertura de la duramadre, ésta no debe cerrarse a menos que disminuyamos la tensión por medio de una punción lumbar o con la administración de manitol, furosemida u otros deshidratantes cerebrales. Solamente en casos excepcionales, cuando existe un edema cerebral marcado, es preferible no reponer el hueso y, en tales casos, el colgajo se puede quitar definitivamente.
El método de reparar las fracturas deprimidas mediante una craneotomía osteoplástica es más cómodo, y al mismo tiempo permite una revisión amplia de las meninges y la superficie cerebral en un área más amplia que en el campo de los fragmentos. Este método es menos traumático para el tejido cerebral, pues la reconstrucción del hueso se realiza fuera de la superficie cerebral.
Es utilizable en pocos casos, sobre todo en niños, porque los huesos de ellos tienen una mayor elasticidad y las fracturas deprimidas pueden existir sin fracturas radiadas, que es una condición indispensable para el uso de éste método.
En el segundo método se levantan todos los fragmentos óseos; diariamente; éste se utiliza en fracturas deprimidas, con fisuras radiadas o fracturas múltiples de gran extensión, que no permiten realizar un colgajo osteomuscular. La incisión de partes blandas tiene forma de herradura o de “S” itálica. Se separa la piel, el tejido celular subcutáneo y la aponeurosis epicraneal, y el periostio se deja sobre la superficie del hueso. Pero, habitualmente, cuando se separa el colgajo de partes blandas y se dobla hacia fuera se encuentran los fragmentos con periostio lacerado y embebido en sangre.
Todos los fragmentos pequeños libres del periostio y del tejido cerebral necrótico se extraen. Los fragmentos mayores se quitan o se levantan con su periostio, para permitir el examen y el trabajo sobre la duramadre y el cerebro, tal como se describe en el método anterior; después se repone a su lugar.
Muchas veces, algunos fragmentos deprimidos están firmemente fijados, y el borde de su lámina interna queda por debajo de la bóveda, lo que no permite su movilización. En tales casos, se puede practicar un agujero de trepano en el hueso sano, inmediatamente por fuera de la fractura, y se amplía esta trepanación alrededor del fragmento, hasta ser posible su movilización cuando la duramadres esta lacerada y existe una herida del cerebro, todos los tejidos necróticos y coágulos se limpian, y la herida se lava son solución isotónica.
Después de la sutura de la duramadre lo fragmentos mayores se colocan en el defecto óseo de tal manera que sus bordes se fijen fuertemente en el defecto, y al final se suturan los tejidos blandos epicraneanos. Cuando existen fracturas múltiples y no es posible cerrar el defecto óseo con los fragmentos, los últimos se extraen por completo y los bordes del defecto se regularizan. En estos casos, si no se presenta hipertensión intracraneana, podemos realizar, inmediatamente, una plastia del defecto.
El tercer método se utiliza en las fracturas deprimidas de los lactantes. La mayor elasticidad de la bóveda craneal de los lactantes no permite formar líneas de fracturas y fragmentos. Habitualmente se observa un hundimiento uniforme y con una base redonda (como en pelota de ping-pong). Estos fragmentos también se levantan por medio de un agujero de trépano inmediatamente por fuera del borde de la depresión, a través de lo cual se introduce, cuidadosamente, un disector fino en el espacio epidural, y haciendo un suave movimiento de palanca se obtiene la restitución a su lugar del hueso deprimido. Cuando esta técnica se emplea en las primeras horas después del traumatismo, el levantamiento del hueso se logra fácilmente. Algunos días más tarde, mediante este método, el levantamiento es más difícil.
Cuando se sospecha una lesión del nervio óptico por una fragmento en el canal óseo, sobre todo en los casos con acentuada disminución de la visión en los que radiológicamente se ven líneas de fractura en esta región, se recomienda una exploración quirúrgica con resección de la pared superior del conducto óptico. Se practica una craneotomía osteoplástica frontal o frontotemporal y la duramadre se separa del techo orbitario. Mediante un agujero del trepano en el techo orbitario, por delante del ala menor utilizando una gubia fina, se reseca la pared superior del conducto óptico y se extraen todos los fragmentos en caso de imposibilidad de liberar el nervio óptico se puede abrir la duramadre y resecar el bordo interno del conducto óptico bajo control visual del nervio.
Operaciones en los hematomas intracraneanos.
En los traumatismos encefalocraneanos se pueden observar hematomas epidurales, subdurales, e intracerebrales, que provocan una comprensión cerebral y exigen un tratamiento quirúrgico. La operación se debe realizar lo más precozmente posible.
El diagnóstico mismo de un hematoma intracraneal es una indicación quirúrgica. Cuando el estado del paciente es grave y no permite hacer un examen radiológico complementario, la sospecha de un hematoma intracraneal es ya una indicación para una trepanación exploratoria. El higroma subdural que provoca un cuadro de comprensión cerebral es también indicación de intervención urgente. En ocasiones, una hemorragia subaracnoidea grave puede ser también objeto de una operación de urgencia.
En el tratamiento de la contusión hemorrágica, cabe realizar una descompresión quirúrgica si existe riesgo de hernia cerebral.
En los casos de hematoma epidural la tomografía axial computerizada (TAC) de cráneo es de utilidad para detectar incluso los hematomas epidurales pequeños y sirve, para realizar el tratamiento evolutivo, pero en la mayoría de los casos es necesario evacuarlo quirúrgicamente y las indicaciones son: todo hematoma epidural sintomático, hematoma epidurales asintomático de grosor más de 1 cm la reabsorción de estos hematomas es poco probable. Los hematomas epidurales que se forman en niños son más peligrosos que los adultos pues los niños tienen menos lugar para alojar el coágulo.
Los objetivos del tratamiento quirúrgico son: evacuar el coágulo, reducir la presión intracraneal (PIC), eliminar el efecto de masa focal, lograr la hemostasia, es preciso coagular las partes blandas hemorrágicas, venas y arterias durales, sobre todo la arteria meníngea media. Se aplica cera ósea sobre los vasos sangrantes intradiploicos, generalmente venas, para evitar la recidiva del hematoma colocar puntos de tracción en la duramadre.
En el caso de los hematomas subdurales agudos se debe llevar a cabo una evacuación quirúrgica rápida en los pacientes sintomáticos con un grosor de hematoma superior a 1 cm o mayor de 5 mm en los niños. Algunos refieren que los hematomas más pequeños no necesitan ser evacuados y, además, una intervención quirúrgica puede aumentar la lesión cerebral si hay edema cerebral y hernia del cerebro a través de la craneotomía. Por lo general se precisa una craneotomía para poder evacuar el coágulo denso y acceder a los lugares posibles de la hemorragia, no siempre es fácil de identificar durante la intervención. Se puede comenzar con una pequeña abertura lineal de la duramadre y agrandarla cuando sea necesario y solo si la tumefacción del cerebro parece controlable.
En los casos de hematomas subdurales agudo infantil el estado clínico y el tamaño del hematoma determinan el tratamiento adecuado. Los casos que presentan síntomas mínimos como vómitos, irritabilidad, ausencia de alteraciones del conocimiento y trastornos motores y un hematoma licuado pueden tratarse con punción subdural percutánea, tratamiento que es posible repetir cuantas veces sea necesario. Los casos crónicos pueden llegar a necesitar un sistema de derivación subduroperitoneal.
Los casos que presentan síntomas más graves y un coágulo hiperdenso en la tomografía axial computerizada (TAC) deben tratarse mediante craneotomía. No es infrecuente hallar una membrana subdural similar a la que cubre a los hematomas subdurales crónicos de los adultos. Como precaución estos pacientes corren el riesgo de sufrir un shock hipovolémico intraoperatorio.
El hematoma subdural crónico en su tratamiento hay que tener en cuenta la prevención de las convulsiones: su uso no está totalmente aceptado. Se administra una dosis de carga de fenitoína, 17 miligramos por kilogramo mediante vía intravenosa (iv) lenta y luego 100 miligramos en infusión lenta cada 8 horas. Cabe suspender la fenitoína si después de una semana aproximadamente no aparecen convulsiones. En los casos que presentan convulsiones tardías, se hayan administrado tratamientos anteriores o no, es necesario instituir un tratamiento prolongado. Algunos consideran que la incidencia de los efectos colaterales de uso de fármacos antiepiléptico es similar a la de las convulsiones, por lo que no recomiendan realizar este tratamiento preventivo. Es necesario revertir las Coagulopatías y la anticoagulación yatrogénica. Se indica evacuación quirúrgica del hematoma si las lesiones son sintomáticas, déficit focal, cambios del estado mental o si el espesor máximo del hematoma subdural supera 1 cm.
Hematoma epidural.
El hematoma epidural se debe generalmente a rupturas de la arteria meníngea media o una de sus ramas, por fracturas lineales que cruzan su trayecto. Está situado frecuentemente en la región temporal o temporoparietal, donde se debe realizar la trepanación.
La intervención comprende una craniectomía sobre el área del hematoma. Esta se inicia con un agujero de trépano, y una vez encontrado el hematoma enseguida comienza a salir sangre líquida o en coágulos y la craniectomía se amplía hasta 5 o 7 centímetros de diámetro, la que permite evacuar completamente el hematoma mediante aspiración, cureta u otro instrumento. Es muy importante, una vez evacuado el hematoma observar cuidadosamente la superficie dural, para no dejar ningún vaso sangrante. En muchos casos no se puede encontrar el vaso que ha sangrado. Otras veces podemos encontrar roto el tronco de la arteria meníngea media o una de sus ramas. La hemostasis se realiza por medio de electrocoagulación, clips o ligadura. Esta última se realiza con hilo fino y aguja atraumática, que se pasa por debajo del vaso sangrante entre las dos capas de la duramadre cuando hay ruptura del tronco de la arteria meníngea media, la trepanación se amplía hacia l base craneal, hasta descubrir el vaso sangrante. Si la arteria está rota cuando emerge o cerca del agujero redondo menor se hace la hemostasis con más facilidad mediante un taponamiento con algodón prensado y cera hemostática. Antes de cerrar la herida quirúrgica se pueden poner puntos de fijación de la duramadre al periostio, a fin de prevenir un nuevo sangramiento. Si hay duda en la hemostasis completa, se debe dejar un drenaje en la parte inferior de la herida durante 24 horas.
Si no tuviésemos datos precisos de la localización, y no se pudieran realizar exámenes radiológicos por falta de medios o por estado grave del paciente, el hematoma se puede buscar con trépanos exploratorios en las siguientes regiones:
- En la región temporal a 3 centímetros por delante y por encima del conducto auditivo externo.
- En la región frontal a 3 centímetros por fuera de la línea media e inmediatamente por delante de la sutura coronaria. Esta sutura coincide con la línea que reúne los dos puntos medios de los arcos cigomáticos y está perpendicularmente situada a ellos.
- En la región parietal posterior a 3 centímetros por encima y por detrás del polo superior del pabellón de la oreja. Cuando se sospecha un hematoma epidural en la fosa craneal posterior se realiza un agujero de trepano a 3 centímetros por fuera y por debajo de la protuberancia occipital externa.
Cuando se encuentra el hematoma, el agujero de trepano se amplía suficientemente para permitir su evacuación.
Cuando existen datos precisos de la evacuación del hematoma., y el estado del paciente lo permite, se puede practicar una craneotomía osteoplástica que permita visualizar la mayor parte de la superficie externa del hematoma. Mediante esta craneotomía la extirpación del hematoma se realiza más fácil y, al mismo tiempo, no deja defecto de la bóveda craneana.
Hematoma subdural.
Los hematomas subdurales son provocados habitualmente por la ruptura de las venas de la superficie convexa del cerebro, en el lugar por donde atraviesa el espacio subdural para desembocar en los senos de la duramadre. Los hematomas subdurales están situados sobre una superficie ancha de la cara convexa del hemisferio cerebral, normalmente en la región parietooccipital, con menos frecuencia se encuentra en la región frontal occipital o basal. Aproximadamente el 10% son bilaterales.
La evacuación de un hematoma subdural se puede realizar por medio de uno o dos trépanos, para lavar la cavidad con solución isotónica a través de ellos, o por una craneotomía osteoplástica permita además de evacuarlos, extirpar su cápsula.
En casos de hematomas subdural agudo o en casos crónicos en grave estado, se aconseja evacuarlo con el menor trauma quirúrgico, es decir, con uno o dos trépanos; en casos crónicos en buen estado, recomendamos una evacuación con extirpación de la capsula por medio de una craneotomía osteoplástica.
La evacuación mediante uno o dos trépanos se realiza mediante la siguiente manera: según los datos clínicos y exámenes imagenológicos (preferiblemente tomografía axial computerizada (TAC) de cráneo) se practica un agujero de trepano sobre el supuesto centro del aérea del hematoma, generalmente en la región temporoparietal. Si no existen datos clónicos precisos de la localización, y no se puede realizar exámenes imagenológicos por falta de condiciones o por el estado grave del paciente, el hematoma se puede buscar con trépanos en las regiones temporal, parietotemporal y frontal. El agujero de trepano se activa hasta un diámetro de 3 cm. la duramadre se encuentra tensa y de color azulado homogéneo; se abre en cruz y si el hematoma es reciente sale inmediatamente sangre de color oscuro, con pequeños coágulos. En los hematomas crónicos debajo de la duramadre encontramos su capsula, que tiene un color verde parduzco, y al ser abierta deja salir una sangre muy oscura también verdosa.
Una vez evacuado todo el contenido del hematoma, se lava cavidad con abundante solución isotónica hasta que esta salga clara; si se han hecho dos trépanos se hace la inyección de solución a través de uno de ellos y sale por el otro. A este fin es conveniente hacer el lavado a través de un catéter flexible que se pueda colocar en todas las direcciones.
En los hematomas subdurales es habitual no encontrar el vaso sangrante, pues, la compresión que el mismo hematoma produce, provoca su ocluŁsión trombótica; en algunos casos con hematoŁmas agudos podemos hallar una vena sangrante, y las más frecuentes son las grandes venas cortiŁcales que afluyen al seno longitudinal supeŁrior. En tales casos, la hemostasis se logra por medio de electrocoagulación o taponamiento. Después de evacuada y lavada la cavidad del hematoma con solución isotónica, la herida opeŁratoria se cierra sin suturar la duramadre. CuanŁdo no estamos seguros de haber realizado una completa hemostasis, debemos dejar un drenaje por 24 horas. Cuando la evacuación del hematoma se hace por una craneotomía osteoplástica, debemos procurar que ella abarque la mayor área posible del hematoma. Esta evacuación se hace por inciŁsión de la cápsula, que se abre ampliamente y después se reseca en fragmentos, pues ésta no está adherida ni a la aracnoides ni a la duramaŁdre.
Como los hematomas ocupan una extensa área sobre la convexidad de los hemisferios, a veces no es posible resecar toda su cápsula. La capa profunda de la cápsula se puede despegar de la aracnoides mediante un lavado a presión con solución isotónica a través de un catéter blando por debajo de ella.
Una vez evacuado el hematoma, si persisten signos de hipertensión intracraneana, es decir, la superficie del cerebro queda hipertensa con una tendencia a protruir a través de la trepanaŁción, debemos pensar en un posible hematoma contralateral, lo que constituye una indicación de exploración del otro lado.
La evacuación de los hematomas subdurales en los lactantes tiene algunas particularidades. En ellos, la presencia de la fontanela anterior permite explorar el espacio subdural por punción con una aguja introducida por un ángulo exterŁno, y dirigida hacia afuera, en dirección tangenŁcial a la bóveda; si caemos en el hematoma, evaŁcuamos la mayor cantidad posible de sangre.
Las punciones se repiten cada 2 ó 3 días, hasta tanto éstas sean blancas. La etapa siguiente del tratamiento es un agujero de trépano para investigar si existe una cápsula; si ésta existe y es densa, o hay contenido líquido no evacuado por las punciones, está indicada una craneotoŁmía osteoplástica amplia, que en los lactantes se realiza con tijeras, y se extrae entonces la cápsula. En casos de hematomas bilaterales, esta operación se repite del otro lado 8 o 10 días más tarde.
Consideraciones sobre el tratamiento quirúrgico del hematoma subdural crónico.
Opciones de tratamiento quirúrgico.
No hay acuerdo acerca de cuál es el mejor método para tratar los hematomas subdurales crónicos.
- Dos agujeros de trepanación, que se irrigan con solución salina tibia hasta que el líquido sale claro.
- Irrigación y aspiración mediante un gran agujero de trepanación o agujero de trefina.
- Drenaje subdural colocado mediante un agujero de trepanación y mantenido durante 24 o 48 horas, se retira cuando la cantidad de líquido pasa a ser insignificante.
- Craneostomía con mecha y taladro manual (twist drill), cabe destacar que el drenaje pequeño a través de un orificio de mecha con taladro sin colocar un drenaje subdural tiene un alto índice de recidiva del hematoma.
- Craneotomía formal con escisión de la membrana subdural, puede ser necesaria en los casos que recidiva después de realizar algunos de los procedimientos descritos, posiblemente debido a una filtración de sangre desde la membrana subdural. Es una técnica válida y segura. Muchos recomiendan que no se debe intentar extirpar la membrana profunda que está adherida a la superficie del cerebro.
Las técnicas que fomentan el drenaje continuo después de un procedimiento de evacuación con el objetivo de reducir la cantidad de liquido residual y evitar la recidiva son: el empleo de un drenaje subdural, la apertura de un agujero de trepanación amplia por debajo del músculo temporal, el mantenimiento del paciente en reposo absoluto con la cabecera horizontal, puede usar una almohada y la sobrehidratación leve durante 24 o 48 horas después de la intervención o, si se utiliza un drenaje, hasta 24 o 48 horas después de retirarlo. Estas medidas fomentan la expansión del cerebro y la expulsión del líquido subdural remanente. Cuando el cerebro no se expande, algunos preconizan el empleo de una infusión continua en el espacio subaracnoideo lumbar, pero este método no carece de complicaciones.
Craneostomía con mecha y taladro manual (TWIST DRILL) como tratamiento de los hematomas subdurales crónicos.
Se supone que este método provoca una descompresión lenta del cerebro e impide que se produzcan los cambios abruptos de presión que suelen seguir a otros métodos y que pueden estar asociados a complicaciones tales como hemorragia intraparenquimatosa o intracerebral. Incluso algunos los realizan en la habitación con anestesia local.
La técnica consiste en insertar un catéter ventricular dentro del espacio subdural para drenar el contenido del hematoma hacia una bolsa convencional de ventriculostomía colocada 20 cm debajo del nivel de la craneostomía, se mantiene el paciente en posición horizontal sobre la cama y se evalúa si el drenaje es suficiente mediante tomografía axial computerizada (TAC) de cráneo seriadas. Una vez que se ha extraído al menos el 20% de la acumulación y el paciente muestra signos de mejoría, de 1 a 7 días después de iniciado el tratamiento, con una media de 2,5 días, se retira el drenaje.
Agujeros de trepanación como tratamiento de los hematomas subdurales crónicos.
A fin de prevenir las recidivas, se recomienda no utilizar agujero de trepanación pequeño, sin drenaje subdural. Es preferible realizar una craneotomía subtemporal amplia, 2.5 centímetros de diámetro reales, que deben medirse con exactitud y emplear coagulación bipolar para que los bordes de la duramadre y de l membrana subdural coincidan con el ancho de la apertura ósea, no hay que tratar de separar esas dos capas por que se puede provocar una hemorragia. Este procedimiento permite el drenaje continuo del líquido subdural hacia el músculo temporal. Es de utilidad colocar una lámina de algún material hemostático como el Gelfoam, sobre el orificio para evitar que entre sangre nueva orinada en las partes blandas del abordaje.
Drenaje subdural.
Si se emplea un drenaje subdural es conveniente que sea un sistema cerrado. Los catéteres de ventriculostomía no son adecuados por que tienen agujeros pequeños que están ubicados en el extremo del catéter diseño que responde a la necesidad de evitar que el plexo coroideo tape el catéter al insertarlo en el ventrículo cuando se lo integra a un sistema de derivación del líquido cefalorraquídeo (LCR), sobre todo cuando el liquido acumulado es denso y oleoso en el lado positivo, puede ser útil cuando el objetivo es hacer un drenaje lento. La bolsa colectora se coloca 50 a 80 centímetros debajo a la altura de la cabeza.
Después de la intervención, el paciente debe permanecer en posición horizontal. Cabe administrar profilaxis antibiótica hasta 24 o 48 horas después de retirar el drenaje y, en ese momento se comienza a elevar poco a poco la cabecera de la cama. Puede ser de utilidad obtener una tomografía axial computerizada (TAC) antes de retirar el drenaje o poco después para establecer un punto de referencia en caso de que el paciente se deteriore.
Si bien estos hematomas parecen inocuos pueden generar complicaciones graves luego del tratamiento quirúrgico tales como la convulsiones incluso de mal epiléptico intratable, hemorragia intracerebral que suele verse del 0.7 al 5% de los casos. Estas hemorragias son devastadoras en estos cuadros, el 33% de los pacientes fallecen y otro 33% queda con incapacidades graves, puede también ocurrir una imposibilidad del cerebro para reexpandirse u ocasionar una recidiva, puede ocurrir un neumoencéfalo tensional o un empiema subdural que también puede formarse en hematomas no tratados.
En el 60% de los pacientes mayores de 75 años y en ninguno de los menores de los 75 años, una descompresión rápida está asociada a hiperemia de la corteza subyacente que puede estar relacionada con la aparición de una hemorragia intracerebral o de convulsiones. Todas las complicaciones son más frecuentes en los ancianos y en los pacientes debilitados.
La mortalidad general tras el tratamiento quirúrgico es de 0% hasta el 8%. En una serie de 104 pacientes tratados en su mayoría mediante craneostomía, la mortalidad fue de un 4%, y todos los decesos fueron mayores de 60 años y se debieron a afecciones concurrentes. Otra publicación sobre una serie de gran magnitud informa de una mortalidad de 0,5%. El estado neurológico empeora tras el drenaje en el 4% de los casos.
Higroma subdural.
En el higroma subdural se acumula líquido cefalorraquídeo en el espacio subdural por un mecanismo de válvula, que comprime el encéfalo. El higroma acompaña habitualmente las contusiones cerebrales donde la aracnoides está rota, y por esto el líquido cefalorraquídeo del higroma es sanguinolento. Éste puede estar situado sobre toda la superficie del cerebro o en uno de sus hemisferios.
En el higroma subdural traumático no es necesario tratar los asintomáticos.
El tratamiento quirúrgico consiste en un trépano en la región temporoparietal o bilateralmente. Cuando se abre la duramadre sale a presión, líquido cefalorraquídeo, y después se aprecia la corteza cerebral despegada de la duramadre. La herida quirúrgica se cierra sin suturar la duramadre para crear una vía de dreŁnaje hacia las partes blandas epicraneanas. Si durante el período postoperatorio la hipertenŁsión intracraneana persiste, se debe hacer una punción del espacio subdural a través de la herida quirúrgica.
Puesto que son frecuentes las recidivas después de efectuar una evacuación simple por agujeros de trepanación, es aconsejable, en caso de intervenir, dejar un drenaje subdural durante 24 o 48 horas. En casos graves se puede dejar un drenaje durante unos días.
Puede llegar a ser necesario efectuar una craneotomía en los casos de recidivas reiteradas para localizar el lugar de la pérdida del líquido cefalorraquídeo (LCR), que generalmente, es difícil de reconocer, o bien si es posible recomendamos colocar un sistema de derivación subduroperitoneal.
Hematoma intracerebral.
En los traumatismos encefalocraneanos cerraŁdos encontramos los hematomas intracerebrales generalmente cerca de un foco de contusión. La intervención quirúrgica se realiza, por lo común, después de la comprobación del diagnóstico por exámenes complementarios (tomografía axial computerizada (TAC), resonancia magnética nuclear (RMN); angiografía), que ofrecen datos de un proceso expansivo.
Se practica un agujero de trépano sobre el foco del hematoma y se amplía hasta 3 cm de diámetro; cuando se abre la duramadre se encuentran cambios de la corteza cerebral, que aparece con una coloración amarillenta oscura, y con aumento de la presión intracraneana. Por la palpación se puede apreŁciar fluctuación; otras veces es posible constaŁtar un foco de contusión.
En la corteza sospeŁchosa se hace una punción con trocar cerebral, y si caemos en el hematoma, aspiramos la mayor cantidad posible.
Cuando el hematoma está situado en la profundidad y se aspira una canŁtidad suficiente, debemos terminar aquí la opeŁración; si el hematoma es superficial, se hace una incisión de la corteza y se penetra en la cavidad, ya que esto facilita una evacuación más completa y eventualmente el hallazgo del vaso sangrante. En los casos en que encontremos, conjuntamente, un foco de contusión debemos proceder a la limpieza del tejido necrótico.
Hemorragia subaracnoidea.
La hemorragia subaracnoidea de origen trauŁmático se debe, generalmente, a una contusión cerebral y en ella la intervención quirúrgica no está indicada.
En las hemorragias subaracnoideas graves con obstrucción de las cisternas basales, Ody ha propuesto una operación por la cual se abre la fosa craneal posterior y se drena la cisŁterna magna.
La operación se realiza de la siguiente manera: se practica una incisión vertical de partes blanŁdas, en la región de la nuca, en la línea media, desde la protuberancia occipital externa hasta la apófisis espinosa de la tercera vértebra cerŁvical; se separan los músculos de la región estricŁtamente en la línea media. En la profundidad se liberan el arco posterior del atlas y la concha occipital, alrededor del agujero occipital. Estos últimos se resecan, mediante gubia, hasta 1,5 cm por fuera de la línea media. La duramadre y la aracnoides se abren con una incisión vertical, de la cisterna magna y brotará cierta cantidad de sangre mezclada con líquido cefalorraquídeo. La herida se cierra y se deja un drenaje durante unos días.
Hematoma subdural espontáneo.
En el caso de un hematoma subdural espontáneo el tratamiento de elección es la evacuación quirúrgica y, en el caso que el hematoma sea subagudo o crónico, por lo general es suficiente efectuar una evacuación por trepanación.
La acumulación extraxial de líquido en pediatría.
La acumulación extraxial de líquido en pediatría tiene opciones de tratamiento:
Lo primero es la observación y seguimiento mediante mediciones seriadas del perímetro craneal, ecografía y la tomografía axial computerizada (TAC) de cráneo.
Punciones subdurales seriadas: en algunos pacientes, fueron necesarias hasta 16 punciones. Algunas publicaciones dan cuenta de buenos resultados, mientras que otras muestran un bajo índice de resultados satisfactorios.
El drenaje por trepanación acompañado o no de drenaje externo prolongado. El drenaje simple por trepanación puede no ser eficaz en los casos de desproporción craneoencefálica pronunciada porque el cerebro tarda en expandirse y en ocupar el espacio extraxial.
La derivación subduroperitoneal: por lo general, basta con una derivación unilateral, incluso en los casos de efusiones bilaterales, no es necesario realizar ningún estudio para verificar que existe o que haya comunicación entre los dos lados. Es preciso utilizar un sistema de muy baja presión.
Generalmente se retira la derivación después de 2 a 3 meses de drenaje, una vez que desaparecen las acumulaciones, a fin de reducir la posibilidad de mineralización o calcificación de la duramadre y de la aracnoides y el riesgo de convulsiones. Es fácil retirar estos sistemas después de 2 o 3 meses, pero puede resultar más dificultoso hacerlo más tarde.
Otras recomendaciones son, que es preciso realizar al menos una punción percutánea transfontanelar de la acumulación de líquido para descartar la presencia de infecciones, muchos autores recomiendan observar a los lactantes asintomáticos o que sólo presentan macrocrania y retraso en el crecimiento. (20, 38,96)
Operaciones en el traumatismo encefalocraneano abierto.
El objetivo del tratamiento quirúrgico del traumatismo encefalocraneal (TEC) abierto es limpiar el foco de contusión cerebral, del tejido necrótico, las esquirlas óseas, los cuerpos extraños, los coágulos; levantar los fragmentos óseos que estén deprimidos y reconstruir íntegramente la duramadre la pared ósea si es posible, y los tejidos blandos epicraneanos.
Indicaciones y contraindicaciones.
En todos los casos con traumatismo encefalocraneal (TEC) abierto, debe hacerse limpieza quirúrgica en las primeras horas siguientes al trauma.
Esta limpieza puede ser propuesta para horas o días más tarde, en presencia de un estado general muy grave, coma profundo, trastornos cardiovasculares y respiratorios, además de un estado de shock.
En tales casos se toman primeramente todas las medidas necesarias para que el paciente mejore su estado hasta un grado que sea posible practicar la limpieza quirúrgica, esta se puede también posponer en los casos de politraumatizados, en beneficio del tratamiento quirúrgico de urgencia e otros órganos cuyas lecciones graviten en el pronóstico del enfermo.
Técnica quirúrgica.
La técnica quirúrgica depende de la profundidad y la característica de la lesión es decir, si se trata solamente de la herida de la parte blandas epicraneanas o si la herida comprende el hueso, la duramadre (heridas penetrantes o no penetrantes), el cerebro, o si se trata de una herida por contusión por sección o por punción. Las técnicas quirúrgicas de las heridas por arma de fuego se describen a parte.
Limpieza quirúrgica de las heridas de los tejidos blandos epicraneanos.
Ella se practica según las reglas generales de la cirugía. Los bordes de la herida se resecan unos dos o tres milímetros sobre los tejidos sanos y se quitan todos los tejidos necróticos y cuerpos extraños. La hemostasis se logra cómodamente con electrocoagulación, y se debe evitar emplearla en la piel. Las suturas se hacen en un solo plano. En casos con grandes laceradas y defectos de la piel es necesario practicar incisiones adicionales que formen colgajos para cubrir los defectos y hacer una reconstrucción plástica de los tejidos blandos epicraneanos. Cuando la herida está contaminada por tierra u otro material extraño se emplean antibióticos localmente y se deja drenaje.
Limpieza quirúrgica del traumatismo encefalocraneano abierto por lesión del cráneo y cerebro.
Después de la resección de los tejidos blandos epicraneanos es necesario ampliar la herida de las partes blandas con incisiones adicionales, para abordar todos los fragmentos.
La rica vascularización de las partes blandas epicraneanos permite una gran variedad de las incisiones.
La necrosis de los bordes de la herida se observan solamente cuando cometemos errores técnicos evidentes, como por ejemplo.
La sección de grandes vasos, un colgajo con una base muy estrecha, o gran tensión de los puntos.
Cuando el área de la herida ósea no es muy extensa se pueden hacer dos incisiones adicionales a ambos extremos de la herida en una línea recta: y si la herida es extensa, dos extensiones en forma de arco trazadas de tal manera que toda la herida obtiene forma de “S”.
La forma de la incisión depende de la localización de la herida. En la región frontal las incisiones adicionales se planean de tal forma que permitan una buena exploración sin provocar cicatriz innecesaria en la frente.
Cuando la herida tiene una forma irregular, y en heridas múltiples, se hacen incisiones más complicadas, que se adaptan a la dirección de la herida y a veces las incisiones unen una o varias heridas.
Se extraen todos los fragmentos libres y se conservan aquellos que tienen periostio y se doblan a modo de colgajo. Esta maniobra se facilita mediante un agujero de trépano en el borde de los fragmentos en las fracturas conminuta y en un área extensa, no es necesario extraer todos los fragmentos, sino solamente lo que están dentro de la cavidad craneal, y por debajo de los cuales la duramadre esta lesionada.
En la mitad de los casos la duramadre está intacta y si el color y la tensión son normales no se abre. Si la duramadre esta lacerada, habitualmente se observan coágulos y sangre líquida que deben evacuarse. La abertura de la duramadre se amplía y se efectúa la limpieza de la herida cerebral, que comienza desde la superficie y poco a poco sigue hacia la profundidad.
Habitualmente la extensión de la lesión cerebral no sobrepasa el área ocupada por los fragmentos. El tejido cerebral necrótico y todos los coágulos se extraen fácilmente mediante un lavado a presión con solución isotónica o por aspiración. Los fragmentos y los cuerpos extraños visibles incrustados en el tejido cerebral e extrae mediante un instrumento quirúrgico.
Se debe considerar que la limpieza ha terminado cuando se alcanza el fondo de la herida. En casos de heridas cerebrales profundas sus bordes se pueden separar con espátulas cerebrales y protegerlas previamente con algodones embebidos en solución isotónica. No es aconsejable pracŁticar incisiones adicionales del tejido cerebral sano para penetrar en la profundidad. Es mejor dejar algunos cuerpos extraños en la profundidad del cerebro sin necesidad de provocar nuevas destrucciones cerebrales mediante incisiones adiŁcionales, sobre todo, en las áreas de la corteza cerebral con importancia funcional.
Después de una hemostasis completa, la duraŁmadre se sutura, si es posible. Si quedase algún defecto podemos utilizar una película de fibrina y otro material plástico. Esto no se debe hacer en heridas sucias, en las que entonces se deja abierta la duramadre. Los fragmentos óseos con periostio conservado y que habíamos doblado a modo de colgajo se reponen en su lugar. Los fragmentos libres más grandes se colocan tamŁbién en su lugar, y se trata de que queden fijos por el afrontamiento de sus bordes y evitar así el uso de hilo u otro material extraño para su fijación.
En fracturas con múltiples fragmentos en que no se puede reconstruir la bóveda craneana, desŁpués de extraer todos los fragmentos, se deben regularizar los bordes del defecto óseo y no es aconsejable usar material plástico, sobre todo en heridas sucias o cuando el paciente llega tardíamente a manos del cirujano.
Hemostasis en la ruptura de los senos de la duramadre.
La hemostasis en la ruptura de los senos de la duramadre no es una operación independiente. Ella es necesaria, a veces, en el tratamiento quiŁrúrgico, en cualquier lesión craneoencefálica cerrada o abierta, pero tiene una técnica quirúrŁgica específica y por eso exige una descripción aparte.
La hemorragia de los senos de la duramadre se produce por trauma directo de sus paredes en las heridas penetrantes craneocerebrales y, en ocasiones, en las fracturas deprimidas cerradas.
Con más frecuencia se lesiona el seno longituŁdinal superior por su accesibilidad mayor, y es más rara la lesión de los senos laterales y el seno occipital; la ruptura de la prensa de Herófilo se considera extremadamente grave.
En la mayoría de los casos, la ruptura es provocada por los fragmentos óseos y no por el agente traumático; aquéllos generalmente atraviesan la pared y se incrustan en el seno, obliterando el orificio de la ruptura, por lo que es común no encontrar un sangramiento profuso en la herida. La hemorragia se produce, habitualmente, en el momento de la limpieza quirúrgica, cuando extraemos los fragmentos incrustados en la pared.
Cuando existe un sangramiento abundante por la herida, que puede atribuirse a ruptura de los senos, debe hacerse la hemostasis inmeŁdiatamente; ésta puede hacerse provisionalmente por taponamiento, si el paciente presenta trasŁtornos bulbares o estado de shock periférico, y se pospone la hemostasis quirúrgica hasta que la recuperación del estado del paciente la perŁmita.
Habitualmente se aplica anestesia general, excepto en casos de muy buen estado general y con lesiones poco extensas del cráneo y del cereŁbro, en los que podemos emplear anestesia local.
La posición del traumatizado en la mesa opeŁratoria depende de la localización de la herida; se colocarán en decúbito supino los pacientes con lesiones de- los dos tercios anteriores del seno longitudinal, y en posición lateral o en decúbito prono los que presentan lesión del tercio posterior de éste, o de los senos laterales. La cabeza debe estar colocada por encima del plano del tronco (Ligera posición de Fowler) para disŁminuir la presión venosa intracraneal.
Sin embarŁgo, debemos cuidar que esta posición no se exaŁgere, ya que puede provocar una presión venosa negativa y aspiración de aire por la ruptura, con la consiguiente embolia gaseosa.
Durante la exploración quirúrgica de una fractura en la línea media o en otra región del cráneo sobre la proyección de los senos de la duramaŁdre, la extracción de los fragmentos tiene que comenzar desde la periferia hacia el lugar donde se sospecha la ruptura. En tales casos, el defecto de la bóveda craneal tiene que ser mayor para permitir un trabajo cómodo sobre el seno. CuanŁdo se descubre el lugar de la ruptura y comienza a salir sangre venosa en gran cantidad, el ciruŁjano debe poner su dedo sobre el orificio para contener el sangramiento provisionalmente, mienŁtras, se aspira la sangre y se precisa la localizaŁción exacta y amplitud de ésta.
Manteniendo siempre la compresión digital, se amplía con gubia alrededor el defecto óseo, en un diámetro de unos 5 o 6 cm aproximadamente. Esta maniobra nos permite proseguir el trabajo sobre el seno y obtener una hemostasis definitiva. ¿De qué manera realizaremos dicha hemostasis? Ella depende del lugar y del tamaño de la lesión. En presencia de rupturas lineales del seno, con borŁdes regulares, la técnica más adecuada es la sutuŁra directa, con aguja atraumática e hilo fino, tales como las que se emplean en cirugía vascular.
En las lesiones pequeñas y sobre todo en las que la parte lesionada es la pared superior, es conveniente hacer plastia con un fragmento de músculo. Si la herida de partes blandas es extensa y alcanza la región temporal, fácilmente se puede tomar un fragmento de músculo con su fascia (2 X 2 cm), el cual se pone debajo del dedo que tapona la hemorragia, se oblitera el orificio y se sutura con algunos puntos a cada lado, por fuera del seno, sobre duramadre sana. Un defecto de la pared lateral del seno se puede cerrar también con un pedazo del músculo. Con este fin, después de la abertura de la duramadre, lateralmente al seno, el orifiŁcio se tapona con un pedazo de músculo que se fija mediante uno o dos puntos de suturas.
En lesiones graves se puede intentar una plastia con duramadre del la vecinŁdad, y utilizar pequeños colgajos. Con este fin la duramadre se abre mediante una incisión recta paralela al seno y a distancia suficiente para formar un colgajo que pueda cubrir bien la ruptura. Este colgajo se forma de uno u otro lado tratando de evitar la lesión de las venas corticales que antes de su desembocadura en el seno pasan a corta distancia entre las dos capas de la duramadre.
En las laceraciones graves del seno, cuando sufre no solamente la pared superficial, sino también la pared lateral, y la lesión está en sus tercios anteriores, se puede intentar un taponamiento con gasas. Estas se colocan entre la cara interna de la bóveda y la duramadre despegada de la parte anterior y posterior de la craniectomía. Este método no debe emplearse como hemostasis definitiva más que excepcioŁnalmente, sino como una maniobra provisional que permita hacer una plastia con más comoŁdidad.
La ligadura de los senos se utiliza en laceraŁciones graves cuando la sutura o la plastia no son posibles. La técnica de la ligadura es la siguiente: se hace una incisión en la duramadre a cada lado de la lesión del seno y paralela a éste. Después se separan los bordes superiores de ambos hemisferios cerebrales, con espátulas, proŁtegidas por algodón, y se hace una transfixión en la hoz, inmediatamente por debajo del seno. De este modo se hacen ligaduras por delante y por detrás de la ruptura.
Todas las venas corticales que desembocan en el seno entre las dos ligaduras deben ser coaguŁladas. Es necesario señalar que la ligadura de los senos de la duramadre es una conducta heroica, que solamente es soportada en la mitad anterior del seno longitudinal superior; la ligaŁdura de la mitad posterior de éste y de los senos laterales provoca trastornos graves del drenaje venoso. No está permitida la ligadura a nivel de la prensa (torcular) de Herófilo, pues tiene conŁsecuencias fatales. (20, 38,96)