El síndrome de Brugada es responsable del 4% de los casos de muerte súbita, fenómeno frecuente en la práctica clínica. Descrito alrededor de 17 años atrás por los hermanos Joseph, Ramón y Pedro Brugada, está genéticamente determinado por más de 100 mutaciones de un gen en el cromosoma 3, mostrando una herencia autosómica dominante. Se diagnostica fácilmente por electrocardiografía ante la presencia del patrón típico de bloqueo de rama derecha hisiana asociado a la elevación del punto J y del segmento ST en derivaciones precordiales derechas (V1, V2 y V3), de forma espontánea o tras la administración de antiarrítmicos que bloqueen la actividad del canal de sodio y por ende eleven el segmento ST, entre ellos la flecainida, procainamida y ajmalina, este último el más usado en Cuba. Puede ser detectado en fase asintomática por medio de un chequeo de rutina o en el curso de arritmias ventriculares malignas que causan estados sincopales o incluso muerte súbita. Se han utilizado varias drogas para su control sin éxito. Su tratamiento eficaz requiere la implantación de un cardiodesfibrilador automático, considerando una serie de parámetros, entre ellos la edad, antecedentes de salud personales y familiares, síntomas y signos del paciente, de ahí que la sapiencia y experiencia del médico resulte vital en estos casos.
El Síndrome de Brugada en imágenes.
Ā
Albert Cabrera Marco J. (a); Rodríguez García Marcos A. (b); Pino Peña Yaima C. (c) Flórez Prieto Armando M. (d); Ferras Menéndez Greisa M. (e); Jiménez Gil Yilena (e);Hernández Martínez Laura(e).
Policlínico Universitario Vedado. Plaza de la Revolución, Ciudad de la Habana. Cuba.
Ā
(a)ĀĀĀ Master en Ciencias en Investigación en Aterosclerosis. Especialista de Primer y Segundo Grado en Medicina Interna. Especialista de Segundo Grado en Medicina General Integral. Profesor Auxiliar del ISCM-Habana.
(b)ĀĀĀ Especialista de Primer Grado en Medicina General Integral. Residente de 3er año de Cardiología del Instituto de Cardiología y Cirugía Cardiovascular de Cuba (ICCCV)
(c)ĀĀĀ Especialista de Primer Grado en Medicina General Integral.
(d)ĀĀĀ Estudiante de 2║ año de Ciencias Médicas
(e)ĀĀĀ Estudiantes de 3er año de Ciencias Médicas.
Ā
Resumen
Ā
El síndrome de Brugada es responsable del 4% de los casos de muerte súbita, fenómeno frecuente en la práctica clínica. Descrito alrededor de 17 años atrás por los hermanos Joseph, Ramón y Pedro Brugada, está genéticamente determinado por más de 100 mutaciones de un gen en el cromosoma 3, mostrando una herencia autosómica dominante. Se diagnostica fácilmente por electrocardiografía ante la presencia del patrón típico de bloqueo de rama derecha hisiana asociado a la elevación del punto J y del segmento ST en derivaciones precordiales derechas (V1, V2 y V3), de forma espontánea o tras la administración de antiarrítmicos que bloqueen la actividad del canal de sodio y por ende eleven el segmento ST, entre ellos la flecainida, procainamida y ajmalina, este último el más usado en Cuba. Puede ser detectado en fase asintomática por medio de un chequeo de rutina o en el curso de arritmias ventriculares malignas que causan estados sincopales o incluso muerte súbita. Se han utilizado varias drogas para su control sin éxito. Su tratamiento eficaz requiere la implantación de un cardiodesfibrilador automático, considerando una serie de parámetros, entre ellos la edad, antecedentes de salud personales y familiares, síntomas y signos del paciente, de ahí que la sapiencia y experiencia del médico resulte vital en estos casos.
Ā
Palabras clave: Muerte súbita, Síndrome de Brugada.
Ā
Summary
Ā
Brugada Syndrome is involved in the 4% of cardiac sudden death cases. This syndrome was described by Brugada Brothers (Joseph, Ramón and Pedro) about seventeen years ago. More than 100 mutations of a gene located on chromosome three, determinate it genetically. Diagnosis can be made by electrocardiography, with the characteristic pattern of right bundle-branch block and ST segment elevation in the right leads (V1, V2 and V3), spontaneously or by the administration of antiarrhythmic sodium block channels drugs, such as: flecainide, procainamide and finally ajmaline, the most used in Cuba. It´s often detected by routine checkup or during ventricular arrhythmias, which may cause syncope or even sudden death. Few drugs have unsuccessfully been used to control Brugada Syndrome. Up still now, the only effective treatment consists in the use of an implantable cardioverter defibrillator, however, it´s necessary the experience and doctor's knowledge in order to evaluate some conditions like age, previous illness, familiar health history and symptoms or patient’s signs.
Ā
Keywords: Sudden death, Brugada Syndrome.
Ā
A pesar del descenso que han sufrido los índices de mortalidad de causa cardiaca ajustadas a la edad en los últimos 40 a 50 años, las enfermedades cardiovasculares continúan siendo la primera causa de muerte en países desarrollados y en vías de desarrollo, siendo la muerte súbita responsable de aproximadamente el 50% de ellas. 1
Ā
Ya desde principios del siglo pasado se empezaron a registrar casos de muerte súbita cardiaca (MSC) en países de todo el mundo, un grupo considerable de ellas en individuos fundamentalmente jóvenes en plena capacidad física y sin enfermedad aparente (aunque en la actualidad se conoce que el 90% de los fallecidos presentan alguna afección cardiaca orgánica y solo del 5 al 10% tienen el corazón sano). 1,2,3
Ā
Al síndrome de Brugada (SB) se le atribuye el 4% de todas las muertes súbitas, lo que equivale a 10 por cada 10 000 personas y de hasta un 20% en pacientes con el corazón estructuralmente sano. Es una anomalía eléctrica primaria del corazón, con una base genética y predisposición a arritmias ventriculares rápidas, responsables de su expresión clínica habitual: síncope y/o muerte súbita. 1,4
Al parecer, prevalece en poblaciones de la región del Sureste asiático y se le atribuye parcialmente las muertes súbitas nocturnas conocidas como “lai tai” (muerte durante el sueño) en Tailandia, o como también se le conoce “bangungut” (el ascenso, gemido durante el sueño y luego la muerte) en las Filipinas y “pokkuri” (inesperada muerte súbita cardiaca en la noche) en Japón 5. Las manifestaciones clínicas son 9 veces más frecuentes en hombres, generalmente aparecen en la 3ra o 4ta década de la vida durante el descanso o el sueño. 5, 6
Este síndrome es una canalopatía de origen genético con transmisión autosómica dominante y penetrancia incompleta ocasionada por una variedad de mutaciones de los genes que dan origen a la proteína de los canales de sodio cardiacos, algunas de ellas asociadas además al síndrome de QT largo variante 3 (LQT3). Se hace alusión al gen SCN5A en el cromosoma tres, donde hasta el momento se han identificado más de 100 mutaciones diferentes. Esta parte permanece aún oscura pues dichas mutaciones solo se han detectado en el 30% de los pacientes con el diagnóstico del síndrome, lo que ha obligado a continuar las investigaciones al respecto. 5, 7, 8
Los mecanismos celulares e iónicos de las alteraciones electrocardiográficas y de las arritmias están originados por una actividad anormal de los canales iónicos. Las bases iónicas y celulares del síndrome se han adjudicado a una anomalía del funcionamiento de los canales de sodio en el epicardio del tracto de salida del ventrículo derecho 5, 9, con un predominio de la actividad de las corrientes de potasio que conduce a una pérdida del domo en la fase 2 del potencial de acción originando una heterogeneidad en la repolarización entre el endocardio y epicardio, y por tanto creando una zona vulnerable para la ocurrencia de estas arritmias malignas. 9
Ā
El supradesnivel del segmento ST resulta de la depresión o pérdida de “domo” del potencial de acción en las células del epicardio ventricular derecho, debido a la mayor densidad de corrientes de potasio en esta zona, de ahí su reflejo electrocardiográfico sólo en precordiales derechas. Las arritmias y la muerte súbita se deben al acortamiento del potencial de acción y a la repolarización de tipo “todo o nada”, que originan fenómenos de reentrada en fase 2 con punto de partida en el epicardio del ventrículo derecho. Luego estas arritmias son perpetuadas por las extrasístoles ventriculares asociadas a reentrada en fase 2, con intervalos de acoplamiento muy cortos. Esta conjunción de elementos confiere al síndrome una de sus características únicas: el mismo sustrato origina tanto el disparador como el sostenedor de la arritmia. Las variaciones circadianas explican la mayor incidencia de muerte súbita durante la noche, cuando el tono vagal es más acentuado; sin embargo, el sistema nervioso autónomo parece ser únicamente un modulador del síndrome y no la causa del mismo. 9
El síndrome de Brugada se caracteriza por un patrón electrocardiográfico de aparente bloqueo de rama derecha y supradesnivel del segmento ST que cae con lentitud y finaliza en una onda T negativa en derivaciones precordiales derechas V1, V2 y V3, con dos variantes morfológicas específicas: the coved shape (convexa) y saddle-back (cóncava o en silla de montar). No se produce depresión en las derivaciones opuestas. 1,4,10,11
Ā
En ocasiones se producen variaciones espontáneas y temporales de la morfología precordial del segmento ST, e incluso su normalización transitoria, lo que unido a la existencia de formas ocultas en ocasiones dificulta su reconocimiento. Tal es el caso de la variante precordial alta 4 donde el diagnostico se realiza al ubicar los electrodos exploradores de V1-V3 en el 2║ – 3er espacio intercostal en vez de donde normalmente se colocan (4║).
Ā
Desde el punto de vista clínico existe una tendencia a desarrollar episodios sincopales y/o muerte súbita causados por Arritmias Ventriculares Malignas (AVM) como Taquicardia Ventricular Polimórfica (TVP), Taquicardia Ventricular Monomórfica (TVM) y/o Fibrilación Ventricular (FV) en pacientes sin trastornos electrolíticos, isquemia, ni patología estructural cardiaca que las expliquen. 1,10,11 La respiración agónica nocturna es otra de las manifestaciones más comunes. 6
Ā
Muchos pacientes cursan asintomáticos por largos periodos, otros son diagnosticados mediante la realización de un electrocardiograma (EKG) en un chequeo de rutina y otros por escrutinio debido a la muerte súbita cardiaca de un familiar antes de los 45 años.
Existen pacientes en los que el cuadro clínico se ha interpretado como un síncope vaso-vagal y tiempo después el electrocardiograma (ECG) ha cambiado de normal a completamente patognomónico del síndrome. 6
Ā
En otros pacientes se sospecha el síndrome mas el electrocardiograma (ECG) es completamente normal. En estos casos el diagnóstico requiere la inducción del patrón electrocardiográfico a través de la administración intravenosa u oral de fármacos bloqueadores de los canales de sodio como la ajmalina, flecainida, procainamida, pilsicainida, propafenona y encainida, a dosis terapéuticas. 6
Ā
De forma general existen 3 patrones electrocardiográficos del síndrome de Brugada, mas el tipo 1 es el único con importancia clínica; el resto no cobra relevancia si no se convierten en tipo 1 espontáneamente o tras la inducción farmacológica. La presencia del patrón electrocardiográfico aislado, o sea, en ausencia de sintomatología, indica que se es portador del signo de Brugada, no así el síndrome, como muchos piensan. Estas 3 modalidades son: 12
Ā
·ĀĀĀĀĀĀĀĀ Tipo 1: Patrón convexo y elevación del punto J ≥ 2 milímetros o 0.2 milivoltios a su pico, ST gradualmente descendente en su porción terminal seguido de onda T negativa.
·ĀĀĀĀĀĀĀĀ Tipo 2: Patrón cóncavo, en silla de montar, con elevación del punto J ≥2 milímetros o 0,2 milivoltios, ST gradualmente descendente en su porción terminal, manteniéndose ≥1 milímetro o 0.1 milivoltio por encima de la línea basal seguido de onda T positiva o bifásica. Este tipo es también conocido como Síndrome Pseudo-Brugada.
·ĀĀĀĀĀĀĀĀ Tipo 3: Patrón en silla de montar y elevación del punto J ≥2 milímetros o 0,2 milivoltios, ST gradualmente descendente en su porción terminal, manteniéndose <1 milímetro o 0.1 milivoltio por encima de la línea basal, seguido de onda T positiva.
El diagnóstico diferencial debe establecerse con entidades que muestran patrones electrocardiográficos similares, entre ellos el infarto agudo de miocardio sobre todo del ventrículo derecho, miocarditis aguda, tromboembolismo pulmonar agudo, hiperpotasemia, displasia arritmogénica del ventrículo derecho, Enfermedad de Chagas y especialmente con el bloqueo de rama derecha hisiana asociado con una repolarización precoz (Ver fig. 4), pues esta última se presenta al igual que el síndrome de Brugada en pacientes relativamente jóvenes, deportistas y aparentemente sanos. 13
Ā
El tratamiento de estos pacientes genera una verdadera disyuntiva, pues a pesar de ser una enfermedad potencialmente mortal, muchos pacientes permanecen asintomáticos por años. El único tratamiento que ha logrado salvar vidas es la implantación de un cardiodesfibrilador automático (DAI), el cual es colocado a los pacientes sintomáticos con el patrón tipo I espontáneo o inducido, de acuerdo al consenso internacional.
En los pacientes asintomáticos la decisión es más compleja y teniendo en cuenta que el patrón inducido es de menos riesgo que el espontáneo, los hermanos Brugada recomiendan el cardiodesfibrilador automático implantable (DAI) en todos aquellos donde se ha logrado inducir arritmias ventriculares malignas mediante estimulación eléctrica, conducta no compartida por otros investigadores. Los fármacos constituyen el 2do pilar a valorar, entre ellos el sulfato de quinidina, único medicamento probado que reduce las arritmias ventriculares malignas en estos pacientes. Otros como el tedisamil o isoproterenol, que normalizan el segmento ST y controlan las tormentas eléctricas, pueden ser utilizados. 13
Imágenes:
Ā
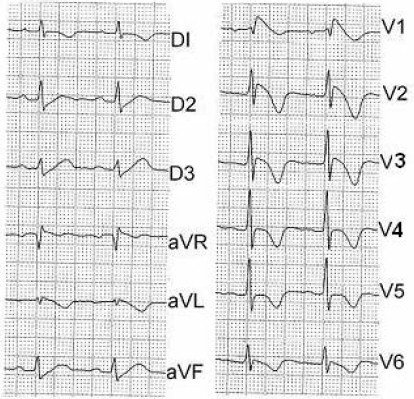
Figura # 1: Electrocardiograma (ECG) Āde 12 derivaciones en un paciente con patrón tipo 1. Nótese el desplazamiento de 3 mm del punto J con el supradesnivel del ST de convexidad superior, así como la negativización asimétrica de la onda T en V1, V2 y V3. Además es notable el patrón de bloqueo de rama derecha RSr´ en V1 y V2 con prolongación del QRS que mide 0.12 segundos.
Ā
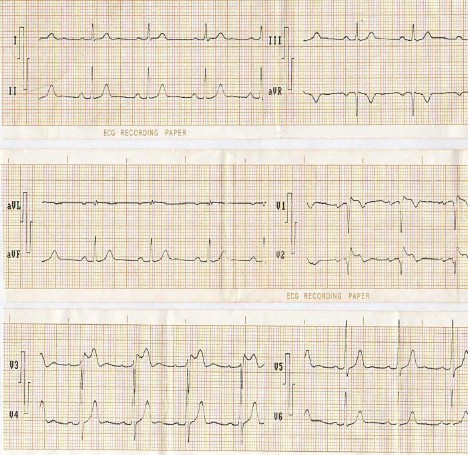
Figura # 2: Electrocardiograma (ECG) Āde 12 derivaciones en un paciente masculino con Síndrome de Pseudo Brugada. Obsérvese los elementos que conforman el patrón electrocardiográfico tipo 2. En este caso el desplazamiento positivo del punto J y del segmento ST (2.5 mm) en las derivaciones precordiales derechas presenta una concavidad superior, semejando una silla de montar con onda T bifásica y el patrón de bloqueo de rama derecha hisiana no tan evidente como el caso anterior pero con un QRS prolongado.
Ā
Ā
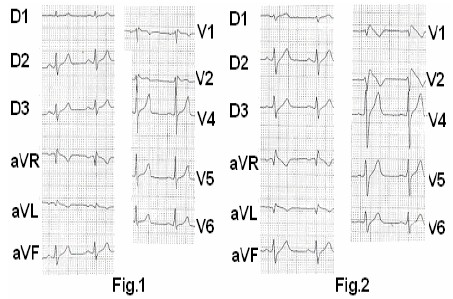
Figura # 3: Electrocardiograma (ECG) Āde 12 derivaciones de un paciente sintomático con SB antes y después de la administración de ajmalina. Inicialmente (Figura 1) el ECG, aunque se aprecia el bloqueo de rama derecha no describe el patrón clásico (tipo 1). Tras la inducción farmacológica con ajmalina (Fig. 2) se produce el supradesnivel convexo del segmento ST, alcanzando casi 4 mm por encima de la isoeléctrica en V2 y se negativiza la onda T con asimetría de sus ramas.
Ā
Ā
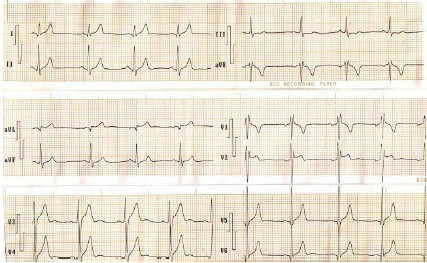
Figura # 4: Electrocardiograma (ECG) Āde 12 derivaciones de un paciente masculino, 19 años, deportista, con signos de despolarización precoz. Nótese el supradesnivel del segmento ST en la totalidad de las derivaciones precordiales (V1- V6) y un patrón de bloqueo de rama derecha que le confiere cierto parecido al SB en las derivaciones V1 y V2.
Referencias bibliográficas
Ā
1.ĀĀĀĀ Rodríguez Mejías J.C, Lardouyet Soto E. Síndrome de Brugada. En: www. bvs. sld.cu/ revistas /san/vol7_ 4_03/ san 08403 .htm 2003. Fecha de acceso: 20-11-08
2.ĀĀĀĀ Giménez Inés Nélida, Foglia C. Yanela, Aguirre Antonio. Síndrome de Brugada: Revisión. Revista de Postgrado de VillIa Clara: Cátedra de Medicina. Febrero 2006. p. 16-20. En: www. google. com.cu . Fecha de acceso: 23-11-08
3.ĀĀĀĀ Giménez Inés Nélida, Foglia C. Yanela, Aguirre Antonio. Síndrome de Brugada: Revisión. Revista de Postgrado de VillIa Clara: Cátedra de Medicina. Febrero 2006. p.16-20. En: www. google. com.cu . Fecha de acceso: 23-11-08
4.ĀĀĀĀ Brugada P, Brugada J. Right bundle-branch block, persistent ST segment elevation with normal QT interval and sudden cardiac death: a distinct clinical and electrocardiographic syndrome. A multicenter report. J Am Coll Cardiol. 1992;20:1391-6.
5.ĀĀĀĀ Chen Q, Kirsch GE, Zhang D, et al. Genetic basis and molecular mechanism for idiopathic ventricular fibrillation. Nature. 1998; 392:293–6.
6.ĀĀĀĀ Braunwald Eugene. Tratado de Cardiología. 7ma ed. Madrid: Gea; 2006. Cap. 28. p. 692. Vol I.
7.ĀĀĀĀ Giménez Inés Nélida, Foglia C. Yanela, Aguirre Antonio. Síndrome de Brugada: Revisión. Revista de Postgrado de VillIa Clara: Cátedra de Medicina. Febrero 2006. p.16-20. En: www. google. com.cu . Fecha de acceso: 23-11-08
8.ĀĀĀĀ Brugada R, Brugada J, Antzelevitch C, et al. Sodium channel blockers identify risk for sudden death in patients with ST-segment elevation and right bundle branch block but structurally normal hearts. Circulation. 2000; 101: 510-5.
9.ĀĀĀĀ Wilde AM, Antzelevitch C, Borggrefe M, et al. Proposed diagnostic criteria for the Brugada syndrome. Consensus report. Circulation. 2002;106:2514-9.
10.Ā Franco Salazar Guillermo. Compendio de Electrocardiografía. 2009. Cap. 1. p. 8.
11.Ā Abud, Atilio. Bagattin, Daniel. Lujan, Osvaldo. Birollo, Oscar. Lovecchio, José. Detección de un síndrome de Brugada en las derivaciones precordiales altas del electrocardiograma de doce derivaciones. Rev Fed Arg Cardiol 2003; 32: 107-109
12.Ā Marill, Keith A. Ellinor, Patrick T. Case 37-2005: A 35-Year-Old Man with Cardiac Arrest while Sleeping. N Engl J Med. 2005; 353:2492-2501
13.Ā Huikuri, Heikki V. Castellanos, Agustin. Myerburg, Robert J. Sudden Death Due to Cardiac Arrhythmias. N Engl J Med. 2001; 345:1473-1482