A menudo se relaciona la aparición de la enfermedad veno‑oclusiva hepática con la administración de busulfán como parte del régimen preparativo para el trasplante de médula ósea, con una menor incidencia de la enfermedad en niños que en adultos. Los intentos de reproducir la enfermedad veno‑oclusiva hepática en la rata tras la administración de dosis altas de busulfán fracasaron, por lo que no se pudo demostrar la correlación anterior, sugiriendo que la administración del busulfán no es la única causa que provoca la aparición de la enfermedad.
Enfermedad veno-oclusiva hepática (EVOH) en ratas tras administración de busulfán.
Navarro Moreno MA, Moreno Gálvez A. Dpto. de Ciencias Experimentales y Matemáticas, Facultad de Ciencias Experimentales, Universidad Católica de Valencia San Vicente Mártir, Valencia (Spain).
Dra. MŞ Ángeles Navarro Moreno. Dpto. de Ciencias Experimentales y Matemáticas. Facultad de Ciencias Experimentales, Universidad Católica de Valencia San Vicente Mártir, Valencia (Spain).
Resumen
A menudo se relaciona la aparición de la enfermedad veno oclusiva hepática con la administración de busulfán como parte del régimen preparativo para el trasplante de médula ósea, con una menor incidencia de la enfermedad en niños que en adultos. Los intentos de reproducir la enfermedad veno oclusiva hepática en la rata tras la administración de dosis altas de busulfán fracasaron, por lo que no se pudo demostrar la correlación anterior, sugiriendo que la administración del busulfán no es la única causa que provoca la aparición de la enfermedad.
Palabras Clave: Enfermedad veno-oclusiva hepática, ratas, busulfán
Introducción
El busulfán es un antineoplásico sintético perteneciente al grupo de los agentes alquilantes, que presenta 4 grupos metileno entre dos grupos metil-sulfonato:
H3C-SO2-O-CH2-CH2-CH2-CH2-O-SO2-CH3
Diferentes autores han atribuido la aparición de la enfermedad veno oclusiva hepática (EVOH) a la administración de altas dosis de busulfán como parte del régimen preparativo para el trasplante de médula ósea 1-5.
El régimen pretrasplante seguido actualmente en clínica consta de la administración de busulfán durante 4 días consecutivos (4 mg/Kg/día) seguido de ciclofosfamida durante el mismo número de días (50 mg/Kg/día). El noveno día tiene lugar el trasplante de médula ósea y la disfunción hepática aparece a los 21 días 6. Como se sabe, la quimioterapia del busulfán es mielosupresiva, mientras que la de la ciclofosfamida es inmunosupresiva 7. El orden de la administración de estos dos antineoplásicos en el régimen pretrasplante se debe a que el individuo tiene que estar el mínimo tiempo posible inmunodeprimido.
De entre la bibliografía disponible, únicamente se ha observado la enfermedad veno oclusiva hepática (EVOH) en tratamientos con busulfán y con la combinación de busulfán y ciclofosfamida 1.
Mientras que para algunos autores los parámetros farmacocinéticos del busulfán no se relacionan con la aparición de enfermedad veno oclusiva hepática (EVOH) 1,8, otros detectan ciertas correlaciones de la enfermedad con determinados parámetros 1,4. En este sentido, Grochow y col. 4 observaron la correlación con bajos valores del aclaramiento plasmático. Posteriormente, los mismos autores 1 relacionaron la enfermedad con elevados valores de AUC del antineoplásico.
Según este último grupo de autores, es conveniente la monitorización de los niveles plasmáticos del busulfán y el cálculo de los parámetros farmacocinéticos para determinar la dosis óptima y así conseguir una mejor eficacia y una menor incidencia de enfermedad veno oclusiva hepática (EVOH).
Las discrepancias entre los trabajos consultados acerca de la relación entre niveles de busulfán y el desarrollo de enfermedad veno oclusiva hepática (EVOH) nos llevaron a intentar reproducir la enfermedad en la rata para establecer la posible relación entre los parámetros cinéticos del busulfán y la enfermedad veno oclusiva hepática (EVOH).
Material y métodos
Se ensayaron varias pautas posológicas con el fin de reproducir dicha enfermedad en la rata. La metódica de trabajo fue la siguiente: finalizado el régimen posológico determinado, se procedió a la anestesia del animal con éter etílico y se sometió a la perfusión con una solución fijadora como se detallará más adelante. Posteriormente se seccionó el hígado, se lavó con alcoholes de distinta graduación y se incluyó en parafina. A continuación, se realizaron cortes histológicos con un microtomo para su posterior coloración y observación en el microscopio.
Administración de una dosis de uretano al 10 % por vía intraperitoneal. Grupo 1.
La administración intraperitoneal de uretano en la rata provoca la aparición de la enfermedad veno-oclusiva hepática. Por ello, con el fin de caracterizar histológicamente la enfermedad en nuestras condiciones experimentales, se procedió a la administración de distintas dosis de uretano a diferentes grupos de animales:
- 2 animales recibieron una inyección intraperitoneal de 5 ml de uretano al 10 %, los cuales murieron un minuto después de la administración.
- 2 animales recibieron una inyección intraperitoneal de 3,5 ml de uretano al 10 %. Estos animales se perfundieron con la solución fijadora para el posterior estudio histológico a las 5 horas después de la administración.
- 3 animales recibieron una inyección intraperitoneal de 3 ml de uretano al 10 %. Dos de ellos se perfundieron a las 5 horas y uno a las 24 horas tras la administración.
El anestésico utilizado en este caso para el proceso de fijación de los órganos fue el hidrato de cloral (450 mg/Kg) en solución al 6 %.
2.2. Administración de una dosis de busulfán por vía intraperitoneal. Grupo 2.
Este grupo estaba constituido por 5 animales:
- 1 de ellos recibió una inyección intraperitoneal de 1 ml de una solución de busulfán, de 50 mg/ml en DMSO, y se perfundió con solución fijadora a las 5 horas después de la administración.
- 1 de ellos recibió una inyección intraperitoneal de 1 ml de una suspensión de busulfán, de 50 mg/ml en metilcelulosa al 0,25 %, y se perfundió a las 4,5 horas después de la administración.
- 2 de ellos recibieron una inyección intraperitoneal de 1,5 y 2,5 ml, respectivamente, de una solución de busulfán, de una concentración de 33,3 mg/ml en DMSO y aceite de oliva. Para su preparación, se disolvieron 200 mg de busulfán en 1 ml de DMSO y posteriormente se añadieron 5 ml de aceite de oliva. Dos horas después de la administración, el segundo animal empezó a presentar fuertes convulsiones y una hora más tarde murió. El primer animal empezó a tener fuertes convulsiones a las 3 horas de la administración y 3 horas después se perfundió con la solución fijadora.
- 1 de ellos recibió una inyección intraperitoneal de 1 ml de metilcelulosa al 0,25 % y durante 24 horas no se observó ninguna manifestación de toxicidad.
2.3. Administración de varias dosis de busulfán por vía oral. Grupo 3.
Para la realización de este ensayo se utilizó un grupo de 10 animales. En todos ellos se llevó a cabo un tratamiento crónico con un seguimiento diario del peso del animal. Para las diferentes administraciones no se anestesiaron los animales. La anestesia previa a la perfusión con la solución fijadora se efectuó con éter etílico.
- 4 animales recibieron 8 administraciones orales de 5 mg cada una de ellas, siendo la dosis total de 40 mg distribuidos en 3 días consecutivos. El primer día recibieron dos administraciones, una a mediodía y otra por la noche. El segundo y tercer día se les administraron tres dosis, por la mañana, a mediodía y por la noche. Los animales se perfundieron con la solución fijadora al cuarto día desde el comienzo del tratamiento.
- 6 animales recibieron una dosis total de 30 mg distribuidos en 12 tomas de 2,5 mg cada una de ellas, durante 4 días consecutivos, administrando tres dosis cada día (por la mañana, a mediodía y por la noche).
Cuadro 1. Resumen de las condiciones correspondientes a los grupos indicados
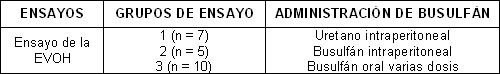
Resultados
En el cuadro 2, se muestran los valores de peso corporal, expresados en gramos, de los animales correspondientes al grupo 3 14. En todos ellos se llevó a cabo un tratamiento crónico, con la administración de varias dosis de busulfán por vía oral, en el que se llevó un seguimiento diario del peso del animal.
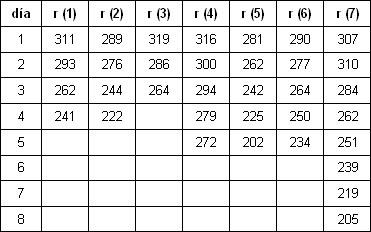
CUADRO 2. Valores de peso corporal, expresado en gramos, correspondientes a los grupos de animales en los que se llevó a cabo un tratamiento crónico, con busulfán administrado por vía oral, con un seguimiento diario del peso del animal. Los tres primeros animales recibieron 8 administraciones orales de busulfán de 5 mg cada una de ellas, siendo la dosis total de 40 mg distribuidos en 3 días consecutivos. Los cuatro últimos animales recibieron una dosis total de 30 mg de busulfán distribuidos en 12 tomas de 2,5 mg cada una de ellas, durante 4 días consecutivos, administrándoles 3 dosis cada día.
En las figuras 1, 2 y 3, se muestra una microfotografía del parénquima hepático de una rata control.
En las figuras 4 y 5, se puede observar una parte del parénquima hepático de una rata a la que se le administraron 3,5 ml de uretano al 10 % por vía intraperitoneal.
En la figura 6, se muestra una microfotografía del parénquima hepático correspondiente a un animal que recibió una inyección intraperitoneal de 1 ml de una solución de busulfán, de 50 mg/ml en DMSO.
En las figuras 7 y 8, se observan dos microfotografías del parénquima hepático correspondientes a una rata que recibió una inyección intraperitoneal de 1 ml de una suspensión de busulfán, de 50 mg/ml, en metilcelulosa al 0,25 %.
En la figura 9, se puede observar el parénquima hepático correspondiente a una rata que recibió una inyección intraperitoneal de 1,5 ml de una solución de busulfán de una concentración de 33,3 mg/ml en DMSO y aceite de oliva.
En la figura 10, se muestra una microfotografía correspondiente al parénquima hepático de un animal que recibió 8 administraciones orales de busulfán de 5 mg cada una de ellas, siendo la dosis total de 40 mg distribuidos en 3 días consecutivos.
En la figura 11, se puede observar una microfotografía del parénquima hepático de una rata que recibió una dosis total de 30 mg de busulfán distribuidos en 12 tomas de 2,5 mg cada una de ellas, durante 4 días consecutivos, administrándole 3 dosis cada día.
FIGURA 1. Microfotografía (x10) correspondiente a una rata control.
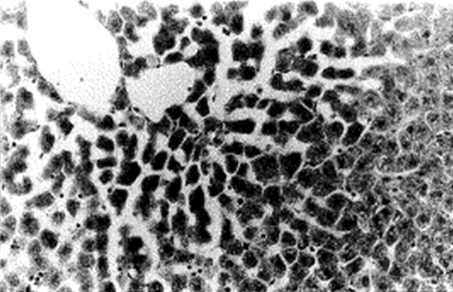
FIGURA 2. Microfotografía (x20) correspondiente a una rata control.
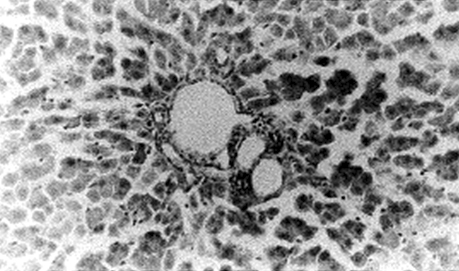
FIGURA 3. Microfotografía (x20) correspondiente a una rata control.
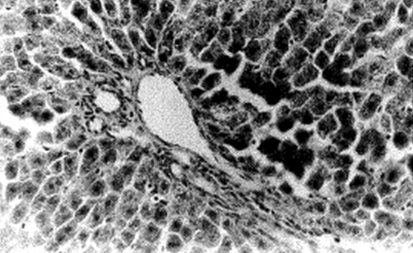
FIGURA 4. Microfotografía (x10) correspondiente a una rata a la que se le administraron 3,5 ml de uretano al 10% por vía intraperitoneal. Obsérvese la vacuolización en los hepatocitos y la separación entre el endotelio y los cordones hepáticos.
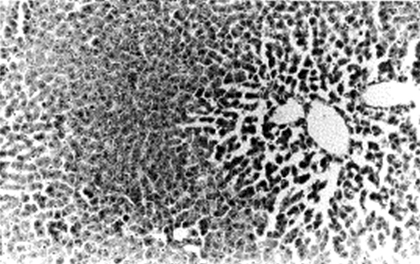
FIGURA 5. Microfotografía (x20) correspondiente a una rata que recibió 3,5 ml de uretano al 10 % por vía intraperitoneal. Obsérvese la separación entre el endotelio y los cordones hepáticos y la vacuolización en los hepatocitos.
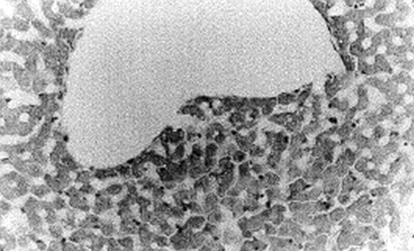
FIGURA 6. Microfotografía (x10) correspondiente a una rata que recibió una inyección intraperitoneal de 1 ml de una solución de busulfán, de 50 mg/ml en DMSO. Obsérvese el parénquima hepático con signos de destrucción (alguna región de necrosis cerca de la tríada).
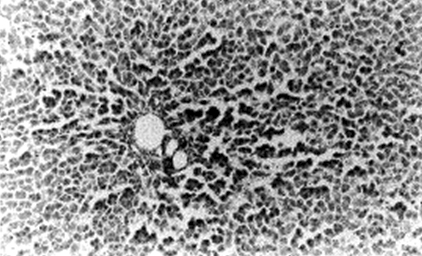
FIGURA 7. Microfotografía (x10) correspondiente al parénquima hepático de una rata que recibió una inyección intraperitoneal de 1 ml de una suspensión de busulfán, de 50 mg/ml, en metilcelulosa al 0,25%. Obsérvese la fragmentación de las células.
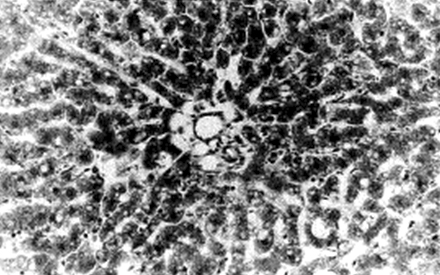
FIGURA 8. Microfotografía (x10) correspondiente al parénquima hepático de una rata que recibió una inyección intraperitoneal de 1 ml de una suspensión de busulfán, de 50 mg/ml, en metilcelulosa al 0,25 %. Obsérvese la fragmentación de las células.
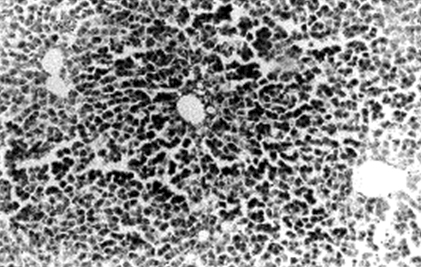
FIGURA 9. Microfotografía (x20) correspondiente al parénquima hepático de una rata que recibió una inyección intraperitoneal de 1,5 ml de una solución de busulfán, de 33,3 mg/ml, en DMSO y aceite de oliva. Obsérvese la presencia de lípidos en el interior de las células.
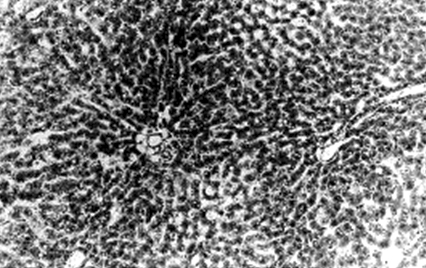
FIGURA 10. Microfotografía (x10) correspondiente al parénquima hepático de una rata que recibió una dosis oral total de 40 mg de busulfán distribuidos en 3 días consecutivos. Obsérvese la infiltración de linfocitos entre los hepatocitos y algunas zonas del parénquima destruidas.
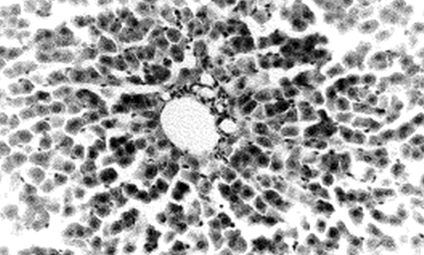
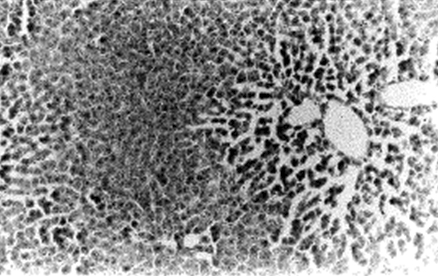
FIGURA 11. Microfotografía (x10) correspondiente al parénquima hepático de una rata que recibió una dosis oral total de 30 mg de busulfán distribuidos en 12 tomas de 2,5 mg cada una de ellas, durante 4 días consecutivos, administrándole 3 dosis cada día. Obsérvese la destrucción del parénquima hepático.
Discusión
Para caracterizar la enfermedad, administramos en primer lugar uretano por vía intraperitoneal y se pudo observar de forma bastante clara la extravasación y posterior oclusión de las venas hepáticas en los cortes histológicos. Este hecho había sido estudiado con anterioridad por distintos autores 9, por lo que la homogeneidad de los resultados obtenidos muestra el efecto tóxico vascular del uretano.
Una vez caracterizada la enfermedad, se administró busulfán en diferentes regímenes con el fín de reproducir la enfermedad veno oclusiva hepática (EVOH), pero no se consiguió. En los hepatocitos de estos animales se observaron grandes alteraciones, pero no se observó la oclusión de las venas hepáticas observada en los animales a los que se les había administrado uretano.
Los animales tratados con busulfán mostraron grandes alteraciones gastrointestinales, pérdidas de peso bastante notables (cuadro 2) y fuertes convulsiones. En ningún caso se manifestó la enfermedad veno oclusiva hepática (EVOH). Incluso algún animal murió antes de poder diagnosticarle histológicamente la enfermedad.
Llama la atención el hecho de que claramente se relaciona la enfermedad con la administración de busulfán y, en nuestro caso, tras la administración de altas dosis del mismo no se consiguiera llegar al diagnóstico histológico de la misma.
A nuestro juicio esto podríamos atribuirlo a varias causas:
En nuestro estudio administramos busulfán en dosis muy altas pero no concomitantemente con ciclofosfamida ni seguido del trasplante de médula ósea (TMO). Aunque la mayoría de los autores relacionan la enfermedad veno oclusiva hepática (EVOH) con la administración de busulfán, en nuestro caso esta administración no llevó consigo la aparición de la enfermedad. Probablemente, la enfermedad veno oclusiva hepática (EVOH) esté relacionada con la terapia conjunta previa al trasplante y/o con el propio trasplante.
Por otra parte, se ha observado que los pacientes con lesiones iniciales en el hígado 10,4 y pacientes con la aspartato aminotransferasa (SGOT) elevada 11 son susceptibles de contraer la enfermedad veno oclusiva hepática (EVOH) a pesar de la individualización de la dosis 4. En nuestro caso, los animales no tenían lesiones iniciales en el hígado ni la SGOT elevada, lo que también podía haber influido en no presentar la enfermedad veno oclusiva hepática (EVOH).
Referencias
1. Grochow LB. Busulfan disposition: the role of therapeutic monitoring in bone marrow transplantation induction regimens. Seminars in oncology 1993; 20: 18 25.
2. Vassal G, Deroussent A, Challine D, Hartmann O, Koscielny S, Valteau Couanet D et al. Is 600 mg/m2 the appropriate dosage of busulfan in children undergoing bone marrow transplantation? Blood 1992; 79: 2475 2479.
3. Peters WP, Henner WD, Grochow LB, Olsen G, Edwards S, Stanbuck S et al. Clinical and pharmacologic effects of high dose single agent busulfan with autologous bone marrow support in the treatment of solid tumors. Cancer Research 1987; 47: 6402-6406.
4. Grochow LB, Jones RJ, Brundrett RB, Braine HG, Chen TL, Saral R et al. Pharmacokinetics of busulfan: correlation with veno-occlusive disease in patients undergoing bone marrow transplantation. Cancer Chemother. Pharmacol 1989; 25: 55-61.
5. Schuler U, Schroer S, Kühnle A, Blanz J, Mewes K, Kumbier I et al. Busulfan pharmacokinetics in bone marrow transplant patients: is drug monitoring warranted?”. Bone Marrow Transplantation 1994; 14: 759-765.
6. Jones RJ, Lee KSK, Beschorner WE, Vogel VG, Grochow LB, Braine HG, Vogelsang GB et al. Veno-occlusive disease of the liver following bone marrow transplantation. Transplantation 1987, 44: 778.
7. Hassan M, Öberg G, Ericson K, Ehrsson H, Eriksson L, Ingvar M et al. In vivo distribution of [11C]-busulfan in cynomolgus monkey and in the brain of a human patient. Cancer Chemother Pharmacology 1992, 30: 81-85.
8. Vassal G, Challine D, Koscielny S, Hartmann O, Deroussent A, Boland I et al. Chronopharmacology of high-dose busulfan in children. Cancer Research 1993; 53: 1534-1537.
9. Doljanski, M.D., y A.Rosin. “Studies on the early changes in the livers of rats treated with various toxic agents, with special reference to the vascular lesions”.
10. Yu LC, Malkani I, Regueira O, Ode DL, Warrier RP. Recombinant Tissue Plasminogen Activator (rt-PA) for veno-occlusive liver disease in pediatric autologous bone marrow transplant patients. American Journal of Hematology 1994; 46: 194-198.
11. McDonald GB, Sharma P, Matthews DE, Shulman HM, Thomas E.D. Veno-occlusive disease of the liver after bone marrow transplantation: diagnosis, incidence and predisposing factors. Hepatology 1984; 4: 116-122.