Con el objetivo de determinar la influencia del sangrado inmediato en la aparición de complicaciones postoperatorias en cirugía cardiovascular realizamos un estudio observacional prospectivo con una serie consecutiva de 1517 pacientes operados de corazón, ingresados en la Unidad de Cuidados Intensivos (UCIQ) del Cardiocentro del Hospital Hermanos Ameijeiras. Se analizaron posibles complicaciones relacionadas con el sangrado excesivo en las primeras 4 horas.
Relación entre sangramiento postoperatorio inmediato y complicaciones en la cirugía cardiovascular
MSc. Dr. Francisco José Pérez Santos. Especialista en Medicina Familiar y Medicina Interna. Master en Urgencias Médicas.
Dr. José Carlos Almeida Pina. Especialista en Medicina Interna y Medicina Intensiva y Emergencias.
Dr. Carlos Rafael Moret Hernández. Especialista en Medicina Interna.
Dr. Abdel Pérez Navarro. Especialista en Medicina Interna.
MSc. Dr. Liván A. Gil Sosa. Especialista en Medicina Interna y Medicina Intensiva y Emergencias.
MSc. Dra. Sinay García Nidetz. Especialista en Medicina Familiar y Nefrología. Master en Urgencias Médicas
Hospital Clínico Quirúrgico Hermanos Ameijeiras
Resumen
Con el objetivo de determinar la influencia del sangrado inmediato en la aparición de complicaciones postoperatorias en cirugía cardiovascular realizamos un estudio observacional prospectivo con una serie consecutiva de 1517 pacientes operados de corazón, ingresados en la Unidad de Cuidados Intensivos (UCIQ) del Cardiocentro del Hospital Hermanos Ameijeiras. Se analizaron posibles complicaciones relacionadas con el sangrado excesivo en las primeras 4 horas.
Se tomó como nivel de significación estadística una p<0.05. Del total de pacientes, 260 (17,2%) presentaron sangrado excesivo, predominó el sexo masculino (64,7%) comprobándose rebote de heparina en 113 (43,8%), déficit o disfunción plaquetaria en 63 (24,2%), otros trastornos de la coagulación en 41(15,7%) y hemostasia deficiente en 43 (16,5%) p<0,05.
De las reintervenciones, el 61,8% lo fue por sangrado excesivo. Se asoció a disfunción neurológica (15,3%), pulmonar (17,3%), renal (19%), hepática (11,1%), gastrointestinal (8,2%), bajo gasto cardiaco (BGC) (21,4%), arritmias supraventriculares (24,7%), ventriculares (10,1%), falla multiórgano (16,9%), sepsis (31,2%) y muerte (15%). Aumentó el tiempo de ventilación, los días de sangrado y la estadía en la Unidad de Cuidados Intensivos (UCIQ), con mayor consumo de sangre y hemoderivados en las primeras 24 y 48 horas en los casos con sangrado excesivo. Concluimos que el sangrado de las primeras 4 horas tiene valor predictivo en la aparición de otras complicaciones, por el mayor consumo de sangre, de hemoderivados y el mayor número de reintervenciones por esta causa.
Palabras clave: Cirugía cardiaca, circulación extracorpórea, sangrado posquirúrgico.
Abstract
Expected and unexpected bleeding occurs frequently in patients undergoing cardiac surgery, excessive bleeding is associated with adverse outcomes. To evaluate the complications related to bleeding in patients subjected to cardiac surgery using an extracorporeal circulation pump a prospective study was perform in 1517 consecutive patient admitted at the cardiovascular ICU of a tertiary hospital. Results were analyzed by Student t test and chi-square considering p values significant at <0.05. Heavy bleeding was found in 260 (17,2%) patient, mostly in male (64,7%).
The principal causes was heparin overdoses 113 (43,8%), Plaquetary dysfunction in 63 (24,2%) patients, and others inconvenience in 41(15,7%) and deficient haemostasis in 43 (16,5%) p<0,05. The most frequent complication were neurology dysfunction (15,3%), pulmonary (17,3%), renal (19%), hepatic (11,1%), gastrointestinal (8,2%), low output syndrome (21,4%), supraventricular arrhythmias (24,7%), ventricular arrhythmias (10,1%), multiorgan fall (16,9%), sepsis (31,2%) and death (15%). We conclude that excessive bleeding have and prognostic value. A thorough understanding of these factors is necessary to reduce bleeding. This is a desirable clinical goal
Key words: Cardiac surgery, extracorporeal circulation, excessive bleeding,
Introducción
La Cirugía Cardiovascular mantiene una tendencia creciente en cuanto a número de operaciones, diversidad e indicaciones. En las primeras horas de la recuperación postquirúrgica se desarrollan un gran número de complicaciones que ponen en riesgo la vida del paciente. El uso de la circulación extracorpórea (CEC) en el desarrollo de la cirugía cardiovascular puede provocar algunas complicaciones; una de las más frecuentes es el sangrado postoperatorio que lleva a un aumento importante en la reposición de sangre y hemoderivados, re-intervenciones en el posquirúrgico inmediato, estancia prolongada en UCI, duración de la hospitalización y un aumento en la morbimortalidad en el paciente. La hemorragia asociada con la cirugía cardiaca puede ser devastadora y una amenaza para la vida, se calcula que la incidencia de la mortalidad por hemorragia asociada con la circulación extracorpórea (CEC) varía entre el 5% y 25%.
Los trastornos hemobiológicos producidos durante la circulación extracorpórea (CEC) son debidos a fenómenos mecánicos por el contacto de la sangre con las superficies no endotelizadas de la máquina de CEC, así como a las fuerzas reológicas aplicadas sobre las células. La circulación extracorpórea (CEC) induce una coagulopatía secundaria a hemodilución, consumo de elementos y factores de la coagulación y a la hipotermia que se asocia con una supresión generalizada de la cascada de la coagulación. El consumo obedece a varias causas. Por una parte las plaquetas sufren alteraciones cualitativas y cuantitativas. El número de plaquetas disminuye debido a los traumatismos mecánicos, la adherencia a las superficies artificiales, la pérdida de sangre, y la coagulación intravascular subclínica inducida por el by-pass cardiopulmonar (BCP). Las plaquetas remanentes se tornan disfuncionantes por la degranulación, proceso que reduce la agregación plaquetaria, ya de por si disminuida por el tratamiento antiagregante previo. Así mismo durante el by-pass cardiopulmonar (BCP) se produce la destrucción y consumo de los distintos factores de la coagulación, cuya actividad se encuentra reducida posteriormente en un 30-60%.
Otra causa son las reacciones bioquímicas debidas a factores mecánicos como son los choques, contactos y fuerzas de cizallamiento producidas por la bomba, la tensión de superficie y la fuerte presión negativa utilizada en la aspiración de sangre del campo operatorio. Estas reacciones incluyen la formación de proteasas, responsables de la aparición de trastornos hemostáticos, hemodinámicos e inflamatorios.
Entre las complicaciones el sangrado excesivo es la mayor causa de morbilidad postoperatoria. Las consecuencias de la anemia en el paciente crítico incluyen una inadecuada oxigenación tisular y eventualmente isquemia de los órganos terminales como pulmón, corazón, hígado y cerebro. La decisión de transfundir depende de un juicio clínico, que requiere sopesar los posibles beneficios y los riesgos conocidos frente a los tratamientos alternativos.
En los últimos años los requerimientos transfusionales han disminuido, gracias al mejor conocimiento de los cambios en los mecanismos de la coagulación que se producen en este tipo de cirugía y la creación de nuevas técnicas y medicamentos encaminados a la prevención del sangrado intra y postoperatorio. Estos cambios en la medicina transfusional van encaminados a disminuir la morbimortalidad relacionada con la administración de sangre y hemoderivados. 1-7 En la actualidad, las transfusiones son, probablemente, más seguras que nunca, pero el riesgo, así como la percepción del mismo y el temor a la transmisión de enfermedades del público, obligan a obtener el consentimiento informado del paciente.
Se han desarrollado nuevas técnicas (farmacológicas y no farmacológicas), encaminadas a disminuir el consumo de sangre homóloga en el perioperatorio.
Entre las técnicas no farmacológicas, tenemos la hemodilución, la autotransfusión programada, la autotransfusión perioperatoria mediante hemodilución normovolémica, de recuperación intraoperatoria de sangre del campo operatorio (Cell Saver) y en el postoperatorio, del reservorio de drenaje mediastinal, hemoconcentración por hemofiltración y plasmaféresis perioperatoria entre otras. (8 – 17)
Las técnicas farmacológicas incluyen el uso de Aprotinina, Ácido Tranexámico y Ácido Epsilon Aminocaproico (EACA) Otros menos utilizados son: Desmopresina, Prostaciclina y Dipiridamol. (18 – 30)
Motivados por la frecuencia del sangrado excesivo en el postoperatorio inmediato de esta cirugía, nos propusimos estudiar esta complicación como causa de otras complicaciones y el valor predictivo de su cuantificación en las primeras 4 horas.
Objetivos
General:
Determinar el valor predictivo del sangrado inicial postoperatorio en la aparición de otras complicaciones en cirugía cardiovascular.
Específicos:
1. Determinar la influencia del sangrado inicial sobre otras complicaciones postoperatorias en cirugía cardiovascular y su valor predictivo.
2. Valorar el consumo de sangre y hemoderivados de los pacientes con sangrado excesivo.
3. Analizar las causas de re-intervenciones.
Material y Método
Se realizó un estudio observacional prospectivo con una serie consecutiva de 1517 operaciones de corazón e ingresados en la Unidad de Cuidados Intensivos (UCIQ). A todos se les aplicó el mismo protocolo intraoperatorio de trabajo, apoyado en una anestesia general balanceada con el uso de benzodiacepinas, morfínicos, halogenados y relajantes musculares no despolarizantes. Las técnicas quirúrgicas y de circulación extracorpórea fueron similares. El tiempo de coagulación activado basal para pacientes normales oscila entre los 100 y los 130 segundos, mientras que el valor medio tras la infusión de 3mg/Kg. de heparina se encuentra entre los 450 y 500 segundos.
La anticoagulación durante este período se realizó con heparina a razón de 3 mg/Kg de peso como dosis inicial, controlada por Tiempos de Coagulación Activados (TCA) por encima de 480 segundos, con dosis adicionales de 1 mg/Kg si el Tiempo de Coagulación Activado (TCA) descendía por debajo de ese valor. Al final de la CEC, la heparina residual se revirtió con una infusión lenta de Sulfato de Protamina en proporción a la dosis de heparina (1,2- 1,5); de ser necesario, se administraron dosis adicionales de 30 a 50 miligramos.
A todos los pacientes se les administró de forma profiláctica épsilon aminocaproico (EACA) (100-150 mg/Kg) o Ácido Tranexámico (10 mg/kg), previo a la incisión quirúrgica y al final de la CEC, antes de la administración del Sulfato de Protamina, con el objetivo de reducir el sangrado postoperatorio.
Se consideró sangrado excesivo la presencia de más de 500ml (8 ml/kg) en la 1rŞ hora, mas de 400 ml (7ml/Kg) en la segunda hora, mas de 300 ml (6 ml/Kg) en la tercera hora, mas de 5 ml/Kg/hora durante cualquier hora posterior, sangrado total mayor de 1000 ml en las primeras 4 horas, mas de 200 ml durante 3 horas consecutivas o incremento brusco del sangrado. Se indicaron exámenes de la coagulación (Tiempos de Coagulación Activados (TCA) y/o coagulograma) cuando se constataron pérdidas anormales.
Se denominó primer día desde la salida del salón de operaciones hasta las 6:00 AM del día siguiente y segundo día hasta las 6:00 AM del tercer día. Se consideró rebote de heparina cuando el Tiempo de Coagulación Activado (TCA) fue superior a los 140 segundos en presencia de sangramiento excesivo.
Se valoró también el tiempo de ventilación mecánica, la estadía en la Unidad de Cuidados Intensivos (UCIQ) y las causas de reintervenciones, así como las posibles complicaciones relacionadas con el sangrado excesivo en las primeras 5 horas. La información fue registrada en una base de datos computarizada, de forma prospectiva y de actualización en tiempo real. Procesamiento estadístico: Para variables cualitativas se utilizó la prueba de Chi cuadrado expresado en valores absolutos y relativos, para los valores cuantitativos la T de Student, expresando los valores en media y desviación estándar. Se tomó como nivel de significación estadística una p 0,05.
Resultados:
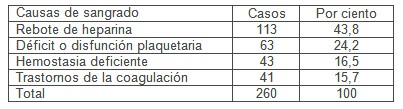
Del total de los pacientes estudiados fue encontrado sangrado excesivo en las primeras 4 horas del postoperatorio en 260 pacientes (17,2%). De estos comprobamos rebote de heparina en 113 (43,8%), disfunción plaquetaria en 63 (24,2%), otros trastornos de la coagulación en 41(15,7%) y hemostasia deficiente en 43 (16,5%). Estos datos se muestran en la tabla 1. En el periodo de estudio de los pacientes reintervenidos el 61,8% lo fue por sangrado excesivo.
Tabla 1. Causas de sangrado excesivo en el postoperatorio de cirugía cardíaca.
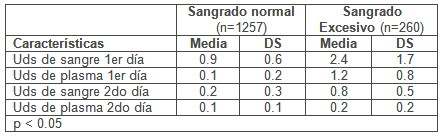
La tabla 2 muestra la relación del consumo de sangre y plasma en los dos primeros días de evolución tanto en los pacientes con sangrado normal como excesivo. La media del consumo de unidades de sangre fue de 0,9 y 0,2 el primer y segundo día en los pacientes con sangrado normal y de 2,4 y 0,8 en los de sangrado excesivo.
Por otra parte el consumo de plasma fue de 0,1 unidades en ambos días por paciente con sangrado normal y de 1,7 y 0,5 unidades el 1er y 2do día respectivamente en los pacientes con sangrado excesivo.
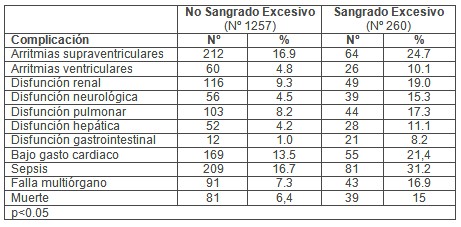
La tabla 3 muestra las complicaciones postoperatorias asociadas tanto en el grupo de sangrado excesivo como no excesivo. Los porcientos en que aparecieron las complicaciones fueron inferiores en todas en el grupo de sangrado normal comparado con el de sangrado excesivo; arritmias supraventriculares (16.9 vs 24.7%), ventriculares (4.8 vs 10.1%), disfunción renal (9.3 vs 19.0%), disfunción neurológica (4.5 vs 15.3%), disfunción pulmonar (8.2 vs 17.3%), disfunción hepática (4.2 vs 11.1%), disfunción gastrointestinal (1.0 vs 8.2%), bajo gasto cardíaco (BGC) (13.5 vs 21,4%), sepsis (16.7 vs 31.2%), falla múltiple de órganos (7.3 vs 16.9%) y muerte (3,1 vs 4,8%).
Tabla Nş 2. Consumo de sangre y hemoderivados postoperatorios.
Fuente: dato primario. Uds: unidades DS: Desviación estándar
Tabla Nş 3: Complicaciones postoperatorias asociadas.
Fuente: Dato primario. No.: Número%: Por ciento en relación a Nş de cada columna.
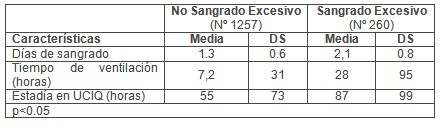
Tabla Nş 4. Relación entre carácter del sangrado y tiempo de sangrado, ventilación y estadía.
Fuente: Dato primario. DS: Desviación estándar
En la tabla 4 aparece la relación entre carácter del sangrado y tiempo de sangrado, ventilación y estadía. La media de días de sangrado fue de 1,3 en los pacientes con sangrado normal y 2,1 en lo de sangrado excesivo, las horas de ventilación de 7,1 vs 28 y la estadía de 55 vs 87 horas respectivamente.
Discusión
Estudios amplios y a nivel mundial reporta que la reintervención por sangrado ocurre en 5 a 7% de los casos asociándose a esta complicación una mortalidad que va desde el 5 a 25%, alcanzando en el grupo pediátrico hasta un 35%. Los mecanismos de alteración de la función plaquetaria incluyen daño en la membrana debido al contacto con material extraño, que puede resultar en la liberación de los contenidos plaquetarios, un revestimiento de la membrana con proteínas no específicas o productos de la degradación de las proteínas; o daño no definido producido por el flujo de la bomba. Estos daños se vuelven más pronunciados en perfusiones que duran más de sesenta minutos y depende también de las técnicas utilizadas en las mismas, como el flujo, el sistema de oxigenación utilizado, el tipo de bomba, la composición del primado y si la perfusión se realiza en normotermia o hipotermia.
El rebote heparínico ha sido definido entonces, como la reaparición de sangrado clínico y tiempo de coagulación prolongado luego de la neutralización con sulfato de protamina. El rango en el cual la heparina es metabolizada, la cantidad de sulfato de protamina necesario para la neutralización y la respuesta del paciente a la heparina está sujeta a grandes variaciones. La etiología del rebote heparínico no ha sido clarificada satisfactoriamente. Se conoce que la heparina se une al endotelio y lo que sucedería es una liberación tardía de esta. Los tiempos prolongados de coagulación ocurren una hora después de la neutralización de la heparina y puede prolongarse hasta las 6 horas.
La actividad fibrinolítica generalmente decrece o se inhibe durante y después de la mayoría de los procedimientos quirúrgicos generales. Pero en cirugía con circulación extracorpórea (CEC) ocurre todo lo contrario. Otros señalan que la mortalidad aumentó del 3,3% al 9,5% en los pacientes reintervenidos por esta causa. (31) En nuestro estudio la mortalidad fue de 6,4 en el grupo de sangrado normal y de 15% en el grupo de sangrado excesivo.
El mayor consumo de sangre y hemoderivados, el primer y segundo días del postoperatorio en el grupo con sangrado excesivo, se explica por el mayor volumen de pérdidas hemáticas. El plasma solo se utilizó para corregir desórdenes de la coagulación. (8,9,33,36)
El origen de las arritmias encontradas es multifactorial, invocándose trastornos hidroelectrolíticos, temperatura, alteraciones en los haces de conducción eléctrica por edema de la zona quirúrgica, isquemia, etc.
Como factores postoperatorios de riesgo de disfunción neurológica se ha encontrado el uso de sangre y hemoderivados, el sangrado mayor de 75 ml/m2/hora en las primeras cinco horas, el paro cardiaco, el Síndrome de Bajo Gasto Cardiaco (BGC), la re-intervención quirúrgica, la diuresis aumentada y la fibrilación auricular. Tiene una incidencia esta complicación entre el 1,3 y 31,9% con una mortalidad de alrededor del 42%. (37-39)
En los pacientes con falla multiórgano (FMO) en general, los órganos o sistemas más afectados son el respiratorio, el cardiovascular, el hígado y el riñón con una mortalidad entre un 30 y 80%. Su fisiopatología aun no es clara, intervienen varios factores entre los que se cita el sangrado excesivo y la administración masiva de sangre y de hemoderivados. (40-42)
El bajo gasto cardiaco (BGC) es una complicación frecuente caracterizada por cambios hemodinámicos e hipoperfusión visceral con aumento de la demanda miocárdica de oxígeno producida por la anemia aguda, la taquicardia y la falla de bomba. Es una causa importante de muerte. (6, 31, 37, 40,43)
Existe gran relación entre el sangrado excesivo, la re-intervención, el consumo elevado de sangre y la sepsis. Esta complicación aumentó la estadía hospitalaria y la mortalidad en una amplia revisión de Stahle E. y colaboradores que encontraron una incidencia de sepsis del 1,7% después de cirugía de revascularización y de 0,7% en cirugía de valvulares. (44)
Existen varios factores postoperatorios predisponentes de disfunción renal aguda: bajo gasto cardiaco (BGC), infarto agudo del miocardio (IMA) perioperatorio, paro cardiaco, ventilación mecánica prolongada, reoperación, sangrado excesivo, coma y mediastinitis. (45)
La disfunción pulmonar aumenta en relación con la cantidad de sangre y hemoderivados administrados y como parte de una falla multiórgano (FMO) alcanza una mortalidad entre 65,5 y 78,6%. (40,41)
La disfunción gastrointestinal encierra una alta morbimortalidad. Encontramos íleo paralítico, hepatopatías, úlcera gastroduodenal sangrante y pancreatitis aguda. Estudios como el de González Ojeda y colaboradores informan de una incidencia de complicaciones gastrointestinales del 3,3% y dentro de éstas, la disfunción hepática ocupó un 29,5% con una mortalidad cercana al 25%. (43,46-49)
En los pacientes con sangrado excesivo, la acumulación de coágulos perpetúa una hiperfibrinolisis que aumenta el tiempo de sangrado. Esto ha sido igualmente reportado por otros autores. (34, 35, 50-52)
Mientras persista la inestabilidad hemodinámica, alteraciones de la coagulación o el paciente por el volumen de sangrado, tenga posibilidad de ser reintervenido, no se comienza el destete ventilatorio, lo que explica el mayor tiempo de ventilación mecánica necesitado por estos pacientes. La estadía en Unidad de Cuidados Intensivos (UCIQ), aumentó en los pacientes con sangrado excesivo como consecuencia de la elevada tasa de morbimortalidad relacionada con esta complicación; la mayor administración de sangre, de hemoderivados y de las reintervenciones por esta causa.
Conclusiones
1. El sangrado excesivo postoperatorio inmediato influye significativamente en la aparición de otras complicaciones: Arritmias supraventriculares, ventriculares, disfunción neurológica, muerte, falla multiórgano (FMO), disfunción pulmonar, renal, hepática, gastrointestinal y sepsis y en el aumento de los días de sangrado, tiempo ventilatorio y estadía en Unidad de Cuidados Intensivos (UCIQ).
2. El sangrado en este periodo (4 horas) tiene valor predictivo por su estrecha relación con las complicaciones analizadas.
3. Hubo mayor consumo de sangre y hemoderivados el primer y segundo días del postoperatorio en los pacientes con sangrado excesivo.
4. Más de la mitad de las re-intervenciones son debidas a sangrado excesivo.
Bibliografía
1. Hess PJ Jr. Systemic inflammatory response to coronary artery bypass graft surgery. Am J Health Syst Pharm 2005, 62:S6-S9.
2. Hertfelder HJ, Bos M, Weber D, Winkler K, Hanfland P, Preusse CJ Perioperative monitoring of primary and secondary hemostasis in coronary artery bypass grafting. Semin Thromb Hemost 2005, 31:426-440.
3. McCusker K, Lee S, Jack DN. Post cardiopulmonary bypass bleeding: an introductory review. J Extra Corpor Technol 1999 Mar;31 (1):23-36.
4. Levi M, Cromheecke ME, de Jonge E, Prins MH, de Mol BJ, Briet E, et al. Pharmacological strategies to decrease excessive blood loss in cardiac surgery: a meta-analysis of clinically relevant endpoints. Lancet 1999 Dec 4; 354 (9194): 1940-7.
5. Moulton MJ, Creswell LL, Mackey ME, Cox JL, Rosenbloom M Reexploration for bleeding is a risk factor for adverse outcomes after cardiac operations. J Thorac Cardiovasc Surg 1996, 111:1037-1046.
6. Welsby IJ, Podgoreanu MV, Phillips-Bute B, Mathew JP, Smith PK, Newman MF, Schwinn DA, Stafford-Smith M Genetic factors contribute to bleeding after cardiac surgery. J Thromb Haemost 2005, 3:1206-1212.
7. Donahue BS, Gailani D, Higgins MS, Drinkwater DC, George AL Jr. Factor V Leiden protects against blood loss and transfusion after cardiac surgery. Circulation 2003, 107:1003-1008.
8. Carroll RC, Chavez JJ, Snider CC, Meyer DS, Muenchen RA Correlation of perioperative platelet function and coagulation tests with bleeding after cardiopulmonary bypass surgery. J Lab Clin Med 2006, 147:197-204.
9. Karthik S, Grayson AD, McCarron EE, Pullan DM, Desmond MJ Reexploration for bleeding after coronary artery bypass surgery: risk factors, outcomes, and the effect of time delay. Ann Thorac Surg 2004, 78:527-534.
10. Díaz Gonzales M. Caracterización del Sangrado Pos-Quirúrgico en Cirugía Cardiaca con Circulación Extracorpórea. Rev Latinoamer Tecnol Extracorp 2007; 14(2): 26-39.
11. Mac Lennan S, Murphy MF. Survey of the use of whole blood in current blood transfusion practice. Clin Lab Haematol 2001 Dec; 23 (6):391-6.
12. Nuttall GA, Henderson N, Quinn M, Blair C, Summers L, Williams BA, Oliver WC, Santrach PJ Excessive bleeding and transfusion in a prior cardiac surgery is associated with excessive bleeding and transfusion in the next surgery. Anesth Analg 2006, 102:1012-1017.
13. John LC, Deverall PB. Current methods to reduce the adverse haematological consequences of cardiopulmonary bypass. Br J.Clin Pract 1996 Jun; 50(4):203-6.
14. Parr KG, Patel MA, Dekker R, Levin R, Glynn R, Avorn J, Morse DS Multivariate predictors of blood product use in cardiac surgery. J Cardiothorac Vasc Anesth 2003, 17:176-181.
15. Despotis GJ, Skubas NJ, Goodnough LT. Optimal management of bleeding and transfusion in patients undergoing cardiac surgery. Semin Thorac Cardiovasc Surg 1999 Apr;11(2):84-104.
16. Komiya T, Ban K, Yamazaki K, Date O, Nakamura T, Kanzaki Y. Blood conservation effect and saffety of sed mediastinal blood, autotransfusión after cardiac surgery. Jpn. J. Thorac. Cardiovasc. Surg. 1998 Oct;46(10): 961-5.
17. Body SC, Birmingham J, Parks R, Ley C, Maddi R, Shernan SK et al. Safety and efficacy of shed mediastinal blood transfusion after cardiac surgery: a multicenter observational study. Multicenter Study of Perioperative Ischemia. J Cardiothorac Vasc Anesth 1999 Aug; 13(4):410-6.
18. McGill N, O'Shaughnessy D, Pickering R, Herbertson M, Gill R. Mechanical methods of reducing blood transfusion in cardiac surgery: randomised controlled trial. BMJ 2002 Jun 1;324(7349):1299.
19. Gomez-Ambrosi J, Salvador J, Silva C, Pastor C, Rotellar F, Gil MJ, Cienfuegos JA, Fruhbeck G Increased cardiovascular risk markers in obesity are associated with body adiposity: Role of leptin. Thromb Haemost 2006, 95:991-996.
20. Cross MH. Autotransfusion in cardiac surgery. Perfusion 2001 Sep; 16(5):391-400.
21. Hashimoto K, Onoguchi K, Sasaki T, Hachiya T, Takakura H, Nagahori R, et al. Strategy for balancing anticoagulation and hemostasis in aortocoronary bypass surgery: blood conservation and graft patency. Jpn Circ J 1999 Mar; 63(3):165-9.
22. Sainz CH, Rodríguez SF, Santos GJ, González-Prendes AC, García MB Acido Epsilón Aminocaproico (EACA): Efecto de su administración profilactica en Cirugía Cardiaca En: Actas del XXIII Congreso Latinoamericano de Anestesiología. La Habana. 1995: 59.
23. Morlans HK, Prado SE, González-Prendes AC, García MB, Rodríguez SF, Santos GJ y cols. Disfunción neurológica en el postoperatorio inmediato de la Cirugía cardiovascular: Factores de riesgo, complicaciones asociadas, mortalidad y estadía. Revista Cubana de Cardiología y Cirugía Cardiovascular 1999; 13(2): 142-8.
24. Morlans HK, Santos GJ, González-Prendes AC, Rodríguez SF, García MB, Sainz CH. Falla Orgánica Múltiple. Acercamiento al tema. Revista Cubana de Cardiología y Cirugía Cardiovascular 1999; 13(1): 61-71.
25. Jimenez Rivera J, Iribarren J Raya J, Nassar I. Factors associated with excessive bleeding in cardiopulmonary bypass patients: a nested case-control study. Journal of Cardiothoracic Surgery 2007, 2:17
26. Despotis GJ, Avidan MS, Hogue CW Jr. Mechanisms and attenuation of hemostatic activation during extracorporeal circulation. Ann Thorac Surg 2001, 72:S1821-S1831.
27. American Heart Association. "Open-heart surgery statistics." 2007 http://americanheart.org/presenter.jhtml?identifier=4674
28. New York State Department of Health. "Adult cardiac surgery in New York State, 2002-2004. www.health. state.ny.us /diseases/ cardiovascular/ heart_disease /docs /cabg _2002-2004.pdf
29. Steiner, M. E., & Despotis, G. J. (2007). Transfusion algorithms and how they apply to blood conservation: The high-risk cardiac surgical patient. Hematol Oncol Clin North Am, 21(1), 177.
30. Society of Thoracic Surgeon Blood Conservation Guideline Task Force and Society of Cardiovascular Anesthesiologists Special Task Force on Blood Transfusion. (2007). Perioperative blood transfusion and blood conservation in cardiac surgery: The Society of Thoracic Surgeons and the Society of Cardiovascular Anesthesiologists clinical practice guidelines. Ann Thorac Surg, 2007; 83(5 Suppl), S27.
31. Hall, T. S., Brevetti, G. R., et al. Re-exploration for hemorrhage following open heart surgery differentiation on the causes of bleeding and the impact on patient outcomes. Ann Thorac Cardiovasc Surg, 2001.7(6), 352.
32. Pass, S., & Simpson, R. "Discontinuation and reinstitution of medications during the perioperative period." Am J Health-Syst Pharm, 2004; 61(9), 899.
33. Vincentelli, A., Jude, B. et al. Antithrombotic therapy in cardiac surgery. Can J Anesth, 2006; 53(6), S89.
34. Harrington, R., Becker, R. et al. Antithrombotic therapy for coronary artery disease: The seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest, 2004; 126, 513S.
35. 9Bhatt, D. L., Aranki, S., et al. Issues in the management of antiplatelet therapy in patients undergoing surgical revascularization: A roundtable discussion. J Invasive Cardiol, 2005; 17(5), 283.
36. 10. Mannucci, P. M. & Levi, M. Prevention and treatment of major blood loss. N Engl J Med, 2007; 356 (22), 2301.
37. Food and Drug Administration. "FDA requests marketing suspension of Trasylol." 2007 www.fda.gov/bbs/topics/NEWS/2007/NEW01738.html
38. Arellano, R., Gan, B. S., et al. A triple-blinded randomized trial comparing the hemostatic effects of large-dose 10% hydroxyethyl starch 264/0.45 versus 5% albumin during major reconstructive surgery. Anesth Analg, 2005, 100(6), 1846.
39. Food and Drug Administration. "FDA approves Voluven to treat serious blood volume loss following surgery." 2007. www.fda.gov/ bbs/topics/ NEWS/2007/ NEW0 1765.html Spiegelhalter D, Grigg O, Kinsman R. et al Risk‐adjusted sequential probability ratio tests: applications to Bristol, Shipman and adult cardiac surgery. Int J Qual Health Care 2003. 157–13.
40. Bucknell S J, Mohajeri M, Low J. et al Single‐versus multiple‐dose antibiotics prophylaxis for cardiac surgery. ANZ J Surg 2000. 70409–411.
41. Karthik S, Grayson A D, McCarron E E. et al Reexploration for bleeding after coronary artery bypass surgery: risk factors, outcomes, and the effect of time delay. Ann Thorac Surg 2004. 78527–534.
42. Dacey L J, Munoz J J, Baribeau Y R. et al Reexploration for hemorrhage following coronary artery bypass grafting: incidence and risk factors. Arch Surg 1998. 133442–447.
43. Bolsin S N, Colson M. Methodology matters; CUSUM. Int J Qual Health Care 2000. 12433–438.
44. Bolsin S. Routes to quality assurance: risk adjusted outcomes and personal professional monitoring. Int J Qual Health Care 2000. 12367–369.
45. Woodall W H. The use of control charts in health‐care and public‐health surveillance (with Discussion). J Qual Technol 2006. 3889–134.
46. Poloniecki J, Sismanidis C, Bland M. et al Retrospective cohort study of false alarm rates associated with a series of heart operations: the case for hospital mortality monitoring groups. BMJ 2004. 328375–379.]
47. Steiner S H, Cook R J, Farewell V T. et al Monitoring surgical performance using risk‐adjusted cumulative sum charts. Biostatistics 2000. 11441–1452.
48. Bird S M, Cox D, Farewell V T. et al Performance indicators: good, bad, and ugly. J R Stat Soc Ser A Stat Soc 2005. 1681–27.
49. Spiegelhalter D J, Aylin P, Best N G. et al Commissioned analysis of surgical performance using routine data: lessons from the Bristol inquiry. J R Stat Soc Ser A Stat Soc 2002. 165191–231.
50. Walshe K, Shortell S. When things go wrong: how health care organisations deal with major failures. Health Aff 2004. 23103–111.
51. Bolsin S, Colson M. Making the case for personal professional monitoring in health care. Int J Qual Health Care 2003. 151–2.
52. Bolsin S, Solly R, Patrick A. The value of personal professional monitoring performance data and open disclosure policies in anaesthetic practice: a case report. Qual Saf Health Care 2003. 12295–297.