La Diabetes Mellitus (DM) es la enfermedad endócrino- metabólica más frecuente y su prevalencia va en aumento. Está caracterizada por una alteración en el metabolismo de los hidratos de carbono, principalmente, así como de los lípidos y proteínas, a causa de un déficit absoluto o relativo de insulina. Hay dos tipos de Diabetes Mellitus (DM): DM tipo 1 y DM tipo 2, siendo esta última mucho más frecuente que la primera. Durante el transcurso de la evolución pueden producirse complicaciones, que pueden ser agudas o crónicas.
Complicaciones de la Diabetes Mellitus: inicialmente silenciosa, potencialmente peligrosa.
Autor
Musciatti, Mariana Cecilia. Médica del Servicio de Guardia y Urgencias del Sanatorio Carlos MIner, Zárate, Prov. De Bs. As.
Palabras Clave: Diabetes mellitus – Diabetes Mellitus (DM) tipo 1 – DM tipo 2 – hiperglucemia crónica - metabolismo de hidratos de carbono- Glucemia de ayunas alterada- GAAI- TOG - intolerancia a la glucosa- insulina – glucagón - complicaciones agudas- complicaciones crónicas- hipoglucemia – cetoacidosis diabética – CAD- Estado hiperosmolar hiperglucémico no cetósico – EHHNC - Retinopatía diabética– maculopatía diabética – nefropatía diabética – microalbuminuria – neuropatía diabética – polineuropatía diabética - gastroparesia – pie diabético -
Key Words: Diabetes mellitus – type 1 diabetes- type 2 diabetes – chronic hyperglycemia – carbohydrate metabolism- - GAAI- TOG – glucose intolerance- insulin – glucagon – acute complications- chronic complications- hypoglicemia – diabetic ketoacidosis – CAD- hyperosmolar hyperglycemic nonketotic state – EHHNC - diabetic Retinopathy– diabetic maculopathy– diabetic nefropathy – microalbuminuria – diabetic neuropathy – diabetic polineuropathy - gastroparesis – diabetic foot -
Resumen
La Diabetes Mellitus (DM) es la enfermedad endócrino- metabólica más frecuente y su prevalencia va en aumento. Está caracterizada por una alteración en el metabolismo de los hidratos de carbono, principalmente, así como de los lípidos y proteínas, a causa de un déficit absoluto o relativo de insulina. Hay dos tipos de Diabetes Mellitus (DM): DM tipo 1 y DM tipo 2, siendo esta última mucho más frecuente que la primera. Durante el transcurso de la evolución pueden producirse complicaciones, que pueden ser agudas o crónicas.
Las agudas pueden presentarse en cualquier momento de la evolución de la Diabetes Mellitus (DM), incluso como forma de debut. Las complicaciones crónicas se producen a largo plazo, cada una con un tiempo estimable de desarrollo según el tiempo de evolución de la enfermedad, muchas de ellas frecuentemente diagnosticadas en estadios avanzados, demostrándonos la relevancia de una intervención oportuna. En este trabajo se presenta el caso de un paciente con Diabetes Mellitus (DM) tipo 1 de larga data, con un inadecuado control metabólico, quien padeció casi todas las complicaciones posibles de la Diabetes Mellitus (DM), hecho que reproduce una clínica aproximada a la historia natural de la enfermedad.
Review
Diabetes Mellitus (DM) is the most common endocrine and metabolic disease and its prevalence is increasing. It is characterized, primarily, by an alteration in the metabolism of carbohydrates, as well as lipids and proteins, because of a relative or absolute deficiency of insulin. There are two types of DM: “type 1 DM” and “type 2 DM”, the second one being much more common than the first one. During the course of evolution, complications can occur, which may be acute or chronic. The sharpening can occur at any point of the DM evolution, even as a way to debut .Chronic complications occur in the long run, each one with an estimated time of development depending on the disease evolution. Many of them are frequently diagnosed in advanced stages, which show the relevance of a timely intervention. This paper presents the case of a patient with longstanding type 1 DM, with inadequate metabolic control, who suffered almost all the possible complications of DM, a fact that plays a clinic about the natural history of disease.
Introducción
La Diabetes Mellitus (DM) es la enfermedad endócrino- metabólica más frecuente y una de las principales causas de morbimortalidad en el mundo.
La verdadera prevalencia es difícil de determinar, se estima que en América Latina existe alrededor de 15 millones de personas con Diabetes Mellitus (DM), el porcentaje oscila entre 7 y 8% en zonas urbanas, mientras que en las zonas rurales es apenas del 1 al 2%. En España se estima que un 3,5- 4,5% de la población la padece.
Estas cifras van en aumento por varios motivos, fundamentalmente debido a los cambios del estilo de vida y al aumento de la esperanza de vida.
Se cree que un gran porcentaje de pacientes con Diabetes Mellitus (DM) presentan la enfermedad sin haber sido aún diagnosticados debido al carácter silente de la enfermedad.
Se caracteriza por un trastorno metabólico de etiopatogenia multifactorial y también se considera parte de un conjunto de otros trastornos, como el Síndrome Metabólico, con quien comparte muchas características.
El principal inconveniente radica en una alteración del metabolismo de hidratos de carbono, lo cual conduce a una hiperglucemia crónica, pero también existen alteraciones en el metabolismo lipídico y proteico. Las mismas surgen de un déficit relativo o absoluto de insulina.
Según la OMS (Organización Mundial de la Salud) y la ADA (Asociación Americana de Diabetología) la definen como:
- Glucemia en ayunas > 126 mg/dl en ≥2 determinaciones diferentes y espaciadas.
- Glucemia al azar ≥200 +
- Clínica cardinal: (4 “P”) Polifagia, Polidipsia, Poliuria y Pérdida de peso o
- Clínica de descompensación aguda: CAD (cetoacidosis diabética) o CHNC (coma hiperosmolar no cetósico)*
*ver más adelante.
También incluyen 2 nuevas categorías diagnósticas:
- Glucemia de ayunas alterada (GAA): 100- 125 mg/dl
- ITOG (intolerancia a la glucosa): glucemia a las 2 hs tras la prueba de sobrecarga oral de glucosa con 75 gr, entre 140- 199 mg/dl.
La ADA considera a estos estados como prediabetes, constituyendo un factor de riesgo para el desarrollo posterior de Diabetes Mellitus (DM) y Enfermedad Cardiovascular.
La prueba de sobrecarga oral de glucosa, es el test de screening de elección para la población general.
Se recomienda hacerla en:
- Todo paciente > de 45 años
- En < de 45 años con sobrepeso (IMC ≥25 Kg/m2) + un factor de riesgo para el desarrollo de Diabetes Mellitus (DM):
- Antecedentes familiares
- Antecedentes personales de: ITOG, GAA, Diabetes Mellitus (DM) gestacional, antecedentes de fetos macrosómicos
- Hipertensión arterial
- Aumento de Triglicéridos o disminución de HDL colesterol
- Síndrome de ovario poliquístico
- Antecedentes de enfermedad arterial
- Sedentarismo
Hay 2 tipos de Diabetes Mellitus (DM):
- Diabetes Mellitus (DM) tipo 1: 5- 10% del total → Se produce por déficit, habitualmente absoluto, de Insulina. Debido a la destrucción de las células beta del páncreas, de etiopatogenia multifactorial con un gran componente autoinmune implicado. Puede ser objetivable a través del dosaje de niveles muy bajos de péptido C tras el estímulo con glucagón.
- Diabetes Mellitus (DM) tipo 2: es la forma más frecuente, representando al 90 al 95% del total → Dada por resistencia a la Insulina y un déficit relativo, más que absoluto, de la misma.
El objetivo de este trabajo es centrarnos en las complicaciones posibles de la Diabetes Mellitus (DM), teniendo en cuenta que son un componente troncal en la historia de un paciente que presente esta patología, ya que ninguno de ellos, más allá del adecuado control y tratamiento, está exento de padecerlas. A continuación se mencionan las principales.
Hay complicaciones agudas y crónicas.
Las complicaciones agudas pueden presentarse en cualquier momento de la evolución de la Diabetes Mellitus (DM).
A menudo suele ser una forma de debut, sobre todo la cetoacidosis diabética (CAD) en Diabetes Mellitus (DM) tipo 1, más frecuente en niños. También puede darse en otras circunstancias, como por ejemplo, aquellas relacionadas al tratamiento (incumplimiento o exceso del tratamiento farmacológico y no farmacológico, efecto adverso de la droga, etc.) o relacionadas con cambios en los requerimientos de Insulina (Infecciones, diferentes tipos de stress, como quirúrgico o traumático, insuficiencia renal, etc.)
Las complicaciones crónicas, como su definición lo expresa, se producen a largo plazo, cada una con un tiempo estimable de desarrollo según el tiempo de evolución de la enfermedad.
Es fundamental tener en cuenta que dan signos y síntomas cuando ya el proceso de desarrollo está en marcha y muchas de ellas lo hacen en un estadio evolutivo avanzado, motivo que nos demuestra la relevancia que tiene la prevención de factores de riesgo implicados, destacando entre ellos el adecuado control metabólico, así como la detección temprana de la enfermedad y su tratamiento oportuno.
En este trabajo se presenta el caso de un paciente con Diabetes Mellitus (DM) de larga data, con un inadecuado control metabólico, debido, principalmente, al incumplimiento del tratamiento, así como de su seguimiento, quien padeció prácticamente casi todas las complicaciones posibles de la Diabetes Mellitus (DM), hecho que reproduce una clínica aproximada a la historia natural de la enfermedad.
Complicaciones de la Diabetes Mellitus (DM)
Complicaciones Agudas de la Diabetes Mellitus (DM)
Las principales complicaciones agudas de la Diabetes Mellitus (DM) son: la hipoglucemia, la cetoacidosis diabética y la descompensación hiperosmolar.
Hipoglucemia
→La hipoglucemia es frecuente, sobre todo en los pacientes con Diabetes Mellitus (DM) tipo 1 cuando se realiza un tratamiento intensivo para mantener los niveles glucémicos dentro de la normalidad.
→En los pacientes con Diabetes Mellitus (DM) tipo 2 es más frecuente en los que reciben sulfonilureas o se aplican insulina.
→ El aumento en la frecuencia de hipoglucemias puede indicar el comienzo o empeoramiento de una falla renal que tiende a prolongar la vida media de la insulina circulante.
Hay situaciones que aumentan el riesgo de hipoglucemia en la persona con Diabetes Mellitus (DM):
- Retrasar u omitir una comida
- Beber alcohol en exceso o sin ingerir alimentos simultáneamente
- Hacer ejercicio intenso sin haber ingerido una colación apropiada
- Equivocarse en la dosis del hipoglucemiante, como le puede ocurrir a personas de edad avanzada que olvidan si ya tomaron la medicación o que no ven bien la dosis de la insulina que están colocando en la jeringa, etc.
- Coexistencia de insuficiencia suprarrenal y/o déficit de la hormona de crecimiento (GH).
Fisiopatología
Existen dos mecanismos que se desencadenan cuando la glucemia es baja:
- Disminución de la liberación de insulina
- Aumento de las hormonas contrarreguladoras, principalmente el glucagón.
Las catecolaminas (adrenalina y noradrenalina) también intervienen en menor medida. El cortisol y GH no actúan de forma aguda, sino que intervienen en casos de hipoglucemia prolongada.
→ Los pacientes diabéticos están desprotegidos contra la hipoglucemia, ya que no hay posibilidad de reducir la cantidad de insulina una vez administrada.
→ Por otra parte, a medida que la diabetes avanza, se va alterando la respuesta contrarreguladora del glucagón y de las catecolaminas. Como los síntomas adrenérgicos iniciales de la hipoglucemia dependen de la liberación de catecolaminas, pueden producirse hipoglucemias inadvertidas al fracasar dicha respuesta.
Manifestaciones clínicas
Se dividen en dos grupos:
- Síntomas adrenérgicos: sudoración, nerviosismo, temblor, palidez, palpitaciones y sensación de hambre.
- Síntomas neuroglucopénicos: cefalea, disminución de la capacidad de concentración, trastornos de la conducta y el lenguaje, visión borrosa, confusión, pérdida de conocimiento o convulsiones. Se desarrollan cuando la hipoglucemia no es controlada por las hormonas contrarreguladoras o por la ingesta de hidratos de carbono. Si la hipoglucemia ocurre durante la noche, puede manifestarse como sudoración, pesadillas y cefalea matutina o bien ser asintomática.
Los pacientes con Diabetes Mellitus (DM) mal controlada pueden presentar síntomas de hipoglucemia en presencia de cifras de glucemia más alta que los individuos normales o los pacientes con Diabetes Mellitus (DM) bien controlados, puesto que el umbral de contrarregulación de la glucosa está elevado.
Tratamiento de la hipoglucemia
Este depende del estado de consciencia del paciente. Si está consciente deben administrarse hidratos de carbono de absorción rápida por vía oral (V.O.), en caso contrario, la administración se hará por vía parenteral.
Hay que tener en cuenta que la hipoglucemia producida por sulfonilureas puede ser muy prolongada. En esta situación, es necesaria la observación hospitalaria durante al menos 48 horas.
Vía oral: Administrar una sola dosis de azúcar simple que puede ser un vaso de gaseosa corriente, un vaso de agua con tres cucharadas de azúcar, o el equivalente a 20- 25 g de glucosa oral (otros líquidos azucarados, caramelos).
Después de haber recibido la dosis oral o parenteral de glucosa y siempre y cuando continúe consciente y se sienta en capacidad de ingerir alimentos, la persona debe ingerir una colación rica en carbohidratos.
Parenteral:
- Una ampolla subcutánea o intramuscular de 1 mg de glucagón o un bolo intravenoso de glucosa que contenga 25 gr. El mismo puede repetirse las veces que sea necesario para lograr el objetivo.
Hiperglucemia Severa
Las dos formas de presentación de la descompensación hiperglucémica severa son el estado hiperosmolar hiperglucémico no cetósico (EHHNC) y la cetoacidosis diabética (CAD). Las dos comparten características comunes y su manejo es muy similar.
Característicamente:
- La cetoacidosis diabética (CAD) suele ser una complicación de la Diabetes Mellitus (DM) tipo 1, aunque puede darse en un porcentaje bajo en la Diabetes Mellitus (DM) tipo 2.
- La descompensación hiperosmolar, que puede llegar al coma hiperosmolar, es una complicación característica de la diabetes tipo 2, aunque puede aparecer en diabéticos tipo 1 que se ponen insulina suficiente para evitar la cetosis, pero no para evitar la hiperglucemia.
Con frecuencia las descompensaciones agudas severas del paciente con diabetes son causadas por enfermedades intercurrentes, como las infecciones, cuyo diagnóstico y tratamiento deben ser oportunos y adecuados.
Cetoacidosis Diabética
Aunque su frecuencia ha descendido claramente en nuestro medio, la cetoacidosis diabética (CAD) constituye todavía una causa importante de morbilidad en pacientes diabéticos mal tratados o inadecuadamente instruidos.
La incidencia anual es de 3- 8 episodios/1.000 paciente, variando según las estadísticas.
Se desarrolla en varias fases y se caracteriza inicialmente por una producción aumentada de cuerpos cetónicos, con elevadas concentraciones plasmáticas de los ácidos acetoacético e hidroxibutírico.
Para poder definirla debe caracterizarse de:
- glucemia mayor de 300 mg/dl
- cuerpos cetónicos positivos en orina
- acidosis metabólica con anión gap elevado
- disminución del bicarbonato plasmático.
Fisiopatología
La causa última es la insulinopenia grave que origina.
El déficit de insulina es responsable del aumento de la gluconeogénesis y de la glucogenólisis, además de la disminución de la captación celular de glucosa, todo lo cual conduce a hiperglucemia. A ésta contribuye mucho más la producción hepática de glucosa (aumentada unas 3- 4 veces por encima del valor normal) que la disminución de la captación celular.
La hiperglucemia es responsable de glucosuria, la cual determina diuresis osmótica y pérdida de agua y electrólitos, sobre todo sodio, potasio, magnesio, cloro y fosfatos.
En cuanto al metabolismo graso, se produce un incremento en la lipólisis, que puede descontrolarse por el aumento de las hormonas contrainsulares, con liberación de glicerol y ácidos grasos. El glicerol es utilizado para la gluconeogénesis, de modo que contribuye al mantenimiento de la hiperglucemia, mientras que los ácidos grasos libres son convertidos en acil- CoA por betaoxidación en las mitocondrias. La gran cantidad de acil- CoA que se produce excede con mucho la capacidad oxidativa del ciclo de Krebs y, en consecuencia, el exceso pasa a formar cuerpos cetónicos, los cuales se acumulan en el plasma y se excretan por orina.
La situación descrita hasta ahora corresponde en realidad a la cetosis diabética, que no necesariamente evoluciona a la acidosis. De hecho, existen muchos pacientes crónicamente mal compensados que tienen una hiperglucemia constante y una producción aumentada de cuerpos cetónicos, que se traduce por una cetonuria persistente.
El organismo trata de contrarrestar tal situación neutralizando el exceso de hidrogeniones a través de los mecanismos buffers, respiratorios y renales encargados del equilibrio ácido base.
En esta situación de cetosis, cualquier factor que agrave el déficit de insulina o incremente sus demandas producirá el fracaso de los mecanismos mencionados, con acumulación progresiva de aniones y, en consecuencia, descensos del pH y acidosis. La situación se complicará todavía más cuando la diuresis osmótica no pueda ser compensada por la ingesta oral (vómitos, alteración de la conciencia, mal estado general, etc.), en cuyo caso aparecerá deshidratación de curso progresivo, reducción del volumen plasmático, caída de la presión arterial y posibilidad de shock, si no se detiene el proceso.
Etiología
El grave déficit de insulina se produce como consecuencia de que ésta no ha sido administrada en los días anteriores o lo ha sido en dosis insuficientes o bien porque las necesidades de insulina han aumentado de forma importante.
Principales factores implicados:
- Abandono de la insulina (o sustitución por hipoglucemiantes orales)
- Errores en la administración de insulina o el control de la diabetes
- Debut de diabetes juvenil (especialmente en niños)
- Infecciones
- Infarto de miocardio
- Accidente vascular cerebral
- Traumatismos graves
- Estrés psíquico
- Administración de fármacos como glucocorticoides, diazóxido, difenilhidantoína, carbonato de litio, tiazidas, etc.
Cuadro clínico
Es característico su inicio insidioso; el paciente refiere, desde unos días antes, un agravamiento de su clínica diabética, con aumento de la sed y de la emisión de orina y disminución del apetito. Esta anorexia relativa reviste importancia, ya que es la primera manifestación del paso de la hiperglucemia simple a la cetosis. Esta fase de latencia puede ser notablemente corta en niños y adolescentes, aunque siempre dura varias horas como mínimo.
Si no se detiene la evolución, el paciente pasa a la situación de cetoacidosis diabética (CAD).
En general está consciente o sólo ligeramente estuporoso, por lo que es inapropiada la calificación de coma diabético.
Menos de la quinta parte de los pacientes está propiamente en coma, siendo éstos los de mayor edad, los que llevan más tiempo de evolución y, sobre todo, los que tienen una hiperglucemia más acusada. El grado de coma no guarda, en cambio, relación con la acidosis, y no es excepcional asistir a pacientes jóvenes con cifras de pH muy bajas (de alrededor de 6,7- 6,8) que están conscientes.
Cuando se observan graves alteraciones de conciencia en pacientes que no cumplen las condiciones de edad avanzada o hiperosmolalidad, es prudente investigar otras causas del coma, como la ingesta de tóxicos o un accidente vascular cerebral.
El paciente cetoacidótico tiene el aspecto de enfermo grave. Hay dos signos clínicos que llaman la atención: la respiración de Kussmaul y la deshidratación. La respiración de Kussmaul es una taquibatipnea típica que se presenta cuando el pH es aproximadamente inferior a 7,20 o 7,10, de modo que constituye el signo clínico de que el paciente ha pasado de la situación de cetosis a la de cetoacidosis diabética (CAD). Se acompaña del clásico aliento a manzanas y, cuando es muy acusada, puede llegar a provocar intensa fatiga.
Si la acidosis es leve puede ser difícil apreciar la respiración de Kussmaul, y cuando el pH es muy bajo (6,9 o menos) puede desaparecer por afectación del centro bulbar, lo que representa un signo de peor pronóstico. En individuos jóvenes y con un aparato respiratorio normal, la hiperventilación es a menudo muy importante y puede compensar la acidosis durante muchas horas.
El grado de deshidratación es variable y se debe valorar por los signos extracelulares (hipotensión, taquicardia, signo del pliegue, etc.) e intracelulares (sed, hipotonía ocular, sequedad de mucosas, etc.). Los vómitos son frecuentes en su defecto el paciente puede referir distensión epigástrica.
Los vómitos agravan la deshidratación y la pérdida de electrólitos, especialmente de potasio y de cloro. El dolor abdominal es una característica muy frecuente y se debe a la propia acidosis metabólica. En individuos no diagnosticados previamente de diabetes, este dolor abdominal (que se acompaña de leucocitosis) ha llevado a algún enfermo al quirófano con la sospecha diagnóstica de abdomen agudo. Si en el curso del tratamiento la corrección metabólica no se acompaña de la desaparición del dolor y de la resistencia abdominal, deben plantearse de inmediato otras posibilidades diagnósticas (p. ej., trombosis mesentérica, dado que se encuentran aumentados los mecanismos procoagulantes y, por tanto, las complicaciones tromboembólicas no son infrecuentes). Debe recordarse también la posibilidad de que una cetoacidosis diabética (CAD) se acompañe de pancreatitis aguda.
La pancreatitis es presumiblemente química, es decir, secundaria a la grave hipertrigliceridemia que puede acompañar a la cetoacidosis diabética (CAD).
La hipotermia es frecuente, como consecuencia de la pérdida de calor por la vasodilatación periférica cutánea inducida por la acidosis. Esta hipotermia puede enmascarar procesos infecciosos y ser responsable de hipotensión, bradicardia y alteraciones del ritmo cardíaco. Si bien la apirexia no garantiza la ausencia de un proceso infeccioso, la temperatura superior a 37,5 °C es un dato que sugiere esta etiología, por lo que en estos casos, después de efectuar cultivos, puede plantearse la administración de antibióticos. En relación con la posibilidad de infecciones, debe recordarse que las alteraciones funcionales de los neutrófilos de pacientes diabéticos descompensados es un factor desencadenante.
Estado Hiperosmolar Hiperglucémico no Cetósico (EHHNC)
La deshidratación es el trastorno que predomina en este cuadro, además es característica la ausencia de cetosis. Si bien no se conoce el mecanismo exacto que protege a los diabéticos tipo 2 del desarrollo de cetoacidosis, parece ser que una cierta reserva insulínica actuaría a nivel hepático, impidiendo la génesis de la cetosis.
Se trata de individuos, principalmente de edad avanzada, que sufren una deshidratación acusada y tienen cifras de glucemia muy elevadas (superiores a 600 mg/dL [33,3 mmol/L]) y, a menudo, hipernatremia.
El estado hiperosmolar hiperglucémico no cetósico (EHHNC) es menos frecuente que la cetoacidosis diabética (CAD), aunque en muchos países la proporción tiende a invertirse debido a la mejora en la prevención de la cetoacidosis diabética (CAD) y al envejecimiento general de la población.
El estado hiperosmolar hiperglucémico no cetósico (EHHNC) se define metabólicamente por:
- Ausencia de acidosis
- Osmolalidad plasmática efectiva (OPE) superior a 320 mosm/L o una osmolalidad plasmática total (OPT) superior a 340 mosm/L.
En condiciones normales, la OPT es de 300 mosm/L y la OPE de 285 mosm/L.
Fisiopatología
La hiperglucemia sin acidosis se puede producir por varios mecanismos:
- Presencia de secreción residual de insulina endógena con insulinemia periférica, que es capaz de impedir la lipólisis pero no la hiperglucemia
- Concentraciones de insulina adecuadas en la circulación hepática pero insuficientes en la periférica, con lo que la lipólisis aumentada deriva hacia gluconeogénesis y no hacia cetogénesis
- La deshidratación y la hiperosmolalidad per se impiden la lipólisis.
Etiología
Los factores desencadenantes del estado hiperosmolar hiperglucémico no cetósico (EHHNC) son similares a los mencionados en la cetoacidosis diabética (CAD), con la diferencia de que la etiología infecciosa es más frecuente, pueden intervenir algunos fármacos como glucocorticoides, tiazídicos, bloqueadores beta, cimetidina, clorpromazina, difenilhidantoína, inmunodepresores, diazóxido o furosemida, y a menudo se desconoce la existencia de una diabetes previa.
Manifestaciones clínicas
El inicio de las manifestaciones clínicas suele ser aún más insidioso, con incremento gradual de la obnubilación, alucinaciones, hemianopsias, afasias, nistagmo, alteraciones sensoriales, convulsiones y hemiplejías hasta llegar al coma. La afectación de la conciencia es mucho más grave que en la cetoacidosis diabética (CAD) y, a diferencia de ésta, más del 80% de los pacientes están realmente en coma y el resto presenta grados variables de obnubilación.
La deshidratación es aún más importante que en la cetoacidosis diabética (CAD) y se halla agravada por la disminución de la sensibilidad de los centros de la sed que presentan a veces las personas de edad avanzada.
Los hallazgos de laboratorio más característicos son la intensa hiperglucemia, la ausencia de acidosis franca (muy a menudo se observa cetonuria débil y, en ocasiones, disminuciones moderadas del pH) y el aumento de la cifra de urea, que traduce la gravedad de la deshidratación.
La potasemia puede estar disminuida, si bien el déficit de potasio no suele ser tan importante como en la cetoacidosis diabética (CAD). La natremia está elevada, aunque en ocasiones puede aparecer normal o incluso disminuida como consecuencia de que la hiperglucemia produce una redistribución de líquidos desde el espacio intracelular al extracelular (seudohiponatremia).
Principales diferencias entre estado hiperosmolar hiperglucémico no cetósico (EHHNC) y cetoacidosis diabética (CAD).
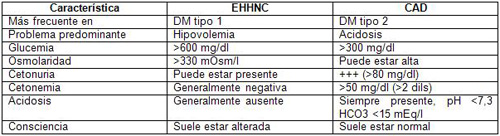
Manejo del estado hiperosmolar hiperglucémico no cetósico (EHHNC) y la cetoacidosis diabética (CAD)
Se debe tratar en un medio hospitalario y es recomendable contar con un glucómetro con tirillas reactivas.
1. Manejo inmediato (primeras dos a tres horas)
• Hidratación: la reposición debe hacerse en lo posible con solución salina normal (SSN 0.9%). Cuando la glucemia descienda a 250- 300, rotar a glucosado al 5%.
El paciente requiere 1 a 1.5 litros en la primera hora y otro tanto en las siguientes dos horas. La velocidad del goteo depende del grado de hipovolemia y requiere un monitoreo muy cuidadoso si el paciente presenta alguna evidencia de falla cardíaca o renal. En el estado hiperosmolar hiperglucémico no cetósico (EHHNC) la reposición de la volemia es crucial y debe ser vigorosa.
• Insulina: se administra en infusión continua a razón de 0.1 U/kg/hora.
Debido a la resistencia a la insulina generada por la cetoacidosis, el paciente con cetoacidosis diabética (CAD) suele requerir un bolo IV inicial de 0.4 U/kg que se repite a la hora si la glucemia no ha descendido al menos un 10%.
• Potasio: se inicia una vez que se haya demostrado diuresis y cuando la acidosis esté parcialmente corregida. Se recomienda no administrar más de 40 mEq/hora.
• Bicarbonato: su empleo es controvertido pero tiende a ser favorable cuando el pH es menor de 7.0 y la vida del paciente está en peligro. Generalmente basta con una infusión de 1 a 2 mEq/kg en la primera hora o hasta que el pH se eleve a 7.0 o 7.1. Cuando se administra bicarbonato se debe iniciar al mismo tiempo la reposición de potasio.
• Monitoreo de glucemia: debe hacerse cada hora con glucómetro que permita conocer el resultado inmediato para hacer las modificaciones del caso.
Se considera que el paciente ha superado la fase aguda cuando el pH es mayor de 7.3 y/o la osmolaridad es menor de 330 mOsm/l. Para entonces no debe haber signos de hipovolemia y la glucemia debe estar igual o menor a 250 mg/dl.
2. Tratamiento ulterior
• Hidratación: en lo posible la hidratación debe continuarse por vía oral con agua ad libitum.
Si el paciente no tolera aún la vía oral, se puede continuar la hidratación con soluciones como dextrosa en agua destilada (DAD) o en solución salina (DSS) al 5% y una infusión de insulina cristalina a razón de 0.2 U por gramo de dextrosa.
• Nutrición: se debe iniciar la vía oral tan pronto la tolere el paciente, con pequeñas porciones de carbohidratos fraccionadas en el día.
• Insulina: una vez restablecida la vía oral, se puede iniciar insulina cristalina subcutánea a razón de 5 a 10 unidades antes de cada comida principal que se pueden ajustar con base en el valor de glucemia al momento de la aplicación.
3. Complicaciones
• Hipoglucemia: se previene iniciando oportunamente la reposición de calorías. Se recomienda comenzar infusión de dextrosa (DAD o DSS al 5%) cuando la glucemia ha descendido a 250 mg/dl.
• Edema cerebral: se previene evitando al inicio soluciones hipotónicas como la solución salina al medio normal. Estas sólo se recomiendan cuando la hiperosmolaridad es muy severa y sostenida (osmolaridades por encima de 360 mOsm/l).
• Hipokalemia: se previene administrando potasio oportunamente.
• Acidosis hiperclorémica: se previene evitando el exceso de solución salina. Por ello se prefiere la hidratación por vía oral tan pronto sea posible.
• Trombosis venosa: se previene con adecuada hidratación, movilización temprana y profilaxis con heparinas de bajo peso molecular.
EL PRONÓSTICO del estado hiperosmolar hiperglucémico no cetósico (EHHNC) es mucho más sombrío y su mortalidad oscila entre el 40 y el 70% en algunas series.
Complicaciones Crónicas de la Diabetes Mellitus (DM)*:
La patogenia de las complicaciones diabéticas no es bien conocida y probablemente la patogenia sea multifactorial.
Suelen presentarse:
Diabetes Mellitus (DM) tipo 1→ A los 15 – 20 años del diagnóstico
Diabetes Mellitus (DM) tipo 2→ Pueden estar presentes al momento del diagnóstico
Se pueden dividir en:
Complicaciones vasculares, que a su vez se subdividen en:
- Macroangiopáticas: (principalmente por aterosclerosis)
- Enfermedades Cardiovasculares (ECV)
- Enfermedad Arterial Periférica
- Microangiopáticas:
- Retinopatía
- Nefropatía
- Neuropatía periférica
- No vasculares:
- Neuropatía Autonómica
- Afecciones de la piel
*para cada complicación hay una serie de recomendaciones, ajustadas al sistema de Niveles de Evidencia Científica de la Medicina basada en la evidencia , cuyo sistema de nomenclatura utiliza números y letras según el nivel al cuál corresponde (remitirse al anexo).
Complicaciones Macroangiopáticas
Son la principal causa de muerte en el paciente con Diabetes Mellitus (DM).
- La aterosclerosis (ATC) en los pacientes Diabetes Mellitus (DM) se produce de manera más extensa y precoz que en la población general.
- La frecuencia de aparición en varones y mujeres se iguala.
- La sinergia entre la Hiperglucemia y otros factores de riesgo cardiovascular (Hipertensión arterial, dislipemias, obesidad, sedentarismo y tabaquismo), favorecen el desarrollo de aterosclerosis (ATC) acelerada, por lo cual se tiende a tomar medidas de control de dichos factores más estrictas que en el resto de la población.
- Además de los antes nombrados, en el paciente con Diabetes Mellitus (DM), existen otros factores de riesgo adicionales:
- Micro y macroalbuminuria
- Aumento de la Creatinina plasmática
- Alteración plaquetaria
- Disfunción endotelial y de la musculatura lisa vascular
La ECV (enfermedad cardiovascular) incluye:
- Coronariopatía: Angor, IAM (Infarto Agudo de Miocardio)
- Pueden ser indoloros (silentes) por la existencia concomitante de disfunción autonómica. Debe sospecharse un IAM, siempre que aparezcan síntomas repentinos de insuficiencia ventricular izquierda, incluso, como se ha mencionado, en ausencia de angor.
- Se asocian con más complicaciones que la población general.
- La mortalidad es más elevada.
- Tiene pero pronóstico a largo plazo con mayor frecuencia de reinfartos.
- ACV (Accidente Cerebrovascular):
- AIT (Accidente Isquémico transitorio)
- Ictus Isquémico establecido.
- Arteriopatía periférica:
- Tiene predilección por la vascularización del área entre rodilla y tobillo, Arterias Tibial y Peronea.
- Suele presentarse en forma de:
1. Claudicación intermitente, es el síntoma más frecuente.
2. Trastornos tróficos.
3. Lesiones que van desde úlcera a gangrena.
Recomendaciones para el Control de los Factores de Riesgo CV
Recomendaciones Generales
- Toda persona con diabetes debe llevar a cabo cambios terapéuticos en el estilo de vida (CTEV). Estos incluyen:
1. Una nutrición saludable con: reducción del consumo de grasa y aumento del consumo de pescado y vegetales. (AA/ALAD) Debe incluir: la modificación de grasas trans, aumento de ácidos grasos omega- 3, fibra, estanoles y esteroles vegetales. (A/ADA)
2. reducción del exceso de peso
3. incremento en la actividad física hasta lograr al menos 30 minutos de actividad moderada 3 a 5 veces por semana
4. racionalización del consumo de alcohol y abolición del tabaquismo.
5. Toda persona con Diabetes Mellitus (DM) debe procurar alcanzar y mantener las metas adecuadas de TA, de lípidos y de glucemia y HbA1c. (AA/ALAD)
6. Toda persona con diabetes y enfermedad coronaria o algún factor de riesgo cardiovascular adicional debe tomar AAS (acido acetilsalicílico) a una dosis que oscila entre 75 y 150 mg al día. (A/ALAD)
7. Toda persona con Diabetes Mellitus (DM) mayor de 55 años y con un factor de riesgo adicional como hipertensión arterial, microalbuminuria, dislipidemia o tabaquismo debe tomar un inhibidor de la enzima convertidora de angiotensina (IECA). (AA/ALAD)
8. El electrocardiograma debe formar parte del estudio inicial de toda persona con Diabetes Mellitus (DM) mayor de 30 años. (D/ALAD)
9. Toda persona con diabetes que haya presentado un evento coronario debe recibir un IECA especialmente en las primeras 24 horas. (AA/ALAD)
10. Toda persona con diabetes que haya tenido un infarto del miocardio debe recibir un betabloqueante mientras no tenga contraindicación. (B/ALAD)
11. Toda persona con Diabetes Mellitus (DM) durante las primeras doce horas de un infarto del miocardio debe recibir un trombolítico en tanto no exista contraindicación para ello. (B/ALAD)
12. En toda persona con Diabetes Mellitus (DM) que cursa con un infarto agudo del miocardio debe evitarse la metformina y las tiazolidinedionas (Contraindicación B)
13. Toda persona con diabetes mayor de 40 años, hombre o mujer, con uno o más factores de riesgo para enfermedad coronaria (incluyendo microalbuminuria, nefropatía clínica, enfermedad vascular periférica y neuropatía autonómica) debe ser sometida a una prueba de esfuerzo. (B/ALAD)
14. Toda persona con diabetes que presente síntomas típicos o atípicos de angina o signos posibles o probables de enfermedad coronaria debe ser investigada para enfermedad coronaria, preferiblemente con una prueba de esfuerzo. (B/ALAD)
15. La prueba de esfuerzo, si la primera fue normal, debe repetirse cada dos a cinco años según el caso. (C/ALAD)
16. En el caso de personas muy obesas o con limitaciones para realizar una prueba de esfuerzo adecuada, esta debe hacerse con medicina nuclear (centellografía) o con un eco estrés (farmacológico). (D/ALAD)
17. Toda persona con diabetes y enfermedad coronaria debe ser valorado por un servicio de cardiología para definir el grado de compromiso de sus arterias coronarias y el tratamiento a seguir. (D/ALAD)
18. Toda persona con diabetes y enfermedad coronaria debe recibir una estatina. (AA/ALAD)
19. Toda persona con Diabetes Mellitus (DM) que cursa coninfarto agudo del miocardio debe mantener un control estricto de su glucemia para alcanzar niveles cercanos al rango normal. Esto se logra de manera más efectiva y segura con infusión continua de insulina y dextrosa y monitoreo frecuente de la glucemia capilar. (A/ALAD)
20. Las personas con diabetes y con síndrome coronario agudo se benefician con procedimientos como la angioplastia con stents a pesar de tener un peor pronóstico que las personas sin diabetes. Los stents medicados han disminuido la recidiva de oclusión también en personas con diabetes. (B/ALAD)
21. Las personas con diabetes y con síndrome coronario agudo se benefician con procedimientos como la revascularización con puentes coronarios. (B/ALAD)
22. Toda persona con diabetes y enfermedad coronaria en el post- infarto debe participar activamente en un programa de rehabilitación cardíaca. (D/ALAD)
Hipertensión Arterial (HTA)
La Hipertensión Arterial (HTA) afecta a un 20% de la población general, pero compromete hasta el 50% de las personas con Diabetes Mellitus (DM) tipo 2.
La Hipertensión Arterial (HTA) forma parte del Síndrome Metabólico y puede presentarse antes de que la Diabetes Mellitus (DM) sea diagnosticada y aún en grados menores de glucemia, por lo cual alrededor de una tercera parte de las personas Diabetes Mellitus (DM) tipo 2 recién diagnosticada ya tienen Hipertensión Arterial (HTA).
La coexistencia de Hipertensión Arterial (HTA) y Diabetes Mellitus (DM) multiplica de manera exponencial el riesgo de morbilidad y mortalidad por problemas relacionados con macroangiopatía y microangiopatía.
Estudios observacionales y análisis epidemiológicos de ensayos clínicos demuestran que la PAS (presión arterial sistólica) ES UN MEJOR PREDICTOR DE RIESGO CARDIOVASCULAR QUE LA PAD (presión arterial diastólica), y por ello se incluye en la mayoría de los modelos predictivos como el de Framingham y el del UKPDS.
En éste último, un incremento de 10 mmHg en la PAS en una persona con DM2 puede elevar el riesgo de enfermedad coronaria a 10 años desde un 0.5 hasta casi un 2%, dependiendo del resto de factores de riesgo.
El UKPDS también sugiere que la relación es bastante lineal hasta niveles de PAS aún por debajo de 100 mmHg. No hay hasta el momento estudios que hayan logrado mantener la presión sistólica (PAS) por debajo de 135 mmHg y demostrar su beneficio, pero la mayoría de las guías de manejo de Diabetes Mellitus (DM) tipo 2, proponen que toda persona con DM2 procure mantener una PAS por debajo de 130 mmHg. Con relación a la PAD (presión arterial diastólica), existen ensayos clínicos aleatorizados que demuestran el beneficio de bajar ésta a 80 mmHg o menos en personas con Diabetes Mellitus (DM) tipo 2 (evidencia nivel 1/ALAD).
La medición ambulatoria continua de la presión arterial se está utilizando con mayor frecuencia para evaluar las variaciones circadianas y evitar el fenómeno de "bata blanca", y se ha propuesto que en su utilización para el diagnóstico de Hipertensión Arterial (HTA) se reste 10 mmHg a la PAS y 5 mmHg a la PAD (presión arterial diastólica).
Recomendaciones
- A toda persona con diabetes se le debe medir la presión arterial cada vez que asista a consulta médica, o al menos una vez por año si no se encuentra elevada. (D/ALAD)
- Aquel paciente con una primera determinación de la TA ≥ 130/80 debe someterse a una segunda determinación en un día diferente, un nuevo resultado de TA ≥ 130/90, confirma el diagnóstico de Hipertensión Arterial (HTA). (C/ADA)
- El JNC VII (séptimo consenso del Joint National Comité) establece el diagnóstico de hipertensión arterial (HTA) cuando la presión sistólica (PAS) es ≥ 140 mmHg y/o la presión arterial diastólica (PAD) es ≥90 mmHg. Mientras que la ADA toma como parámetros las cifras de TA ≥ a 130/80 (C/ADA). Sin embargo ambos coinciden en que una persona con diabetes debe mantener la PAS por debajo de 130 mmHg (C/ADA) y la PAD (presión arterial diastólica) por debajo de 80 mmHg (B/ADA), cifras que el VII JNC (Joint National Comité) incluye dentro del rango de pre- hipertensión. Además basándose en las demás manifestaciones clínica y en la respuesta al tratamiento, cifras mayores o menores de TA pueden ser requeridas. (B/ADA)
- Se debe investigar una causa de hipertensión secundaria en pacientes que la desarrollan tempranamente, que demuestran un difícil control de la misma o que tienen paroxismos, que deterioran la función renal de manera acelerada y/o que tienen hiperkalemia (D/ALAD).
- Se debe iniciar tratamiento, en toda persona con Diabetes Mellitus (DM) tipo 2 que tenga una presión sistólica (PAS) ≥ 130 mmHg (D/ALAD) y/o una PAD (presión arterial diastólica) ≥ 80 mmHg. (A/ALAD) El tratamiento puede consistir inicialmente en CTEV si la persona todavía no tiene presión sistólica (PAS) ≥ 140 mmHg y/o PAD (presión arterial diastólica) ≥ 90 mmHg. Además de las recomendaciones generales para la persona con Diabetes Mellitus (DM) con o sin sobrepeso, estos CTEV incluyen restricción del alcohol, restricción de la sal a menos de 3 g por día y educación sobre la importancia de la adherencia al tratamiento y el automonitoreo frecuente de la presión arterial. (D/ALAD)
- Si no se logra alcanzar la meta de presión sistólica (PAS) y PAD (presión arterial diastólica) en un plazo máximo de 3 meses, o si la persona tiene inicialmente presión sistólica (PAS) ≥ 140 mmHg y/o PAD ≥ 90 mmHg, se recomienda adicionar un fármaco antihipertensivo. (A/ALAD)
- Si no se logra alcanzar la meta de presión sistólica (PAS) y PAD (presión arterial diastólica) en un plazo máximo de 3 meses con monoterapia antihipertensiva, o si la persona tiene inicialmente una presión sistólica (PAS) ≥ 160 mmHg y/o PAD (presión arterial diastólica) ≥ 110 mmHg, se recomienda utilizar terapia combinada adicionando un segundo fármaco antihipertensivo. (A/ALAD)
- Las terapias combinadas con varios fármacos generalmente son necesarias para alcanzar el objetivo control de TA. (B/ADA)
- Para iniciar el tratamiento farmacológico en una persona con DM2 se prefieren los fármacos que actúan directamente sobre el sistema renina- angiotensina como los inhibidores de la enzima convertidora de angiotensina (IECA) y los antagonistas del receptor de angiotensina (ARA). (AA/ALAD) Su ventaja es aún mayor en personas que tienen microalbuminuria. (A/ALAD) Sin embargo, la ventaja de estos fármacos se pierde si no se logra alcanzar las metas de presión arterial.
- El fármaco de elección para combinar con un IECA o un ARA es un diurético tiazídico en dosis bajas equivalentes a 12.5 mg (máximo 25 mg) de hidroclorotiazida (A/ALAD) o, en segundo lugar, un bloqueador de canales de calcio (BCC) preferiblemente no dihidropiridínico. (AA/ALAD)
- Si existen comorbilidades, debe hacerse la selección del primer o segundo medicamento que sea específico para esa condición. . (B/ALAD)
- En pacientes embarazadas con Diabetes Mellitus (DM) e Hipertensión Arterial (HTA) crónica se recomienda como meta objetivo presión sistólica (PAS) 110- 129 y PAD (presión arterial diastólica) 65- 80, cómo medida de prevención y cuidado de salud materna a largo plazo, así como para controlar un factor de riesgo de RCIU (retardo de crecimiento intrauterino). (E/ADA)
- Todas las clases de medicamentos antihipertensivos son efectivas para bajar la presión arterial en personas con Diabetes Mellitus (DM) (evidencia nivel 1/ALAD).
- El tratamiento intensivo de la presión arterial es superior al tratamiento convencional para prevenir eventos cardiovasculares, pero no se encontró que ninguna de las clases de fármacos fuera significativamente más efectiva (comparando IECA, ARA, BCC, diurético y betabloqueador) (evidencia nivel 1/ALAD).
- Sin embargo, los IECA y los ARA son más efectivos que otros antihipertensivos para prevenir el desarrollo de microalbuminuria y la progresión a macroalbuminuria y falla renal terminal (evidencia nivel 1/ALAD).
- Las metas de control de la PA pueden ser más estrictas (presión arterial menor de 125/75 mmHg) en aquellas personas con nefropatía diabética (con proteinuria o reducción de la tasa de filtración glomerular) por actuar ésta como un multiplicador del riesgo cardiovascular, o menos estrictas en personas con problemas vasculares cerebrales y en el adulto mayor por el riesgo de eventos isquémicos cerebrales. (D/ADA)
- Debe tenerse particular cuidado en la reducción de la presión arterial en personas con riesgo de sufrir hipotensión ortostática (D/ADA)
- Para lograr un control óptimo de la presión arterial podría recomendarse la evaluación con monitorización ambulatoria de presión arterial. (D/ADA)
Recomendación para la Medición Estándar de la Presión Arterial
- Los equipos de medición de presión arterial (esfigmomanómetros), incluyendo los que tienen las personas en la casa, ya sean estos de mercurio, aneroide o electrónicos, deben ser regularmente inspeccionados y calibrados.
- Quienes operen los esfigmomanómetros deben ser entrenados, y regularmente re- entrenados, en la técnica estandarizada de la medición de la presión arterial.
- El individuo no puede consumir bebidas que contengan cafeína, ni hacer ejercicio ni fumar por al menos 30 minutos antes de la medición de la presión.
- Previo a la medición, el individuo debe estar en reposo por al menos 5 minutos, preferiblemente sentado en una silla y no en la camilla de examen, con los pies en el piso y el brazo soportado sobre una mesa para que el brazalete quede al mismo nivel del corazón.
- Debe utilizarse un brazalete de tamaño apropiado al individuo en donde la vejiga inflable cubra al menos 80% de la circunferencia del brazo.
- Para determinaciones manuales, el brazalete debe inflarse 20 a 30 mmHg por encima del nivel en que se oblitera la arteria radial (se deja de sentir el pulso radial) y desinflarlo lentamente a una rata de 2 mmHg por segundo.
- La presión arterial sistólica es el punto en el que se escucha el primero de dos o más sonidos de Korotkoff (inicio de la fase 1) y la presión arterial diastólica es el punto en que desaparecen los sonidos de Korotkoff (inicio de la fase 5). No se deben hacer aproximaciones.
- Se deben realizar al menos dos determinaciones y registrarse el promedio de las mismas.
- Periódicamente debe medirse la presión arterial mientras el individuo está en posición de pie (debe estar de pie por al menos 2 minutos) especialmente en aquellos en riesgo de hipotensión arterial, previo al inicio o a la adición de otro medicamento antihipertensivo, y en aquellos quienes reportan síntomas consistentes con baja de la presión arterial al ponerse de pie.
Dislipidemias
La dislipidemia de la persona con Diabetes Mellitus (DM) se caracteriza por:
- Hipertrigliceridemia
- CHDL bajo
- CLDL dentro del rango considerado como normal pero con predominio de partículas de LDL pequeñas y densas que se refleja en la elevación de los niveles séricos de apoproteína B y del colesterol no- HDL.
Los estudios de cohorte y los ensayos clínicos controlados vienen demostrando que el riesgo de enfermedad cardiovascular es directamente proporcional al grado de hipercolesterolemia y que el impacto de la hipercolesterolemia es aún mayor en personas con Diabetes Mellitus (DM) (Evidencia nivel 1/ MRFIT).
La relación del riesgo con el nivel de triglicéridos ha sido más difícil de establecer, aunque parece ser más evidente en personas con Diabetes Mellitus (DM).
Para la mayoría de los pacientes la prioridad, a menos que tenga una hipertrigliceridemia grave, es reducir el LDL, con una meta de niveles ≤ 100 mg/dl (2,60 mmol/l).
Recomendaciones
- Todas las personas con Diabetes Mellitus (DM) deben tratar de mantener el nivel de colesterol LDL (CLDL) lo más bajo posible y el nivel de colesterol HDL (CHDL) más alto posible. Así mismo deben tratar de mantener el nivel de triglicéridos más bajo posible. (D/ALAD)
- En la persona con Diabetes Mellitus (DM) y dislipidemia, los CTEV deben ajustarse para alcanzar y mantener el nivel de colesterol LDL más bajo posible y el nivel de colesterol HDL más alto posible, así como el nivel de triglicéridos más bajo posible. (D/ALAD)
- En personas con Diabetes Mellitus (DM) y síndrome coronario agudo se recomienda utilizar estatinas en dosis altas durante la fase aguda, procurando alcanzar una concentración de CLDL menor de 70 mg/dL (1.8 mmol/L) (Recomendación B).
- La terapia con estatinas está contraindicada en el embarazo. (E/ADA)
- En personas con Diabetes Mellitus (DM) sin enfermedad coronaria se recomienda el tratamiento permanente con estatinas cuando tengan un CLDL igual o mayor a 130 mg/dL (3. 4 mmol/L) con el fin de alcanzar y mantener un nivel de CLDL inferior a este y cercano a 100 mg/dL (2.6 mmol/L) (Recomendación C).
- En aquellas personas sin enfermedad coronaria pero con uno o más factores de riesgo coronario adicionales a la Diabetes Mellitus (DM) y/o con un riesgo de enfermedad coronaria estimado en más del 20% a 10 años, se recomienda el tratamiento con estatinas en forma permanente y en dosis suficiente para alcanzar y mantener una concentración de CLDL inferior a 100 mg/dL (2.6 mmol/L). (AA/ALAD)
- Para el cálculo del riesgo coronario en personas con diabetes y sin enfermedad coronaria se recomienda utilizar el modelo propuesto por el grupo de investigadores del UKPDS (UKPDS Risk Engine) u otros modelos similares basados en cohortes de personas con diabetes. (D/ALAD)
- Las personas con Diabetes Mellitus (DM) que tengan niveles de triglicéridos elevados (mayores de 150 mg/dl que equivale a 1.7 mmol/l) se benefician con CTEV que sean efectivos para bajar triglicéridos.
- Todas las personas que tengan niveles de triglicéridos superiores a 400 mg/dL (4.5 mmol/L) deben ser tratadas con un fibrato al menos en forma transitoria e independientemente del tratamiento con estatinas. (D/ALAD)En caso de intolerancia o contraindicación pueden tomar niacina de acción prolongada. (D/ALAD)
- Se podría recomendar un fibrato como tratamiento inicial en personas con Diabetes Mellitus (DM) y enfermedad coronaria que tengan un CLDL cercano a la meta pero con triglicéridos altos (mayores de 200 mg/dl - 2.3 mmol/L) y CHDL bajo. (D/ALAD)
- Debe tenerse precaución al utilizar la combinación de una estatina con un fibrato por el riesgo aumentado de presentar rabdomiolisis (Precaución). Este riesgo es mayor si el fibrato utilizado en combinación es gemfibrozil (Contraindicación B).
- Las personas con diabetes y con enfermedad vascular periférica o enfermedad vascular cerebral deben tomar estatinas en forma permanente y en dosis suficiente para alcanzar una concentración del CLDL inferior a 100 mg/dL (2.6 mmol/L). (C/ALAD)
- El ezetimibe se puede utilizar para potenciar el efecto de las estatinas en personas con Diabetes Mellitus (DM) y cuando se combina permite alcanzar la meta de CLDL con dosis más bajas de estatinas. (D/ALAD)
- La colestiramina se puede utilizar cuando hay intolerancia persistente a las estatinas o en combinación con ellas (Recomendación D). Debe tenerse en cuenta que puede elevar los niveles de triglicéridos séricos (Precaución).
- La niacina se puede utilizar para elevar el CHDL. Además reduce significativamente los triglicéridos y tiene un efecto modesto cobre el CLDL. (D/ALAD) Las presentaciones de acción prolongada evitan el riesgo de deteriorar el control glucémico.
- Los ácidos grasos omega 3 en altas dosis (3 gramos o más) se pueden utilizar para reducir los triglicéridos. (D/ALAD)
Complicaciones Oftalmológicas
El ojo del paciente con Diabetes Mellitus (DM) puede afectarse por diferentes procesos patológicos. Las manifestaciones a este nivel son numerosas y complejas, pudiendo afectar a cualquier parte del aparato visual. La estructura más frecuentemente implicada es la retina, pero otras estructuras como el segmento anterior del ojo (córnea, cristalino, iris) pueden verse afectadas, incluso algunas alteraciones visuales pueden tener origen en estructuras extra oculares, como es el caso de las neuropatías de los oculomotores, las neuritis del trigémino o del segundo par craneano. Así mismo, las infecciones oftalmológicas siempre deben ser una consideración prioritaria en el diabético.
Clasificación de las oftalmopatías:
1. Retinopatía
2. Cataratas
3. Glaucoma
4. Afecciones de la córnea
Causas de ceguera en el paciente con Diabetes Mellitus (DM):
Diabetes Mellitus (DM) tipo 1: → La retinopatía por Diabetes Mellitus (DM)
Diabetes tipo 2: → El edema macular
Retinopatía diabética
- Tiende a ser más grave y prevalente en los pacientes con glucemias elevadas y mal control.
- Es la principal causa de ceguera bilateral irreversible en pacientes entre 20 y 74 años de edad en los países occidentales.
Según la guía ALAD:
- El control óptimo de la glucemia y de la presión arterial han demostrado ser las medidas de la mayor utilidad tanto en la prevención primaria, como secundaria de la retinopatía diabética (evidencia nivel 1).
- El hábito tabáquico, la hipertensión arterial (principalmente la diastólica) y las dislipidemias son patologías asociadas frecuentes y que incrementan el riesgo de morbilidad ocular (evidencia nivel 1).
- Hasta el presente, ningún tratamiento farmacológico ha demostrado ser efectivo para prevenir o tratar la retinopatía diabética en humanos.
- La remisión oportuna al oftalmólogo permite determinar entre otras cosas el momento adecuado para iniciar fotocoagulación de la retina como medida de prevención terciaria (recomendación D).
Además de estos otros FACTORES DE RIESGO implicados en su génesis son:
- Hormonales: más frecuente en varones y después de la pubertad; el embarazo
- Genéticos: sobre todo portadores de HLA – DR4
- Nefropatía Diabetes Mellitus (DM) presente
Se consideran FACTORES PROTECTORES:
- Miopatía intensa
- Hipertensión ocular
Momento de aparición:
- Diabetes tipo 1: → A partir de los 10 años del diagnóstico.
A los 15 años de evolución: el 90% presenta alguna lesión, el 15% de ellas de tipo proliferativo.
- Diabetes tipo 2: → Al momento del diagnóstico el 30% de los pacientes ya presenta lesiones (lo que demuestra que la enfermedad lleva un tiempo de varios años de evolución, sin haber sido diagnosticada).
Su curso es generalmente progresivo, con algunas excepciones donde hay remisión espontánea.
Las lesiones se producen como consecuencia de trastornos en la microcirculación que ocasionan una pérdida de competencia de la barrera hematorretiniana (signo de lesión más precoz, aunque sólo detectable en la angiografía fluoresceínica).
Se produce engrosamiento de la membrana basal de los capilares, degeneración de los pedicelos, falta de perfusión, obstrucción, aumento de la permeabilidad y una pérdida del tono vascular con aparición de dilataciones aneurismáticas, que llevan a la aparición de exudados y hemorragias, con el tiempo la hipoxia retiniana, inducida por tales alteraciones, estimula, en el estadio final, la proliferación de nuevos vasos anómalos.
OFTALMOSCÓPICAMENTE se observan:
→ Debido a la pérdida del tono vascular.
• Microaneurismas
Primeras lesiones visibles en oftalmoscopia y las más típicas (la primera lesión detectable son los exudados pero sólo son visibles por angiografía fluoresceínica). A su nivel se produce exudación con edema y hemorragias.
→ Debido a la incompetencia de la barrera hematorretiniana.
• Exudados duros o lipídicos: Son un acúmulo de macrófagos cargados de lípidos y material proteico.
• Hemorragias retinianas. Son intrarretinianas, puntiformes o redondeadas.
• Edema macular. En los primeros estadios es reversible, pero con el tiempo aparecen cavitaciones, dando lugar al denominado edema macular quístico. El edema macular es la causa más frecuente de pérdida de visión en la retinopatía diabética.
→ Debido a la isquemia retiniana.
• Exudados algodonosos. Causados por microinfartos retinianos. Traducen isquemia retiniana.
• Neovasos. Típicos de las formas proliferativas. La isquemia retiniana extensa induce, mediante factores de crecimiento, la formación de nuevos vasos de estructura anormal y con crecimiento desordenado, sangrando en la propia retina o en el vítreo. Acompañando a estos vasos hay una proliferación de bandas de tejido fibroso, que pueden retraerse provocando un desprendimiento de retina. La neovascularización puede afectar también al iris (rubeosis de iris) y al ángulo iridocorneal, dando lugar a un glaucoma neovascular.
Según su evolución se clasifica en:
- Retinopatía simple, basal, de fondo o no proliferativa (RPNP)
En el Diabetes tipo 1:
→ AUSENTE (prácticamente) antes de los 5 años
→ PRESENTE en 50% a los 10 años, 90% a los 15 años y 100% a los 20 años.
Consta de: microaneurismas, hemorragias retinianas (puntiformes) y/o exudados.
- Retinopatía prepoliferativa (RPP)
Presencia de exudados algodonosos y zonas no perfundidas visibles mediante angiofluoresceinografía.
*Algunos autores no incluyen este estadio, interpretando estos cambios como retinopatía no proliferativa grave.
El exudado blanco y algodonoso es expresión de la oclusión (e isquemia) capilar reciente.
- Retinopatía proliferativa (RP): La determina la aparición de neovasos. Las bandas de tejido fibroso forman un citoesqueleto con contracción del vítreo, que luego generan, por tracción, desprendimiento la retina.
- Maculopatía: presencia de edema macular que puede no ser visible con la oftalmoscopia de rutina. Es una de las causas de pérdida rápida de agudeza visual.
La OMS define como etapas clínicas terminales la presencia de compromiso significativo de la agudeza visual, hemorragia vítrea, desprendimiento de retina y amaurosis.
Examen Oftalmológico Completo
Este comprende tres estudios básicos:
- Agudeza visual
IMPORTANTE: Siempre debe tenerse en cuenta que la hiperglucemia produce cambios reversibles en la refracción. Se debe evaluar la agudeza visual cuando el paciente esté compensado metabólicamente.
- Fondo de ojo con pupila dilatada
- Tonometría
El oftalmólogo determinará la necesidad de procedimientos diagnósticos o terapéuticos especiales como:
• Angiografía con fluoresceína
• Fotocoagulación
• Vitrectomía
• Criocoagulación
Recomendaciones (ADA Y ALAD):
- Optimizar el control de la glicemia para reducir el riesgo o disminución de la progresión. (A/ADA)
- Optimizar el control de la tensión arterial para reducir el riesgo o disminuir su progresión. (A/ADA)
- Niños mayores de 10 años y adultos Diabetes Mellitus (DM) tipo 1, deben realizar un control y examen oftalmológico inicial dentro de los 5 años del debut de la Diabetes Mellitus (DM). (B/ADA)
- Los pacientes con Diabetes Mellitus (DM) tipo 2 deben realizar este primer control lo más inmediatamente posible al diagnóstico de su patología. (B/ADA)
- Es conveniente que toda persona con DM2 sea examinada anualmente desde su diagnóstico aunque puede ser costo- efectivo un control cada dos años en personas de bajo riesgo. En pacientes con retinopatía en progreso será necesario controles más frecuentes. (B/ADA)
*La guía ALAD menciona que los exámenes iniciales pueden realizarse por un médico no especialista en oftalmoscopía pero ante la presencia de cualquier hallazgo sugestivo de retinopatía, la remisión al oftalmólogo es indispensable. (D/ALAD)
- Se puede hacer una fotografía de retina mediante una cámara no midriática o una oftalmoscopia a través de pupila dilatada. Ambos procedimientos deben ser realizados e interpretados por personas con entrenamiento específico. De todas maneras la ADA aclara que en ningún caso debe reemplazar al examen oftalmológico. (E)
- Mujeres con deseo gestacional o embarazadas deberían tener un examen ocular completo y asesorado sobre el riesgo de aparición y progresión de la retinopatía diabética. La evaluación debería realizarse en el primer trimestre, durante el embarazo y al año del parto. (B/ADA)
Tratamiento de la Retinopatía Diabetes Mellitus (DM)
- Ningún tratamiento farmacológico ha demostrado ser eficaz.
- Derivar rápidamente al oftalmólogo a pacientes con cualquier nivel de edema macular, RPNP grave, RPPP o algún signo de Retinopatía proliferativa (RP). (A/ADA)
- La panfotocoagulación con laser argón está indicada para reducir el riesgo de pérdida de la visión en pacientes con alto riesgo de Retinopatía proliferativa (RP), edema macular clínicamente significativo y para el tratamiento de algunos casos de Retinopatía proliferativa (RPNP) grave o Retinopatía prepoliferativa (RPP). (A/ADA) Tras una hemorragia vítrea, en primera instancia habría que esperar a que esta se reabsorba y luego indicar la panfotocoagulación, pero si esta no se resuelve completamente o el paciente sigue sangrando posteriormente, estaría indicada la vitrectomía. Esta última también podría ser útil en proliferaciones fibrovasculares y desprendimientos de retina traccionales en la Retinopatía proliferativa (RP).
* Dos grandes ensayos, the Diabetic Retinopathy Study (DRS) primero y luego Treatment Diabetic Retinopathy Study (ETDRS), afianzaron el beneficios de la terapia de fotocoagulación con láser.
- En cuanto al edema macular, existen varias opciones de tratamiento: fotocoagulación laser argón, que es el procedimiento de elección, sobre todo para casos de microaneurismas filtrantes, en caso de filtrado difuso se deben plantear otras posibilidades como la inyección de triamcinolona intravítrea (glucocorticoide de acción prolongada) y cómo último recurso, vitrectomía.
- La presencia de retinopatía no es contraindicación a la terapia cardioprotectora de aspirina, ya que esta terapia no aumentan el riesgo de hemorragia retiniana.(A/ADA)
Cataratas
Puede ser de tres tipos:
• Metabólica
• Senil: la más frecuente en Diabetes
• Secundaria
Las cataratas son más frecuentes en la población diabética, ocurren en edades más tempranas y progresan más rápidamente que en la población no diabética.
Glaucoma
Puede ser:
• Crónico, simple:
• Secundario: a proliferación de neovasos en la cámara anterior del iris, sobre superficie del iris (rubeosis iridis).
Son frágiles, producen aumento del contenido proteico del humor acuoso y sangrado en la cámara anterior del ojo. Provoca fuertes dolores, muchas veces el tratamiento es ineficaz y obliga a repetidas intervenciones.
La determinación de la presión intraocular debe ser de rutina en la persona con diabetes
Córnea
Aunque las lesiones de córnea NO son más frecuentes en el diabético, cuando tienen un origen infeccioso pueden ser más difíciles de tratar y requieren atención especial.
Complicaciones Renales
Nefropatía Diabética
La Diabetes Mellitus (DM) tipo 2 es la causa más frecuente de IRT en el mundo occidental (a pesar de que, comparando su incidencia solo entre pacientes con Diabetes Mellitus (DM), es más frecuente en Diabetes Mellitus (DM) tipo 1, el 90% de los diabéticos son tipo 2)
Diabetes Mellitus (DM) tipo 1→ La nefropatía clínica ocurre en el 30- 40% de los casos, siendo más frecuente si la enfermedad comenzó antes de los 20 años de edad.
Diabetes Mellitus (DM) tipo 2→ Su frecuencia varía entre el 10- 25%.
La PREVALENCIA aumenta cada año a partir de los 10 años de evolución de la enfermedad, hasta alcanzar un máximo alrededor de los 25 años de evolución.
Sus principales factores influyentes son el TIEMPO DE EVOLUCIÓN DE LA Diabetes Mellitus (DM) y sobre todo si durante este período NO SE CONTÓ CON UN BUEN CONTROL METABÓLICO.
En la Diabetes Mellitus (DM) 2 la progresión es más rápida, simplemente porque la enfermedad está más avanzada para cuando se diagnostica al paciente de Diabetes Mellitus (DM).
PACIENTE EN RIESGO →Aunque existen cambios precoces relacionados con la hiperglucemia, como la hiperfiltración glomerular, el riesgo de desarrollar una insuficiencia renal solamente se hace significativo cuando se empieza a detectar en la orina la presencia de MICROALBUMINURIA, definida como la excreción de albúmina entre 30 y 300 mg/24 h (20- 200 mg/mL).
Un 20- 40% de los pacientes con MICROALBUMINURIA progresa a nefropatía clínica y de éstos un 20% llega a insuficiencia renal terminal al cabo de 20 años.
Además la microalbuminuria se considera un factor de riesgo cardiovascular establecido. (ADA)
La nefropatía puede permanecer silente durante 10- 15 años antes de la instauración de la nefropatía diabética propiamente dicha, existiendo un largo período caracterizado por la presencia de microalbuminuria.
La primera manifestación de la nefropatía diabética es la proteinuria, que al principio puede ser intermitente. El tiempo medio desde el diagnóstico de la diabetes hasta la proteinuria es de 17 años, aunque es variable.
Una vez establecido el diagnóstico de nefropatía diabética clínica, la evolución hacia la insuficiencia renal es la regla, si bien la velocidad es variable.
La nefropatía diabética propiamente dicha se define por la presencia de PROTEINURIA PERSISTENTE, también denominada MACROALBUMINURIA (superior a 500 mg/24 h de proteínas totales o 300 mg/24 h de albúmina).
Para su diagnóstico es necesario que el paciente tenga además retinopatía, a la vez de descartar otra causa de pérdida de proteínas (insuficiencia cardíaca, infección urinaria, otra enfermedad renal, etc)
En cuanto a la ANATOMÍA PATOLÓGICA se distinguen las siguientes lesiones características:
- Glomeruloesclerosis difusa: la hipertensión e hiperfiltración glomerular provocan un engrosamiento de la MBG y la expansión del mesangio. Además, las proteínas filtradas son tóxicas para los túbulos, dañando su estructura.
- Glomeruloesclerosis nodular (lesión de Kimmelstiel- Wilson). Evolución de la esclerosis difusa caracterizada por la presencia de nódulos PAS+ por fuera del glomérulo. Clínicamente produce un síndrome nefrótico.
- Además se observan células de Armani- Ebstein, patognomónicas de la nefropatía diabética y que representan células del TCP y TCD llenas de glucógeno (PAS+), que indican el estado de hiperglucemia mantenido durante años.
Desde un punto de vista FISIOPATOLÓGICO se pueden considerar cuatro etapas en la historia natural de la enfermedad:
- Primera etapa → HIPERTENSIÓN E HIPERFILTRACIÓN GLOMERULAR:
Por aumento del flujo plasmático renal y de la presión hidrostática glomerular. Ocasiona microalbuminuria intermitente que aparece después del ejercicio físico.
- Segunda etapa → NEFROPATÍA DIABÉTICA INCIPIENTE: Se caracteriza porque el filtrado permanece elevado o se normaliza y la microalbuminuria se hace persistente.
- Tercera etapa → NEFROPATÍA CLÍNICA. Se caracteriza por macroalbuminemia y disminución del filtrado glomerular, pudiendo evolucionar hacia la insuficiencia renal terminal.
- Cuarta etapa → INSUFICIENCIA RENAL TERMINAL: disminución del filtrado glomerular: aclaramiento (clearance) o depuración de la creatinina (Cl Cr) por debajo de 25- 30 ml/min.
Las manifestaciones clínicas comienzan a producirse a partir de la segunda etapa de lesión fisiopatológica.
Estadios Clínicos
- Estadio I → NEFROPATÍA INCIPIENTE (TEMPRANA O SUBCLÍNICA): Aparece entre 10 y 15 años de evolución de la diabetes. Se caracteriza por microalbuminuria persistente en dos o más muestras tomadas durante un intervalo de tres meses.
(Se corresponde con la 2° etapa)
- Estadio II → NEFROPATÍA CLÍNICA: Aparece entre 15 y 20 años de evolución. Caracterizada por la presencia de macroalbuminuria o proteinuria persistente. Se considera una etapa por lo general irreversible que tiende a progresar a la insuficiencia renal crónica y puede también producir un síndrome nefrótico.
En esta etapa se suele detectar por primera vez la elevación de la tensión arterial, aunque en muchos pacientes la hipertensión arterial antecede a la nefropatía y de hecho se constituye en un factor de riesgo para ella. Esta etapa puede subdividirse en: leve a moderada cuando sólo hay proteinuria y severa cuando ya hay deterioro de la función renal determinada por un aclaramiento de creatinina (ClCr) inferior a 70 cc/min con elevación de la creatinina sérica.
- Estadio III: INSUFICIENCIA RENAL CRÓNICA AVANZADA: (Cl Cr menor de 25- 30 ml/min).
Se produce entre los 20 y 30 años de evolución de la diabetes. Se corresponde con la cuarta etapa de evolución fisiopatológica. A partir de este momento ya se empiezan a surgir alteraciones en el metabolismo del calcio y fósforo, la anemia, la insuficiencia cardíaca, etcétera.
- Estadio IV: FALLA RENAL TERMINAL: Se considera que el paciente ha alcanzado este estadio cuando el aclaramiento de creatinina (ClCr) es igual o inferior a 10 cc/min y/o la creatinina sérica igual o mayor a 3.4 mg/dl (300 mmol/l). En esta etapa ya el paciente requiere diálisis y eventualmente un trasplante de riñón ( aunque en la persona con diabetes se tiende a adoptar estas medidas en forma más temprana!)
La diálisis en el paciente con fallo renal a causa de enfermedad Diabetes Mellitus (DM) tiende a iniciarse con Filtrados Glomerulares (FG), cuya estimación se produce con el aclaramiento de creatinina (ClCr), menos deteriorados que en aquellos pacientes cuya causa de Insuficiencia renal es diferente a Diabetes Mellitus (DM), mientras que en los pacientes NO Diabetes Mellitus (DM) suele iniciarse con aclaramiento de creatinina (ClCr) < o iguales a 10, en el paciente con Diabetes Mellitus (DM) se comienza con aclaramiento de creatinina (ClCr) < o iguales a 15.
Estadios de Daño Renal Crónico (según el FGR*1)
1. Daño renal*2 con FGR (filtrado Glomerular) normal o incrementado→> o igual a 90
2. Daño renal*2 con un mínimo descenso del FGR (filtrado Glomerular) → 60 - 89
3. Moderado descenso del FGR (filtrado Glomerular) → 30 – 59
4. Severo descenso del FGR (filtrado Glomerular) → 15 – 29
Fallo renal, FGR (filtrado Glomerular) → < o igual a 15 o diálisis.
*1: expresado en ml/min por 1.73 m2 de superficie corporal.
*2: determinado por análisis bioquímico, imágenes o anatomía patológica.
Evaluación de la Nefropatía Diabética
Se basa en la medición de la microalbuminuria, de la proteinuria y de la filtración glomerular (ver algoritmo y recomendaciones).
Medir proteinuria en muestra aislada de orina (tirillas)
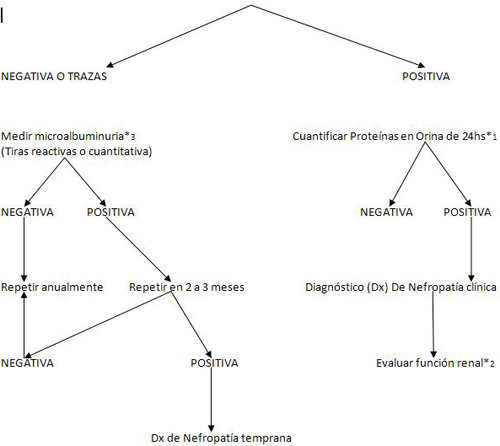
*1: Proteinuria significativa: igual o mayor a 0.5 gramos/24 horas.
*2: Para evaluar la función renal: la tasa de filtración glomerular se puede conocer midiendo el clerance de creatinina (ClCr), sin embargo la determinación del nivel de creatinina sérica constituye un buen índice en personas que no estén desnutridas ni muy añosas. La creatinina sérica suele elevarse cuando ya hay proteinuria positiva (etapa de nefropatía clínica), pero conviene medirla desde un comienzo. El aclaramiento de creatinina (ClCr) o la filtración glomerular isotópica se debe medir a partir del momento en que la creatinina sérica comience a elevarse.
*3: Para su detección inicial (pesquisaje), la microalbuminuria se puede medir utilizando un método semicuantitativo como tirilla o pastilla reactiva, pero siempre se debe confirmar por un método cuantitativo estandarizado (turbidimétrico o inmunoquímico) tomando una muestra de orina de 24 horas o una muestra de la primera orina de la mañana, en cuyo caso hay que medir también creatinuria y calcular un índice microalbuminuria/creatinuria. La prueba no debe realizarse en pacientes con infecciones del tracto urinario, descompensación metabólica, estado febril, insuficiencia cardíaca, coincidencia con la menstruación o que hayan tenido relaciones sexuales el día previo.
Recomendaciones (ADA Y ALAD):
- Optimizar el control de la glicemia para reducir el riesgo o disminución de la progresión. (A/ADA)
- Optimizar el control de la tensión arterial para reducir el riesgo o disminuir su progresión. (A/ADA)
- Comenzar con la pesquisa inicial (ver algoritmo) dentro de los primeros 5 años de diagnóstico en Diabetes Mellitus (DM) tipo 1 y en el momento del diagnóstico en Diabetes Mellitus (DM) tipo 2. (E/ADA)
- Realizar un dosaje de Creatinina plasmática (Cr P) al menos anualmente en todos los adultos con Diabetes Mellitus (DM) sin tener en cuenta el grado de excreción de Albúmina. (E/ADA)
- En el tratamiento del/la paciente no embarazada con micro o macroalbuminemia, IECA o ARA II deben ser utilizados. (A/ADA)
- Si bien no está totalmente establecido, hay recomendaciones avaladas por ensayo clínico que determinan:
- Pacientes con Diabetes Mellitus (DM) tipo 1, con Hipertensión arterial (HTA) y cualquier grado de albuminuria, los IECA han demostrado retrasar la progresión de la nefropatía. (A/ADA)
- En los pacientes Diabetes Mellitus (DM) tipo 2, Hipertensión arterial (HTA) y Microalbuminuria, tanto los IECA como los ARA han demostrado retrasar la progresión a macroalbuminuria. (A/ADA)
- En pacientes con Diabetes Mellitus (DM) tipo 2, Hipertensión arterial (HTA) y Macroalbuminuria e Insuficiencia renal (Cr sérica > 1,5 mg/dl), los ARA II han demostrado retrasar la progresión a nefropatía. (A/ARA)
- Si una clase de estos fármacos no se tolera debe cambiarse por el otro y viceversa. (E/ADA)
- La reducción del consumo de proteínas a 0,8 – 1 gr/kg de peso corporal/día en los individuos con Diabetes Mellitus (DM) y en las primeras etapas de enfermedad renal crónica (ERC), puede mejorar las medidas de función renal (tasa de excreción de albúmina en la orina, FGR (filtrado Glomerular), por lo cual se recomienda. (B/ADA)
- Cuando los IECA, ARA II o diuréticos se utilizan, se deben controlar los niveles de potasio y la concentración de Cr P, por el riesgo para el desarrollo de Insuficiencia Renal Aguda e Hiperpotasemia. (E/ADA)
- Se recomienda un seguimiento continuo de la excreción de albúmina en orina, así como la respuesta a la terapia. (E/ADA)
- Si el FGR es < o igual a 60 ml/min/1,73 m2 evaluar y actuar en efecto de las posibles complicaciones de la ERC. (E/ADA)
- Considerar la derivación a un médico especialista en patología renal cuando haya dudas acerca de la etiología de la enfermedad renal, difícil manejo o estadio avanzado. (B/ADA)
- La vacunación temprana contra la hepatitis B está indicada en pacientes con probabilidad de progresar a enfermedad renal en terminal.
Nefropatía no Diabética en la Persona con Diabetes Mellitus (DM)
- Se debe tener en cuenta que hasta un 10% de las nefropatías en personas con diabetes pueden ser de origen no diabético.
- Debe sospechar especialmente cuando no hay evidencia de retinopatía asociada en un paciente con nefropatía clínica.
- En paciente edad avanzada debe tenerse en cuenta la posibilidad de una estenosis de la arteria renal, en cuyo caso estarían contraindicados los IECA.
- En la nefropatía diabética son frecuentes la acidosis tubular renal (ATR) IV, la necrosis de papila y las infecciones urinarias.
Complicaciones Neurológicas
La neuropatía diabética es la complicación más frecuente y precoz de la diabetes, pero suele ser la más tardíamente diagnosticada.
Su prevalencia no está bien establecida, pero se estima que está presente en menos 10% de los pacientes AL COMIENZO de la Diabetes Mellitus (DM) y en un 50% en pacientes con MÁS DE 25 AÑOS DE EVOLUCIÓN de Diabetes Mellitus (DM).
Su frecuencia así como su evolución y gravedad se correlacionan con la duración de la enfermedad y el mal control metabólico.
Histopatológicamente, las lesiones más comunes son degeneración y pérdida de axones, la desmielinización segmentaria, cambios en las células de Schwann, en las células perineurales y en los vasos endoneurales, alteraciones en los nódulos de Ranvier, atrofia axonal distal y, en las formas crónicas, regeneración en forma de brotes.
Se clasifican en dos tipos: polineuropatías simétricas y asimétricas, aunque lo habitual es que los pacientes presenten manifestaciones clínicas de ambas.
Polineuropatías Simétricas
- Son las más frecuentes
- Es la forma más común en el paciente con mal control metabólico
Polineuropatía Sensitiva Distal:
Es la polineuropatía diabética más frecuente. La clínica dominante depende del tipo predominante de afectación de fibra nerviosa:
- Fibras gruesas → PARESTESIAS E HIPOESTESIA EN GUANTE Y CALCETÍN. Con arreflexia y pérdida de la sensibilidad vibratoria. La pérdida de sensibilidad es responsable de las úlceras neuropáticas que se presentan en los puntos de apoyo del pie (mal perforante plantar), así como de la artropatía neuropática (articulación de Charcot), que afecta preferentemente las articulaciones de los dedos de los pies y, con menos frecuencia, las rodillas y caderas.
- Fibras finas → DOLOR URENTE sobre todo en los PIES, en ocasiones muy intenso, predomina por la noche y se acompaña de hiperestesia, hasta el punto de que el paciente no tolera el roce de las sábanas o el pijama.
Neuropatía Autonómica
Es una alteración frecuente. La afectación aislada del sistema vegetativo es rara y suele acompañarse de manifestaciones de neuropatía sensitiva.
Suele haber afectación de:
- Sistema cardiovascular → HIPOTENSIÓN ORTOSTÁTICA, TAQUICARDIA EN REPOSO.
La hipotensión ortostática ocurre por fracaso de los barorreceptores controlados por el sistema vegetativo; en ocasiones puede ser muy grave y provocar síncopes. Para valorar el grado de afectación cardiocirculatoria, se utilizan las maniobras de Valsalva y la bipedestación, con el objeto de evaluar la respuesta de la frecuencia cardíaca y la tensión arterial, encontrándose, por ejemplo, la respuesta fisiológica habitual de aumento de la frecuencia cardíaca ante Valsalva, abolida.
- Sistema genitourinario → VEJIGA NEURÓGENA, DISFUNCIÓN ERÉCTIL Y EYACULACIÓN RETRÓGRADA.
La disfunción eréctil ocurre con relativa frecuencia en diabéticos de larga evolución y parece estar relacionada con factores vasculares y neuropáticos (afectación simpática del plexo sacro). La eyaculación retrógrada, también frecuente, se produce como consecuencia de una disfunción vegetativa del esfínter vesical. La vejiga neurógena consiste en la incapacidad de ésta, cuando se distiende, de emitir estímulos sensoriales a la corteza. En consecuencia, se producen grandes dilataciones de la vejiga con emisión de más de 1.000 mL de orina en una sola micción, lo que representa un riesgo adicional de infección urinaria.
- Sistema gastrointestinal → DISFUNCIÓN MOTORA ESOFÁGICA, GASTROPARESIA Y ENTEROPATÍA DIABÉTICA.
La gastroparesia diabética es una dilatación átona del estómago que puede ser responsable de náuseas, vómitos, digestiones “pesadas” o simplemente mal sabor de boca al levantarse por la mañana, aunque a menudo es asintomática. La enteropatía diabética se produce por afectación predominante del plexo de Auerbach y consiste en diarreas líquidas, predominantemente nocturnas, que pueden acompañarse de incontinencia fecal.
- Otros síntomas → SUDORACIÓN PROFUSA.
Se caracterizan por crisis de diaforesis profusa, en particular después de comer, que se localiza exclusivamente en la cara y la zona supraumbilical del tronco.
1. Plexopatía o Amiotrofia Diabética: (o Síndrome de Garland)
Aparece en Diabetes Mellitus (DM) de larga evolución y se caracteriza por dolor muy intenso en región lumbar y glútea, seguido de debilidad progresiva de cuádriceps y psoas. También puede haber atrofia muscular y fasciculaciones.
El cuadro se desencadena a veces coincidiendo con mejorías importantes en el control metabólico (p. ej., después de iniciar el tratamiento con insulina en la DMNID). Tiende a resolverse espontáneamente en 6- 12 meses, aunque puede recidivar.
Polineuropatías Asimétricas
- Son menos frecuentes
- Se dan principalmente en ancianos
- Generalmente de aparición más temprana, respecto a las simétricas, en el curso evolutivo de la Diabetes Mellitus (DM).
1. Mononeuropatía De Nervio Craneano
Se afectan principalmente los Pares Craneales, de los cuales el más frecuentemente implicado es el III Par. Dicha afección se asocia a intenso dolor retroorbitario, de comienzo brusco y a diferencia de los III pares de causa compresiva, en la Diabetes Mellitus (DM) suele RESPETARSE LA MOTILIDAD PUPILAR.
Otros pares frecuentemente afectados son el IV, VI y VII.
2. Mononeuropatías por Atrapamiento
Cualquier nervio periférico puede afectarse (mediano, radial, cubital, peroneo, ciático, etc).
Por lo general, las lesiones son unilaterales, aunque en casos excepcionales pueden ser simétricas.
Su pronóstico suele ser bueno y al cabo de varios meses se recuperan satisfactoriamente si la lesión se localiza distalmente.
3. Neuropatía Tronco- Abdominal
Se produce una afectación aguda y dolorosa unilateral de uno o más nervios torácicos. Cursa con dolor y disestesias unilaterales en tórax y abdomen que pueden confundirse con una afectación herpética en fase previa a la erupción.
La detección depende de la sensibilidad de los métodos diagnósticos empleados.
Procedimientos propuestos por consenso ALAD:
Procedimientos más utilizados en el examen médico para evaluar neuropatía periférica
• Sensibilidad vibratoria → Diapasón de 128 Hz colocado en el grueso artejo (1)
• Sensibilidad presora → Monofilamento de 10 g aplicado en el dorso del grueso artejo (1)
• Sensibilidad dolorosa → Punta de alfiler aplicada en el dorso del grueso artejo (1)
(1) Artejo mayor, dedo gordo del pie
Examen clínico breve para pesquisaje propuesto por el grupo de Michigan (cada pie aporta un puntaje por separado).
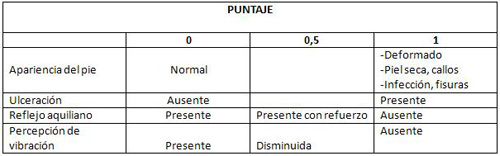
La PROBABILIDAD DE NEUROPATÍA ES ALTA si el puntaje es > 2/8 (sensibilidad 80% especificidad 95%)
Examen clínico neurológico completo propuesto por el grupo de Michigan (cada miembro aporta un puntaje por separado).
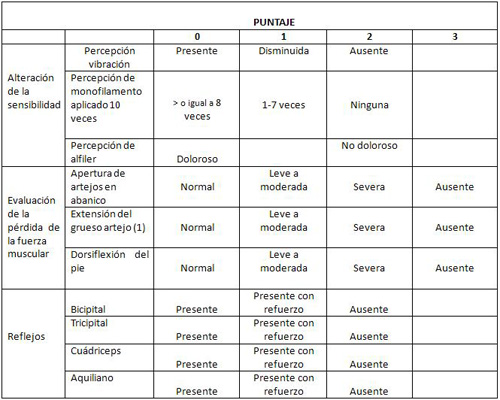
(1) Artejo mayor, dedo gordo del pie.
Se considera DIAGNÓSTICO DE NEUROPATÍA PERIFÉRICA si el puntaje es 7/46 (sensibilidad 80% especificidad 100%)
Recomendaciones
- En todas las formas clínicas mantener un buen control de la glucemia puede evitar o retardar el proceso. (A/ADA)
- Todos los pacientes deben ser examinados, con pruebas clínicas simples, para le detección de Polineuropatía distal simétrica (PND), el momento del diagnóstico y por lo menos una vez al año (B/ADA)
- Las pruebas electrofisiológicas no suelen ser necesarias, excepto bajo hallazgos clínicos alterados. (E/ADA)
- La detección de signos y síntomas de Neuropatía Autonómica se debe instaurar al momento del diagnóstico de la Diabetes Mellitus (DM) tipo 2 y a los 5 años del diagnóstico de la Diabetes Mellitus (DM) tipo 1. (E/ADA)
- Se recomienda el uso de fármacos para el tratamiento de la Polineuropatía distal simétrica (PND) y autonómica, con el objetivo de aliviar los síntomas y mejorar la calidad de vida de los pacientes.
- Para el manejo del dolor:
- Analgésicos comunes tipo acetaminofén, iniciando con dosis bajas (D/ALAD) o tramadol 200 mg/día (B/ALAD)
- Antidepresivos tricíclicos tipo amitriptilina 10 a 150 mg a la hora de acostarse (B/ALAD)
- Anticonvulsivantes: Carbamazepina 200- 600 mg (B/ALAD), gabapentina 600 a 2.400 mg (B/ALAD)
- Ansiolíticos: Flufenazina 1- 3 mg al acostarse (D/ALAD), diazepam 2- 5 mg 1 a 3 veces por día (D/ALAD)
- Acido alfa lipoico 600 - 1.200 mg (B/ALAD)
- Tópicos: Capsaicina (C/ALAD) usar con precaución.
- Tratamiento de la lesión neuronal: por el momento ningún fármaco ha demostrado ser claramente efectivo para modificar la historia natural de la neuropatía. A continuación se enumeran algunos sugeridos:
- Inhibidores de la aldosa reductasa: Aunque existen estudios que demuestran mejoría de la conducción nerviosa motora, su eficacia clínica no ha sido consistente y por el momento no hay ninguno disponible
- Acido alfa lipoico
- Acido gamalinolénico
- Factor de crecimiento neuronal recombinante
- Vitamina E
- Cuidado preventivo de los pies (ver pie diabético)
- Neuropatía Autonómica: La mayoría de los estudios que sustentan estos tratamientos no superan el nivel 3 de evidencia y suelen estar dirigidos al alivio de los síntomas. Por lo tanto la mayoría de las recomendaciones son producto de consenso: (D/ALAD)
- Hipotensión ortostática: Evitar los cambios posturales bruscos, Uso de medias o calzas compresivas, fármacos que retienen sodio (alfa- fluorohidrocortisona)
- Disfunción gastroesofágica: Metoclopramida, domperidona.
- Diarrea diabética: Antibióticos de amplio espectro, loperamida, disminuir la fibra alimentaria.
- Vejiga neurogénica: Entrenamiento vesical (evacuación completa incluyendo maniobras de compresión abdominal), cateterismo vesical intermitente, tratamiento de las infecciones urinarias, betanecol.
- Disfunción sexual: Apoyo psicoterapéutico; Fármacos vía oral: Sildenafil, fentolamina; Fármacos transuretrales: Alprostadil; Fármacos de aplicación intracavernosa: Papaverina, fentolamina, alprostadil; Prótesis peneana.
Pie Diabético
Se denomina pie diabético al pie que tiene al menos una lesión con pérdida de continuidad de la piel (úlcera).
Las úlceras en el paciente con Diabetes Mellitus (DM) son de 2 tipos:
Isquémico: predominan en las extremidades inferiores y se producen como consecuencia de la afección arterial. Son úlceras de bordes bien delimitados, superficiales, de fondo atrófico, muy dolorosas, aumentando con el decúbito y localizadas principalmente en el tercio inferior de la pierna, principalmente sobre prominencias óseas: cabezas de metatarsianos, maléolo externo y tibia.
Neuropáticas: situadas en los puntos de apoyo del pie, de bordes mal delimitados, son profundas e indoloras. El pie diabético constituye en el principal factor de riesgo para la amputación de la extremidad. La principal medida para prevenir esta complicación es el tratamiento precoz y oportuno de las úlceras.
Factores de riesgo para el pie diabético
• NEUROPATÍA PERIFÉRICA (tanto SOMÁTICA, como AUTONÓMICA)
• ENFERMEDAD VASCULAR PERIFÉRICA (tanto MACRO como MICROVASCULOPATÍA PERIFÉRICA)
Ambos constituyen los dos factores de riesgo principales, otros son:
• Infección
• Trauma
• Alteraciones de la biomecánica del pie
Condiciones favorecedoras de su desarrollo
• Edad avanzada
• Larga duración de la diabetes
• Sexo masculino
• Estrato socioeconómico bajo y pobre educación
• Factores sociales como vivir solo, ser poco visitado, poca motivación por vivir
• Pobre control glucémico
• Presencia de retinopatía, nefropatía, enfermedad macrovascular.
Principales Signos y Síntomas de los Componentes que Conducen al Pie Diabético
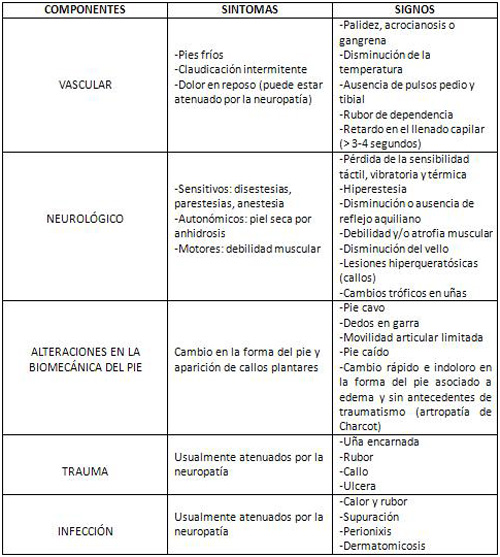
Clasificación de los Grados de Severidad del Pie Diabético de Acuerdo con la Escala de Wagner.
GRADO 0
Pie en riesgo por presencia de enfermedad vascular periférica, neuropatía, deformidades ortopédicas, pérdida de la visión, nefropatía, edad avanzada.
GRADO 1
Ulcera superficial
GRADO 2
Ulcera profunda que llega a tendón, ligamento, articulaciones y/o hueso.
GRADO 3
Infección localizada: celulitis, absceso, osteomielitis.
GRADO 4
Gangrena local
GRADO 5
Gangrena extensa
Evaluación del Paciente Diabético
→ Pacientes SIN FACTORES DE RIESGO: evaluación anual
→ Pacientes CON FACTORES DE RIESGO: evaluación completa anual + examen de los pies en cada consulta.
1. Establecer el estado de salud general del paciente, presencia de comorbilidades, estado de control glucémico y metabólico, historia de intervenciones previas (cirugías de revascularización o reconstructivas de pie, desbridamientos, ortesis, etcétera).
2. Evaluar las lesiones del pie diabético. Deben tenerse en cuenta los siguientes aspectos:
• Historia médica de la lesión de pie (antecedentes de trauma, heridas, que inició el proceso, duración de la herida, progresión, tratamiento y su desenlace).
• Evaluación clínica de la herida (profundidad, extensión, localización, apariencia, temperatura, olor, presencia de infección.
• Evaluar la presencia de infección superficial o profunda: Identificar la presencia de drenaje purulento, celulitis, inflamación y edema alrededor de la úlcera y abscesos profundos. Si en la exploración de la úlcera se observa hueso, o éste se puede tocar con una sonda, existe una alta probabilidad de osteomielitis. Uso auxiliares diagnósticos tales como radiología, cultivos de gérmenes, gammagrafía ósea y resonancia nuclear magnética.
3. Examen neurológico del pie:
Es recomendable remitirse al tema de complicaciones neurológicas, desarrollado previamente, pero básicamente se considera la realización de cinco pruebas sencillas:
• uso de un monofilamento de 10 g
• vibración valorada con un tenedor de 128 Hz
• pruebas de sensibilidad pinchazo
• reflejo del tobillo evaluación y las pruebas de percepción de la vibración umbral con un biotesiómetro)
4. Examen vascular
• Inspección (color, características, alteraciones tróficas). Palpación de pulsos, sobre todo pedio y tibial posterior, pero también se deben evaluar el resto de pulsos incluyendo los poplíteos y los femorales.
• Índice isquémico: Se calcula midiendo la tensión arterial sistólica (TAS) del tobillo con la ayuda de un equipo de ultrasonido cuyo transductor se coloca sobre la arteria tibial posterior o la pedia y dividiéndola por la TAS que resulte más alta de los dos brazos. El índice normal debe ser igual o mayor a 0.9.
• Cuando se sospecha un compromiso vascular severo, está indicado un estudio vascular no invasivo (doppler).
• La arteriografía se realizaría como paso previo a una posible cirugía vascular.
5. Evaluación de la estructura y deformidades del pie.
• Se debe buscar particularmente la retracción de los dedos en forma de garra que suele originar callos y úlceras neuropáticas plantares a nivel de las cabezas de los metatarsianos.
• La presencia de callos plantares indica una presión inadecuada que predispone a úlceras neuropáticas.
• El clínico se puede ayudar con auxiliares diagnósticos como el podoscopio o la rejilla de Harris que permiten evaluar la distribución plantar de la presión del cuerpo en reposo y con aparatos electrónicos más sofisticados también durante la marcha.
Tratamiento del Pie Diabético
En primera instancia, el médico debe definir si el manejo debe ser ambulatorio u hospitalario, el compromiso del estado general, así como los factores sociales influyentes en el cumplimiento del tratamiento.
Las pautas a seguir se basan en una serie de recomendaciones:
Recomendaciones (ADA/ALAD)
- Control glucémico óptico (B/ALAD) y de las comorbilidades.
- En todos los pacientes Diabetes Mellitus (DM), lleve a cabo un examen ANUAL del pie completo, teniendo en cuenta: (ADA)
- Identificar los factores de riesgo y favorecedores del desarrollo del pie diabético
- Que el examen de los pies debe incluya:
1. Inspección de las extremidades
2. Palpación de pulsos
3. Valoración neurológica con Pruebas de pérdida de la Sensibilidad: realizadas con monofilamento de 10 g, más una prueba de cualquiera de: la vibración con prueba con un tenedor de 128 Hz, vibración mediante un biotesiómetro, sensación de pinchazo o los reflejos del tobillo. (B/ADA)
Los principales indicadores de un pie en riesgo son la disminución severa de la sensibilidad vibratoria (equivalente a más de 25 v utilizando un biotesiómetro) y/o la incapacidad para sentir el monofilamento de 10 g. (evidencia nivel 1/ALAD)
● Educación de autocuidado a todos los pacientes con diabetes. (B/ADA)
● Un enfoque multidisciplinario, se recomienda para las personas con úlceras del pie y de alto riesgo, los pies, especialmente aquellos con antecedentes de úlcera o amputación previa. (B/ADA)
● Consulte en los pacientes que fuman si: tienen pérdida de sensibilidad, presentan anormalidades estructurales, o si tienen historia previa de complicaciones en las extremidades inferiores. Se recomienda que dichas complicaciones, sean valoradas por especialistas, con vigilancia toda la vida. (C/ADA)
● Valoración vascular: Signos y síntomas. Valoración de pulsos e Índice brazo- tobillo. (C/ADA). En los pacientes con claudicación significativa o un IBT positivo: considera el ejercicio, medicamentos y opciones quirúrgicas. (C/ADA)
Aunque existen datos limitados que soporten los diferentes tratamientos específicos del pie diabético, las siguientes intervenciones son importantes: (ALAD)
• Aliviar presión: se recomienda retirar el peso de la extremidad mediante el simple reposo, el uso de bastón o muletas para evitar el apoyo o el uso de calzado especial que permita mantener la zona de la úlcera libre (D). En úlceras crónicas no infectadas y sin componente isquémico, uno de los métodos más efectivos para aliviar la presión focal es el yeso de contacto total (AA).
• Desbridamiento: la remoción quirúrgica del tejido desvitalizado de las heridas ha demostrado curar más rápidamente las úlceras neuropáticas (A). El desbridamiento químico no tiene suficiente soporte como para ser recomendado.
• Drenaje y curaciones de la herida mediante el lavado con solución salina. Se recomienda cubrirla con apósito impregnado con coloides que mantengan la humedad (D).
• Manejo de la infección. Los antibióticos deben utilizarse teniendo en cuenta que la mayoría de las infecciones superficiales son producidas por gérmenes gram positivos y las profundas por una asociación de gram positivos, gram negativos anaerobios (D). Los antibióticos tópicos no han demostrado que logren mejores resultados.
• Mejorar el flujo vascular. La pentoxifilina se ha utilizado con la intención de mejorar la perfusión sanguínea a nivel distal (evidencia nivel 3). La revascularización agresiva cuando hay severo compromiso vascular ha demostrado disminuir las amputaciones (evidencia nivel 3).
• Amputación. La decisión de realizar una amputación se toma después de probar medidas de salvamento y de una extensa discusión con el ortopedista, el cirujano vascular y los demás miembros del equipo, que debe incluir al paciente y su familia. Una amputación bien realizada, en el momento apropiado y con una exitosa rehabilitación puede mejorar la calidad de vida de un paciente.
• Existen otros tratamientos que todavía carecen de una evidencia razonable como oxígeno hiperbárico, factores de crecimiento del tipo del becaplermin, equivalentes de piel viva, estimulación eléctrica y láser frío.
Caso Clínico
Paciente de 45 años de edad actualmente, oriundo La coronilla, departamento de Rocha, Uruguay, casado desde el año 1988, 2 hijos, con antecedentes de Diabetes Mellitus (Diabetes Mellitus (DM)) Tipo 1, diagnosticado a los 27 años de edad.
Antecedentes E Historia De Su Enfermedad
Mes 09/1994: Según lo que relata el paciente, el día que efectuaron su diagnóstico, el había acompañado, junto a su esposa, a su suegro a una consulta habitual con su médico de cabecera, en clínica Millenium de Zárate, actualmente en inactividad; En la sala de espera vio un afiche informativo que llamó su atención al describir similares síntomas que él estaba presentando desde hacía unos 3 meses aproximadamente y por haberle restado importancia, nunca había consultado. Presentaba síntomas de: somnolencia, agotamiento, sed intensa y poliuria, además de intensa picazón en la zona de genitales.
Al salir el familiar de la consulta, él le plantea al médico su inquietud, quien decide realizarle de forma inmediata una glucemia, arrojando esta un resultado de 498 mg/dl. Por presentar clínica cardinal y dicha cifra de glucemia, fue diagnosticado de Diabetes Mellitus (DM) tipo 1, siendo tratado con hidratación endovenosa e insulinoterapia, quedando internado en observación unas horas. Luego, al ser dado de alta se le indica comenzar un tratamiento medidas higiénico- dietéticas e Insulina NPH y eventual corrección con Insulina corriente e interconsulta al especialista en endocrinología para comenzar con los controles regulares. En ese momento el paciente, por una oportunidad laboral, había migrado y radicado en la Argentina desde el año 1979, viviendo temporalmente en La Pampa y en Bahía Blanca y finalmente instaurándose definitivamente en Zárate, provincia de Buenos Aires en el año 1988.
Relata que desde que llegó a la argentina hasta julio del año 2009, trabajó en el área de construcción, pasando mucho tiempo afuera de su casa. Refiere que, por tales implicancias y por otros motivos socioeconómicos, desde el momento de su diagnóstico hasta la actualidad, no siguió el régimen higiénico- dietético indicado para su enfermedad, así como tampoco pudo controlarse periódicamente. Además nos cuenta que, por un período de 2 años aproximadamente, no recibió Insulina, siendo medicado en su reemplazo con hipoglucemiantes orales, debido a que su Obra Social no efectuaba su cobertura y el paciente no disponía de recursos para obtenerla. De todos modos dicho control ha mejorado en los últimos años, debido, principalmente, a la evolución avanzada de la misma y las complicaciones padecidas en el último tiempo, aunque no presenta la adherencia óptima al seguimiento y tratamiento de su enfermedad.
Mes 03/2001: Colecistectomía videolaparoscópica (VLP)
Mes 09/2005: Apendicectomía vía convencional.
Mes 03/2005: 1° internación por complicación Diabetes Mellitus (DM): Mal perforante plantar por polineuropatía diabética: úlcera en pie Izquierdo, complicada con osteomielitis. Comenzó con una lesión de contigüidad de la piel que no cicatrizaba, por lo cual consulta al cabo de un mes. Requirió internación por 33 días en el Sanatorio Franchín, Capital Federal, recibiendo cómo tratamiento: toilette quirúrgica, curaciones locales y antibióticoterapia. Fue dado de alta al resolverse la misma.
Mes 03/2008: 2 ° internación: Recidiva de mal perforante plantar: úlcera en el mismo sitio de pie Izquierdo. La internación duró 15 días aproximadamente, fue en el Sanatorio Franchín. Se le realiza Ecodoppler de arterias de ambos miembros inferiores (pese a que no contamos con tal informe el paciente refiere que el médico le informó compromiso vascular de ambos miembros a predominio del lado derecho).
Mes 12/08: 3° internación: Glucemia >600 y Síndrome nefrótico. Estuvo internado en la clínica Delta de Campana, Buenos Aires, por aproximadamente 15 días. Al alta agregó como tratamiento: dieta con restricción proteica a 0,8 mg/kg/día, Enalapril, losartán y furosemida.
13/07/09: 4Ş internación: Anasarca e Insuficiencia Renal Aguda. Internación de 1 semana en clínica Delta. Consulta por edemas, muy acusados en cara y genitales, refiere además oliguria. Se constatan edemas severos generalizados, se destaca: derrame pleural bilateral. Es diagnosticado de Insuficiencia Renal Crónica (IRC), nefropatía DBT en estadio clínico IV comienza a ser tratado con hemodiálisis 17/07/09 en la misma clínica y se le indica al alta continuar con un plan trisemanal de hemodiálisis en el Instituto Nefrológico de Zárate, donde actualmente continúa siendo tratado. Desde dicho momento, prácticamente la totalidad del seguimiento del paciente, es llevada a cabo por por parte de los médicos nefrólogos, ya que no concurre al médico clínico ni a al médico endocrinólogo, así como a ningún otro especialista.
Mes 11/09: Se indica Interconsulta con Oftalmología. Diagnóstico: Cataratas y retinopatía diabética, se le realizó: retinofluesenografía. El paciente no regresó a nuevo control.
11/02/10: 5Ş internación, 1Ş internación en nuestro nosocomio: Sanatorio Carlos MIner, Zárate, Prov. De Bs. As. (El cambio de institución se debió a una modificación de su cobertura médica). Celulitis en cara interna de rodilla derecha.
MOTIVO DE CONSULTA (MC): Dolor en cara interna de rodilla derecha con signos de flogosis. Además refiere escalofríos.
Enfermedad Actual
El paciente refiere que había estado los días previos en la ciudad de La Pampa, viviendo con amigos, habiéndose trasladado para realizar un trabajo temporario por un período de 2 a 3 meses de duración. Nos cuenta que se movilizaba descalzo dentro de la casa, así como en el patio, sitio donde caminaban también aves (gallinas) entre otros animales. Refiere que comenzó con un dolor, tipo punzante, al comienzo intermitente y que a las 24 hs aproximadamente notó que se le puso “colorada” la región interna de la rodilla, motivo por el cual tomó la decisión de regresar a su hogar, se le da el permiso, llegando a Zárate y consultando así a nuestro servicio.
Se interna en UTI, se realizan hemocultivos y se realiza ecografía de rodilla derecha. Se comienza tratamiento empírico con Vancomicina cada 4 días.
- Ecografía: descarta Artritis séptica. Impresiona tenosinovitis o bursitis.
- Hemocultivos + a St. Pyogenes
- Ecocardiograma: normal.
Se le da el alta, luego de 4 días de internación, 2 en UTI y 2 en sala general. El paciente debe viajar nuevamente a La Pampa a su trabajo, se indica continuar con clindamicina + ciprofloxacina vía oral.
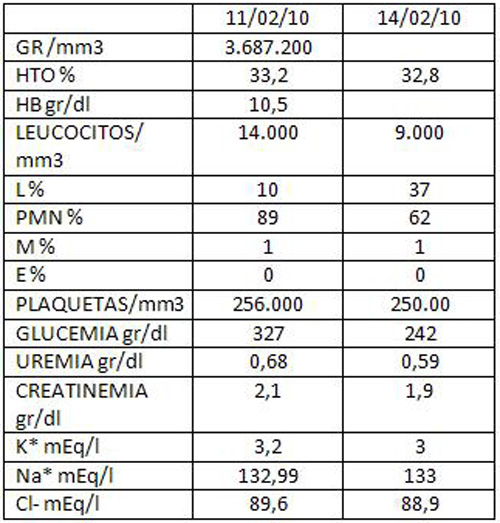
Mes 10/09: Gastropatresia y enteropatía diabética. El paciente refiere que desde el año 2005 aproximadamente presentaba síntomas de nauseas, molestias a nivel del epigastrio, distensión abdominal y diarrea, atribuyéndolo a la ausencia de la vesícula biliar. Durante su estadía e internación en La Pampa, sufrió un episodio de exacerbación de la diarrea, siendo interpretada como diarrea crónica y medicado con trimabutina 400 mg/día más loperamida 2mg/48 horas. Se le realiza CFC: biopsia: infiltrado inflamatorio inespecífico. Tratamiento sintomático: dieta, trimebutina y loperamida.
Mes Julio/ 2010: 6ta internación: Tenosinovitis supurada MC: Dolor en mano y muñeca izquierda. ENFERMEDAD ACTUAL: el paciente refiere que comienza con un dolor muy importante en la cara interna de muñeca y palma izquierdas, de tipo continuo, con exacerbación con los movimientos asociado a impotencia funcional, de 72 hs de evolución aproximadamente. Al principio tomaba ibuprofeno y calmaba, luego ya no. El lunes al llegar a diálisis consulta y le indican dorixina, sospechando un dolor musculo tendinoso atribuido erróneamente a un mal esfuerzo, se le indica una ecografía de mano (no contamos con su informe). En dicho estudio se detecta colección. Por este motivo se interna, por un período de 10 días (5 días en UTI y 5 días en sala general), en Sanatorio Vandor en Campana, provincia de Bs. As., recibiendo como tratamiento antibióticoterapia y drenaje quirúrgico.
Además, refiere que la rodilla continuaba “hinchada” pero sin signos de flogosis
18/10/10: 6Ş internación del paciente. Estado hiperosmolar no cetósico. MOTIVO DE INGRESO: vómitos, dolor abdominal y alteración del sensorio. ENFERMEDAD ACTUAL: paciente refiere que comenzó con dolor abdominal y vómitos de aproximadamente 3 hs de evolución agregando posteriormente alteración del sensorio. AL EXAMEN FÍSICO: Glucemia 550 mg/dl. Mal perforante plantar derecho, lesión ulcerada. Se constata aparente vasculopatía periférica en miembro inferior derecho (pulso pedio no palpable, tibial posterior positivo débil). Se interpreta como un cuadro de estado hiperosmolar hiperglucémico no cetósico (EHHNC), ingresa a UTI, descompensación a punto de partida de una infección en pie diabético derecho. IRC reagudizada. Se pancultiva y se comienza tratamiento con Vancomicina + Imipenem.
Laboratorio
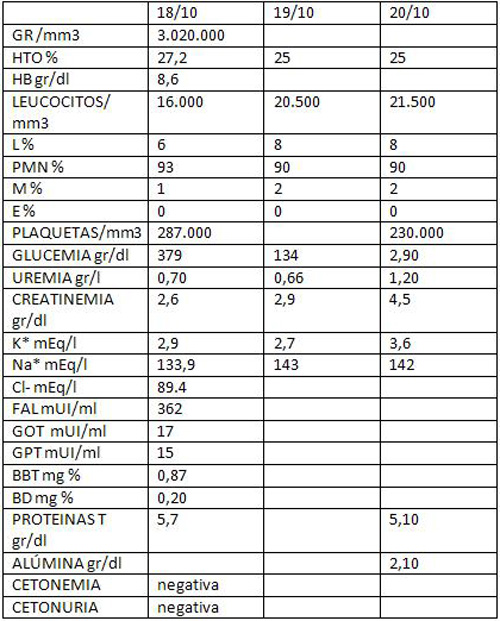
Por presentar síntomas digestivos de dispepsia intensa durante la internación, se le realiza un video endoscopía digestiva alto (VEDA): gastropatía inflamatoria.
Ecodoppler de miembros inferiores (MMII) (20/10/10), INFORME: “Venoso: elasticidad conservada, no se encuentran focos fibróticos, no se observan perforantes varicosas.
Exploración arterial: Lado derecho: segmentos Arteriales femoral común, femoral superficial y profunda, poplítea, tibial posterior, superior y retromaleolar, tibial anterior y pedia: todos los segmentos arteriales muestran paredes engrosadas, con carga ateromatosa, flujometría monofásica turbulenta, con velocidades máximas con evidencia de compromiso hemodinámico. Lado Izquierdo: segmentos Arteriales femoral común, femoral superficial y profunda, poplítea, tibial posterior, superior y retromaleolar, tibial anterior y pedia: todos los segmentos muestran paredes engrosadas, con carga ateromatosa. Flujometría monofásica y bifásica, con velocidades máximas con evidencia de compromiso hemodinámico desde la arteria femoral común, acentuándose en la poplítea, con una estenosis de consideración y a nivel de la arteria tibial posterior no detecta código color ni señal doppler, solamente una colateral con señal mínima.
Impresión diagnóstica: ISQUEMIA MODERADA A SEVERA IZQUIERDA – ISQUEMIA CRÍTICA DERECHA”.
Se toma como conducta la realización de una AMPUTACIÓN SUPRACONDÍLEA de miembro inferior derecho, para lo cual es trasladado desde nuestra institución al Sanatorio “Augusto Timoteo Vandor”, situado en Campana, Bs. As, donde es internado e intervenido el día 21/10/10, cursando internación, con buena evolución, hasta el día 01/11/10 en que fue dado de alta.
31/05/11: 7° internación del paciente: Fractura de fémur. Paciente que ingresa por caída desde su altura durante rehabilitación, se le realiza radiografía de pelvis donde se constata fractura de fémur, fue trasladado nuevamente a Sanatorio “Augusto Timoteo Vandor”, situado en Campana, Bs. As, donde es internado e intervenido quirúrgicamente el 07/06/11: Osteosíntesis de cadera Izq. Con buena evolución durante su internación.
Es dado de alta el 14/06/11.
20/06/11 01 hs: 8° internación del paciente. Neumonía aguda de la comunidad (NAC). MOTIVO DE INGRESO: Paciente 44 años, ingresa por cuadro febril de 48 horas de evolución, tos y expectoración mucopurulenta y diarrea acuosa, náuseas y deshidratación moderada a severa, somnoliento. Se solicita: hemo, uro y coprocultivos. Se interna en sala general y se comienza tratamiento empírico con Ampicilina- sulbactam + claritromicina.
A las 13 horas a la salida de diálisis, ingresa a UTI por presentar gran deterioro del estado general, se rota el tratamiento a: Amikacina + ceftazidima + vancomicina. El paciente tuvo buena respuesta, mejorando su evolución. Los cultivos fueron negativos. Curso internación de 10 días en total, en UTI y sala general. Se da de alta el 27/06/11.
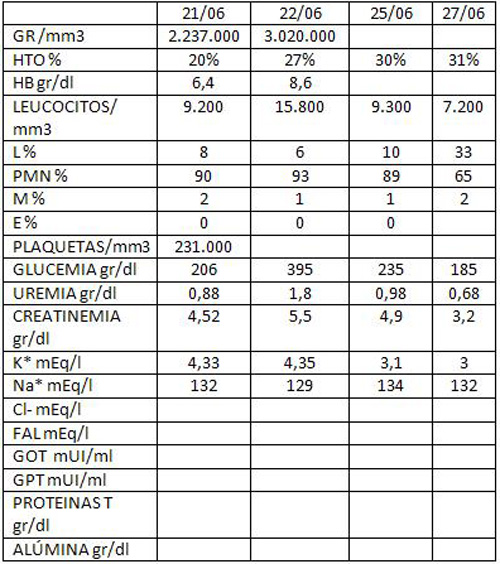
Mes de febrero de 2012: Al momento el paciente se encuentra estable .Presenta úlcera pequeña en pie Izquierdo, que está siendo tratada con curaciones locales. Continúa con su régimen de diálisis trisemanal y con su parcial cumplimiento higiénico- dietético, así como su Insulinoterapia.
Anexo
El nivel o grado de evidencia clínica es un sistema jerarquizado, basado en estudios de investigación, con el objeto de validar la fortaleza o solidez de la evidencia de la práctica profesional.
Niveles De Evidencia y Grados de Recomendación
Según la AHRQ (Agency for Healthcare Research and Quality)
Nivel de evidencia
- Ia: La evidencia proviene de metaanálisis de ensayos controlados, aleatorizados, bien diseñados.
- Ib: La evidencia proviene de, al menos, un ensayo controlado aleatorizado.
- IIa: La evidencia proviene de, al menos, un estudio controlado bien diseñado sin aleatorizar.
- IIb: La evidencia proviene de, al menos, un estudio no completamente experimental, bien diseñado, como los estudios de cohortes. Se refiere a la situación en la que la aplicación de una intervención está fuera del control de los investigadores, pero cuyo efecto puede evaluarse.
- III: La evidencia proviene de estudios descriptivos no experimentales bien diseñados, como los estudios comparativos, estudios de correlación o estudios de casos y controles.
- IV: La evidencia proviene de documentos u opiniones de comités de expertos o experiencias clínicas de autoridades de prestigio o los estudios de series de casos.
Grado de la recomendación
• A: Basada en una categoría de evidencia I. Extremadamente recomendable.
• B: Basada en una categoría de evidencia II. Recomendación favorable
• C: Basada en una categoría de evidencia III. Recomendación favorable pero no concluyente.
• D: Basada en una categoría de evidencia IV. Consenso de expertos, sin evidencia adecuada de investigación.
Referencias Bibliográficas
1. Harrison Principios de Medicina Interna 17a edición. Año 2008 Editorial: Mcgraw- Hill
2. Medicina interna de Farreras- Rozman 16Ş edición. Año 2008. Editorial Elsevier.
3. Standards of Medical Care in Diabetes. Año 2011. AMERICAN DIABETES ASSOCIATION .(ADA):
4. Williams Tratado de Endocrinología. Kronenberg, H. M; Shlomo Melmed y otros. 11Ş edición. Año 2009. Editorial Elsevier
5. Guías ALAD (asociación latinoamericana de diabetes) de diagnóstico, control y tratamiento de la diabetes mellitus tipo 2. Año 2010.
6. Evidencia científica en EPOC. Manual de actuación. Año 2006.