La muerte súbita en pacientes con patología coronaria no es un hecho aislado. Casi 80% de los pacientes hallados muertos en su casa, antes de recibir ayuda médica, después de la autopsia se ha confirmado la obstrucción del tronco común sea por placa o por trombo o lesión del 90% en la zona de bifurcación. La inmediata reacción del médico en situación aguda, o la correcta interpretación del electrocardiograma mientras el paciente está en urgencias pueden salvar la vida del paciente. Los errores en cuanto a su correcta interpretación y manejo agudo es la causa del aumento de mortalidad.
Paciente diagnosticado de enfermedad multivaso con electrocardiograma normal. A propósito de un caso clínico
Dr. Oswald Londono, MD, PhD, Dra. Susana Pacreu, Hospital del Mar, Barcelona
Palabras clave: muerte súbita; enfermedad del tronco común; isquemia severa; sudden death; common trunk occlusion; ischeamic heart disease.
Introducción
La muerte súbita en pacientes con patología coronaria no es un hecho aislado. Casi 80% de los pacientes hallados muertos en su casa, antes de recibir ayuda médica, después de la autopsia se ha confirmado la obstrucción del tronco común sea por placa o por trombo o lesión del 90% en la zona de bifurcación. La inmediata reacción del médico en situación aguda, o la correcta interpretación del electrocardiograma mientras el paciente está en urgencias pueden salvar la vida del paciente. Los errores en cuanto a su correcta interpretación y manejo agudo es la causa del aumento de mortalidad.
Introduction
Sudden death in patients with coronary heart disease is not an isolated fact. Almost 80% of patients founded dead at home, before medical assistence, was confirmed after autopsy the several lesions on the commom trunk with trombs or plaques or 90% lesion at the bifurcation zone. The immediate reaction of the physician or the correctly interpretation of the ECG at the Emergency Department can save patient life. Mistakes in EKG interpretation and management of the acute case are the mean cause of high mortality.
Caso clínico
Presentamos el siguiente caso:
Paciente de 74 años de edad que acude a urgencias por disconfort centrotorácico. No palpitaciones, no vegetatismo, no disnea. No fiebre ni otra sintomática.
Antecedentes patológicos:
No alergias conocidas.
No DM, no EPOC.
Hipertensión arterial (HTA) estable
Adenoma benigno de próstata.
IQ: Amigdalectomía.
Tratamiento actual: omeprazol, calcio, torasemida, urolisin.
Al llegar a urgencias se le realiza un primer (1) electrocardiograma (ECG) (19:20) sin dolor que muestra: ritmo sinusal a 65 latidos por minuto, sin apreciarse alteración de la repolarización aguda. PR, QRS y QT dentro de la normalidad.
Enzimas y troponinas negativas.Ā
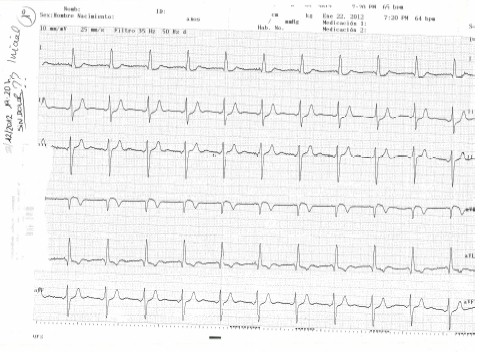
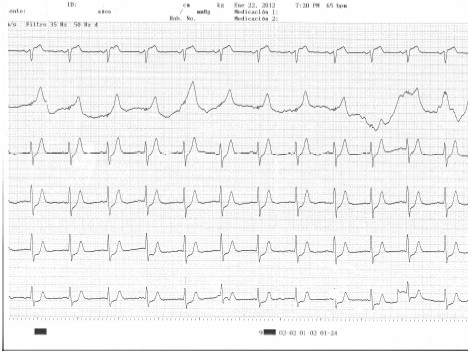
Segundo electrocardiograma (ECG) (2) (22:05): ritmo sinusal a 73 latidos por minuto. PR, QRS y QT dentro de la normalidad. Ondas R pequeñas en V1V2. No se aprecian cambios importantes respecto al anterior.
Continua asintomático.Ā
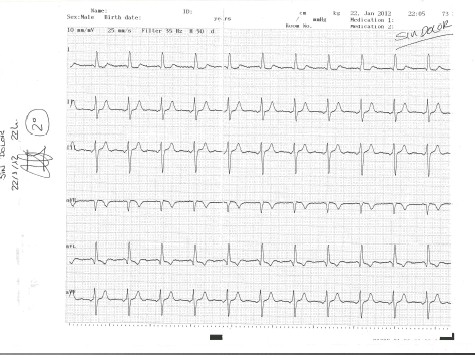
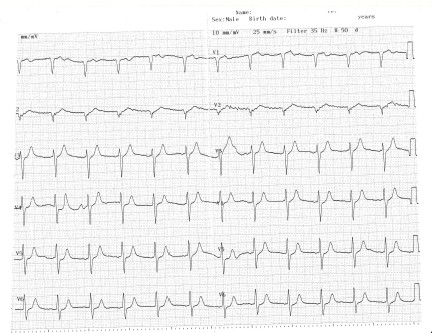
El paciente solicita el alta a su domicilio, pues se encuentra asintomático y según los comentarios del médico de urgencias, no se trata de una angina de pecho.
Al comentar con el cardiólogo de guardia, éste interroga de nuevo al paciente y la sensación “quemante” precordial, no irradiada, le llama la atención, pero con electrocardiograma (ECG) no determinante y enzimas y troponinas negativas no le queda muy claro.
Pasados 30 minutos decide solicitar una coronariografía. El motivo: un electrocardiograma (ECG) no muy típico para la edad del paciente, el cual tiene como factor de riesgo vascular: obesidad e hipertensión arterial (HTA).
Debería tener algunos cambios electrocardiográficos, pero no presentar un electrocardiograma (ECG) tan anormal para la edad del paciente.
Se constata que el electrocardiograma (ECG) sea del paciente y realiza un nuevo electrocardiograma (ECG), él mismo, sin encontrar cambio alguno.
Debido a las dudas que dejaba el caso se decide por el cateterismo cardiaco urgente.
Coronariografía: el paciente es trasladado a la sala de hemodinámica, por vía radial se introduce catéter hasta la aorta. En todo momento el cardiólogo habla con el paciente, hasta que se aprecia en el monitor algo parecido a artefactos, se suponía que era la conexión de los cables al monitor, pero al observar al paciente, éste se encontraba muy pálido y ausente. Se intenta hacerlo reaccionar con una bofetada y al mismo tiempo se retira el catéter de la aorta. El paciente no reacciona, se registra taquicardia ventricular tipo Torsade de Pointes, requiriendo una descarga de 100 jouls y recuperando ritmo sinusal y consciencia.
La sorpresa la vemos en las imágenes de la coronariografía.
Se observa oclusión de la arteria descendente anterior, diagonal y ramo interventricular, que se tratan mediante la implantación de 3 stents coronarios.
La coronaria derecha no se intervino por tratarse de una arteria larga, irregular, con lesiones importantes, pero que no representaba en el momento una prioridad. Se decidió tratar de forma programada.
Coronaria izquierda
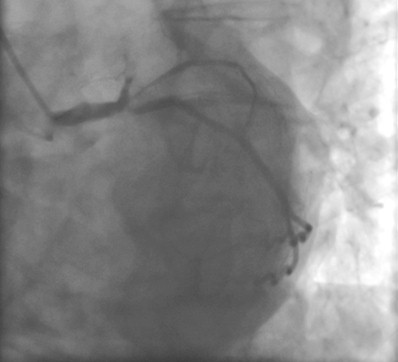
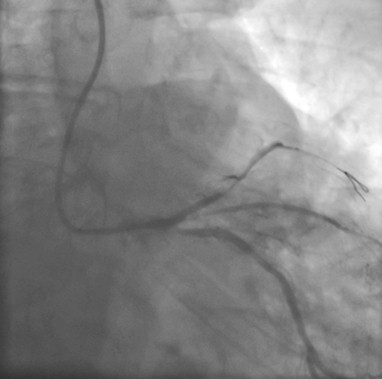
Oclusión de la DA, Diagonal y el del ramo interventricular.
Coronaria derecha
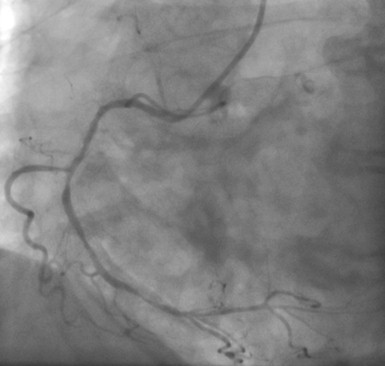
Arteria coronaria derecha con muchas irregularidades, lesiones en el segmento medio y distal. No se observa circulación colateral.
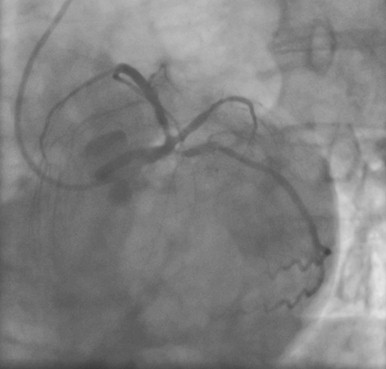
Después de la implantación de tres stents.
El paciente ingresó a la UCI cínica y hemodinámicamente donde permaneció 3 días. Se realizaron 2 ecocardiografías doppler que evidenciaron una fracción de eyección (FE) del 40%.
Al alta la fracción de eyección (FE) era de 53%, con hipocinesia anterolateral moderada.
Discusión
La muerte súbita en pacientes con cardiopatía isquémica silente
Los pacientes que han tenido un episodio de angina inestable o un infarto del miocardio tienen un elevado riesgo de muerte súbita. Pero aquellos pacientes que mueren súbitamente y en la autopsia se revela la presencia de enfermedad coronaria severa no han tenido tanta suerte, a pesar de la tecnología que poseemos actualmente.
La causa de esta muerte súbita es el desarrollo de arritmias ventriculares en la zona necrótica del miocardio.
La muerte súbita es la pérdida abrupta de la función cardiaca que conlleva a la aparición de arritmias, como bradicardia, taquicardia ventricular y, con más frecuencia, por fibrilación ventricular. Se calcula que el 15% de las autopsias que se realizan por muerte natural son muertes súbitas y, de éstas, el 75% son de origen cardiaco.
Del total de casos de muerte súbita de origen cardiaco, el 80 por ciento ocurre en pacientes con cardiopatía isquémica, entre ella, las enfermedades de las arterias coronarias y de las arterias periféricas. Tanto la oclusión de la arteria, como la reperfusión pueden originar arritmias, como la fibrilación ventricular, que conducen a la muerte súbita. Estos casos suelen ocurrir en personas mayores expuestas a factores de riesgo cardiovascular tales como hipercolesterolemia, hipertensión arterial, obesidad, diabetes y tabaquismo.
El 15 por ciento de las muertes súbitas cardiacas ocurren en pacientes que presentan una cardiopatía estructural, tales como en la miocardiopatía hipertrófica, la miocardiopatía arritmogénica del ventrículo derecho y la miocardiopatía dilatada, entre otras, siendo las dos primeras las principales causas de muerte súbita en jóvenes y deportistas.
Finalmente, en menos del cinco por ciento de las ocasiones, las causas de la muerte súbita cardiaca se dan en pacientes con cardiopatías arritmogénicas, donde el corazón es estructuralmente normal pero presenta fallos eléctricos. Las enfermedades cardiacas asociadas a estos episodios de muerte súbita son, principalmente, el síndrome de Brugada y el síndrome de QT largo, pero no debemos olvidar el síndrome de QT corto y la taquicardia ventricular polimórfica catecolaminérgica.
CAUSAS
Mientras que los ataques cardíacos (que suelen confundirse con muertes súbitas cardíacas) están causados por un problema de circulación del corazón, las muertes súbitas cardíacas se producen por algún problema eléctrico.
Así, su causa más importante suele ser tener una enfermedad cardiovascular previa, es decir, toda alteración de la función cardíaca causada por una dilatación del corazón, por una válvula dañada o por anomalías congénitas en el músculo del corazón, podrían motivar el episodio. No obstante, también se han dado casos de personas que no habían padecido ninguna patología de este tipo.
Entre las principales enfermedades cardiacas que pueden desencadenar la muerte súbita y que poseen un componente genético preponderante se encuentran:
Miocardiopatía Hipertrófica
Es una enfermedad hereditaria que se caracteriza por el engrosamiento del músculo cardiaco, más precisamente, del ventrículo izquierdo. Es la principal causa de muerte súbita en los adultos jóvenes (menores de 50 años), quienes desconocen su enfermedad.
Se han identificado 10 genes, de los cuales 9 codifican proteínas sarcoméricas. Entre ellos se encuentran los MYL2, MYL3, ACTC, TPM1, TNNT2, TNNI3, TTN (PRKAG2), MYH7 y MYBPC3. Si bien se han descrito muchas mutaciones asociadas a esta miocardiopatía, las más recurrentes hasta el momento se encuentran en los genes MYBPC3 y MYH7.
La herencia de esta miocardiopatía es autosómica dominante, es decir que los descendientes del paciente afectado tienen un 50 por ciento de posibilidades de poseer la mutación y desarrollar la enfermedad. Su prevalencia es de 1 de cada 500 individuos.
Miocardiopatía Dilatada
Es una enfermedad del corazón que se caracteriza por la dilatación anormal del ventrículo izquierdo y disfunción sistólica, incapacitando al músculo cardiaco para bombear sangre eficazmente. Esta cardiomiopatía suele ser causa de trasplantes cardiacos tanto en niños como en adultos y es una de las causas de muerte súbita. Si bien la prevalencia real aún no se conoce con exactitud, se estima en 1 de cada 3.000 individuos.
De los estudios realizados en pacientes con miocardiopatía dilatada, se han identificado más de 20 mutaciones en 15 genes. La mayoría de ellas son de herencia autosómica dominante, es decir que los descendientes del paciente afectado tienen un 50 por ciento de posibilidades de poseer la mutación y desarrollar la enfermedad.
Entre los genes identificados se encuentran ACTC, TPM1, MYH7, TNNT2, TNNI3, MYBPC-3, TTN, TCAP, DES, DMD, VCL, SGSD, ACTN2 y, LMNA/C. Muchos de ellos codifican para proteínas sarcoméricas.
Displasia Arritmogénica del Ventrículo Derecho
Es una enfermedad del corazón de herencia autosómica dominante, se caracteriza por la pérdida progresiva de miocitos, los cuales son reemplazados por tejido fibroadiposo. Si bien afecta al ventrículo derecho, también puede comprometer al ventrículo izquierdo.
Esta enfermedad se presenta con más frecuencia en los jóvenes, siendo en el 80 por ciento de los casos, personas menores de 40 años. Su diagnóstico clínico es difícil de realizar, tal es así que en muchas ocasiones la primera manifestación de la enfermedad es la muerte súbita, principalmente en personas menores de 30 años. Si bien su prevalencia aún no ha sido bien definida, se calcula de 0.1-1 de cada 1.000 individuos.
Se han identificado mutaciones en 6 genes, de los cuales 4 codifican proteínas del desmosoma. Ente ellos se encuentran la Desmocolina 2, Desmogleina 2, Plakofilina 2, Desmoplakina, receptor cardiaco de la Rianodina (RYR2) y TGFB3.
Cabe destacar que el 25 por ciento de los individuos con esta enfermedad presentan una mutación que afecta a la proteína Plakofilina 2.
Síndrome de Brugada
Es una enfermedad del corazón caracterizada por episodios de taquicardia ventricular polimórfica rápida. Estas pueden causar episodios de síncope (desmayo) o muerte súbita. Su herencia es autosómica dominante y presenta mayor incidencia en hombres (8:1).
El síndrome de Brugada es causa de muerte, principalmente de adultos jóvenes (menores de 50 años) que no presentan síntomas de enfermedad cardiaca previa. Se estima que entre un 4 por ciento y un 12 por ciento de las muertes súbitas se dan como consecuencia de este síndrome. Hasta ahora, sólo se ha identificado un gen relacionado con el síndrome, el SCN5.
Su prevalencia es difícil de determinar dado que no todas las presentaciones de la enfermedad son fáciles de identificar, pero se calcula en 5 de cada 10.000 individuos.
Síndrome de QT largo (SQTL)
Se conocen cuatro formas hereditarias de este síndrome, el síndrome de Romano-Ward (RWS), el síndrome de Andersen-Tawil, el síndrome de Thymothy y el síndrome de Jervell-Lange-Nielsen. El primero de ellos es el más común, presentándose con una prevalencia de 1 de cada 5.000 individuos y representando el 85 por ciento de todos los caso de SQTL. Los tres primeros son de herencia autosómica dominante, en tanto que el último es de herencia autosómica recesiva.
En todos los casos, la enfermedad se caracteriza por arritmias cardiacas, las cuales pueden evidenciarse en un electrocardiograma como un aumento del intervalo QT. Estas arritmias son consecuencia de anomalías estructurales en los canales de potasio y sodio del corazón. Los síntomas pueden aparecer en situaciones de estrés o bien por la toma de ciertos medicamentos. No obstante, en muchos casos los pacientes pueden permanecer asintomáticos durante toda su vida.
Se conocen al menos nueve genes que han sido asociados al desarrollo de esta enfermedad. Estos genes codifican proteínas que regulan el transporte de sodio, potasio o calcio a través de las membranas plasmáticas de las células cardiacas. Los genes KCNQ1, KCNH2, SCN5A, KCNE1, KCNE2 están asociados al Síndrome de Romano-Ward; el gen KCNJ2, al síndrome Andersen-Tawil; el gen CACNA1C, al síndrome de Timothy, y los genes KCNQ1 y KCNE1, al síndrome de Jervell-Lange-Nielsen.
Aproximadamente, entre el 60 y el 70 por ciento de los individuos con este síndrome poseen mutaciones en alguno de estos genes. No obstante, se ha identificado un nuevo gen, el ANK2, que codifica para la ankyrina B, la primera proteína que no está implicada con los canales iónicos.
Taquicardia Ventricular Polimórfica Catecolaminérgica
Es una enfermedad del corazón de carácter hereditario que se presenta en corazones estructuralmente normales. Se caracteriza por desencadenarse ante episodios de liberación de catecolaminas (hormonas producidas por las glándulas suprarrenales, entre ellas la noradrenalina y adrenalina) en situaciones de estrés físico o estrés emocional.
Usualmente, los síntomas aparecen entre los 5 y 10 años; sin embargo los casos de muerte súbita en este rango de edad son raros. Un 30 por ciento de los casos presentan historia familiar de síncope (desmayos) y muerte súbita. Su prevalencia, actualmente es desconocida, se estima en 1 de cada 2.000 individuos.
En la mayoría de los casos el patrón de herencia es autosómico dominante y se debe a una mutación en el gen que codifica para el receptor de la rianodina (RYR2). También existe un patrón de herencia autosómico recesivo, debido a mutaciones en el gen CASQ2, el cual codifica para la proteína calciquestrina.
Otros factores que podrían influir en su formación son la edad, el sexo (los hombres de avanzada edad tienen más posibilidades de sufrirla), el consumo de tabaco, obesidad, diabetes, subidas de tensión o unos niveles de colesterol LDL altos.
SÍNTOMAS
La muerte súbita cardíaca no tiene unos síntomas previos como tal, pero sí se pueden enumerar una serie de posibles factores que pueden influir en su aparición:
Que el sujeto haya experimentado un episodio de estas características anteriormente o que tenga familiares con antecedentes.
Insuficiencia cardiaca; es decir, que el corazón tenga dificultades para realizar sus funciones (o que le haya ocurrido esto previamente).
Haber sufrido un ataque cardíaco (infarto de miocardio)
Arritmias cardíacas (así como haberlas padecido en otra ocasión)
Que el porcentaje de sangre bombeada por el corazón en cada latido, denominada 'fracción de eyección', sea igual o inferior a un 40 por ciento.
¿QUÉ DEBEMOS HACER?
Sólo hay un tratamiento efectivo para frenar la muerte súbita cardíaca y es la desfibrilación precoz. Este procedimiento consiste en realizar una descarga eléctrica en el corazón, a través de unas palas o parches, con la que se pretende reiniciar la actividad eléctrica del corazón.
En el caso de no disponer de un desfibrilador a mano, o de no saber utilizarlo, se puede realizar una reanimación cardiopulmonar; consistente en el masaje cardíaco, combinando éste con la respiración boca a boca.
También existe la posibilidad de implantar un desfibrilador cuando se detecta, por ejemplo, un síndrome de Brugada.
MUERTE SÚBITA CARDÍACA EN DEPORTISTAS
Los deportistas, especialmente los gimnastas, los ciclistas y, sobre todo, los futbolistas, conforman un grupo de población que puede experimentar este episodio durante la práctica de la actividad física. El último caso sucedió hace una semana, cuando el futbolista de la liga italiana, Piermario Morosini, cayó fulminado en el campo de fútbol.
Aunque las noticias que más trascienden en los medios de comunicación suelen ser las relacionadas con deportistas profesionales, los expertos hacen énfasis en que todos, tanto federados como aficionados, deberían someterse a reconocimientos médicos específicos con asiduidad. Esto se debe, entre otras cosas, a que muchas de las muertes súbitas sucedidas en deportistas menores de 35 años, son causadas por malformaciones congénitas del corazón que podrían ser descubiertas con pruebas convencionales. Otro porcentaje mucho menor de estos eventos se produce por miocardiopatías, arritmias y otras causas, como fármacos.
En el caso de los mayores de 35 años, casi el 90 por ciento de las muertes súbitas son producidas por lesiones en las arterias coronarias causadas, en muchas ocasiones, por el consumo de tabaco o por un nivel alto de colesterol.
Así, realizar un examen, algo más exhaustivo en el caso de los deportistas federados, es fundamental para poder descubrir anomalías que puedan desembocar más tarde en una muerte súbita cardíaca. En esta valoración deberían incluirse: estudio de los antecedentes personales y familiares, un electrocardiograma y una ecocardiografía.
CONCLUSIONES:
Cuando acude un paciente a urgencias con una clínica no muy sugestiva de cardiopatía isquémica, electrocardiograma (ECG) sin cambios evidentes y con las enzimas y troponinas negativas, queda la duda si se trata de un evento isquémico o no.
Siempre debemos tener en cuenta los antecedentes del paciente, sus factores de riesgo cardiovascular, pero lo más importante, lo que se mostró en este paciente, un electrocardiograma no típico para su edad, paciente hipertenso. Siempre tendremos un electrocardiograma (ECG) peculiar, pues los años dejan sus huellas.
CONCLUSIONS
When a patient arrives to the Emergency Department with symptoms unlikely ischeamic heart disease, without EKG changes and anylises negatives always we must take on mind the common sense.
We must take care about pathological background, cardiovascular risk factors, but the most important, especially founded in this patient, the EKG not typical for the patient age. Our EKG changes even if we have not clinical symptoms of heart disease.
Referencias bibliográficas
1. Ades PA, Grunvald MH, Weiss RM, Hanson JS. Usefulness of myocardial ischemia as predictor of training effect in cardiac rehabilitation after acute myocardial infarction or coronary artery bypass grafting. Am J Cardiol. 1989;63:1032-1036.
2. Weber JR. Problems associated with clinical evaluation of antianginal medications. Am J Cardiol. 1985; 56:14I-18I.
3. Benson H, McCallie DP Jr. Angina pectoris and the placebo effect. N Engl J Med. 1979;300:1424-1429.
4. Spertus JA, Winder JA, Dewhurst TA, et al. Development and evaluation of the Seattle Angina Questionnaire: a new functional status measure for coronary artery disease. J Am Coll Cardiol. 1995;25:333-341.
5. Goldman L, Cook EF, Johnson PA, Brand DA, Rouan G, Lee TH. Prediction of the need for intensive care in patients who come to emergency departments with acute chest pain. N Engl J Med 1996;334:1498-504.
6. Holmvang L, Clemmensen P, Wagner G, Grande P, on behalf of the TRIM investigators. Admission standard electrocardiogram for early risk stratification in patients with unstable coronary artery disease not eligible for acute revascularization therapy: a TRIM substudy Thrombin Inhibition in Myocardial Infarction. Am Heart J 1999;137:24-33.
7. Cannon CP, McCabe CH, Stone PH, Rogers WJ, Schactman M, Thompson BW. The electrocardiogram predicts one-year outcome of patients with unstable angina and non-Q wave myocardial infarction: results of the TIMI III Registry ECG Ancillary Study Thrombolysis in Myocardial Ischemia. J Am Coll Cardiol 1997; 30:133-40.
8. Maynard SJ, Menown IB, Adgey AA. Troponin T or troponin I as cardiac markers in ischaemic heart disease. Heart 2000;83:371-3.
9. Zimmerman J, Fromm R, Meyer D, Boudreaux X, Wun CC, Smalling R, et al. Diagnostic marker cooperative study for the diagnosis of myocardial infarction. Circulation 1999;99:1671-6.
10. Christenson RH, Duh SH, Newby K, Ohman EM, Califf RM, Granger CR, et al. Cardiac troponin T and cardiac troponin I: relative value in short-term risk stratification of patients with acute coronary syndromes. Clin Chem 1998;44:494-501.
11. Arós F, Loma-Osorio A, Alonso A, Alonso JJ, Cabadés A, Coma I, et al. Guías de actuación clínica de la Sociedad Española de Cardiología en el infarto agudo de miocardio. Rev Esp Cardiol 1999;52:919-56.
12. Buxton AE, Fisher JD, Josephson ME, Lee KL, Pryor DB, Prystowsky EN et al. Prevention of sudden death in patients with coronary artery disease: the Multicenter Unsustained Tachycardia Trial (MUSTT). Prog Cardiovasc Dis 1993; 36: 215-226.
13. Goldberger JJ. Treatment and prevention of sudden cardiac death: effect of recent clinical trials. Arch Intern Med 1999; 159: 1281-1287.