La artroplastia de cadera tiene en la actualidad un bajo índice de complicaciones, sin embargo, la trombosis venosa profunda y el embolismo pulmonar constituyen un problema muy importante. Se estima que hasta un 80% de los pacientes pueden presentar trombosis venosa profunda que en la mayoría de los casos es asintomática y hasta un 20% pueden desarrollar tromboembolismo pulmonar.
Disnea súbita tras artroplastia de cadera.
Sudden breathlessness after hip arthroplasty.
Autor Principal
ME. Esteban Ciriano. Médico especialista en Anestesiología, Reanimación y Cuidados críticos. Hospital Reina Sofía, Tudela, Navarra, España.
Autores Colaboradores
S. Juan Belloc. Médico especialista en Pediatría. Hospital Reina Sofía, Tudela, Navarra, España.
S. Olagorta García. Médico especialista en Medicina Familiar y Comunitaria. Médico especialista en Anestesiología, Reanimación y Cuidados críticos. Hospital Reina Sofía, Tudela, Navarra, España.
R. Molina Luyando. Médico especialista en Medicina Familiar y Comunitaria. Hospital Reina Sofía, Tudela, Navarra, España.
RESUMEN
La artroplastia de cadera tiene en la actualidad un bajo índice de complicaciones, sin embargo, la trombosis venosa profunda y el embolismo pulmonar constituyen un problema muy importante. Se estima que hasta un 80% de los pacientes pueden presentar trombosis venosa profunda que en la mayoría de los casos es asintomática y hasta un 20% pueden desarrollar tromboembolismo pulmonar.
PALABRAS CLAVE: Tromboembolismo pulmonar, artroplastia de cadera.
SUMMARY
Hip Arthroplasty is currently a low index of complications, however, deep venous thrombosis and pulmonary embolism are a very important problem. It is estimated that up to 80% of patients may develop deep vein thrombosis which in most cases is asymptomatic and up to 20% may develop pulmonary embolism.
KEYWORDS: Pulmonary embolism, hip artroplasty.
INTRODUCCIÓN
El riesgo de trombosis venosa profunda y el riesgo de tromboembolismo pulmonar existe SIEMPRE en todos los pacientes intervenidos de artroplastia de cadera a pesar de las medidas de prevención utilizadas en todos los casos tal y como se refleja en este caso clínico.
Existen varios factores asociados a la formación de trombos como son: edad avanzada, obesidad, insuficiencia venosa periférica, tabaco, toma de anticonceptivos (alto contenido de estrógenos), historia previa de trombosis venosa profunda o embolismo pulmonar, proceso neoplásico y determinados factores genéticos.
Sin embargo, se conocen varios mecanismos patogénicos claves implicados en la formación de un trombo.
En primer lugar, se debe prestar atención a las alteraciones en la coagulación: el organismo ante cualquier agresión quirúrgica responde con una fase de hipercoagulabilidad con la formación de coágulos en el sistema venoso periférico. En segundo lugar, los largos periodos de encamamiento tras la intervención quirúrgica favorecen el éstasis venoso y finalmente se ha de tener en cuenta siempre el daño iatrogénico sobre el propio lecho vascular durante el acto quirúrgico (1).
Otros factores perioperatorios que favorecen la formación de un trombo son la necesidad de transfusión y el estado de hidratación del paciente.
La formación de un trombo dar lugar a dos entidades clínicas: la trombosis venosa profunda y el tromboembolismo pulmonar. El tromboembolismo pulmonar se desarrolla en el 90% de los casos en el sistema venoso de las extremidades inferiores (2).
Clínicamente, el embolismo pulmonar cursa de forma asintomática o bien como un embolismo masivo con muerte súbita dependiendo del estado previo del paciente así como de su reserva respiratoria.
El diagnóstico de tromboembolismo pulmonar (TEP) es difícil y requiere una historia clínica minuciosa, una exploración física adecuada y pruebas diagnosticas complementarias (3).
- Los síntomas clínicos más frecuentes del tromboembolismo pulmonar incluyen disnea, dolor pleurítico, tos, dolor y aumento del tamaño del miembro inferior, hemoptisis y taquipnea.
- Los signos clínicos son taquipnea, taquicardia, estertores, cuarto tono y refuerzo del componente pulmonar del segundo tono.
Los exámenes complementarios realizados de forma rutinaria engloban:
- Gasometría arterial: los valores de una gasometría arterial no son específicos de tromboembolismo pulmonar (TEP). Habitualmente estos pacientes presentan hipoxemia, hipocapnia con un gradiente A-a de oxigeno alterado. Una gasometría arterial normal nunca excluye el diagnóstico de tromboembolismo pulmonar (TEP).
- Electrocardiograma: alteraciones inespecíficas de la repolarización con ondas T negativas en derivaciones V1- V4.
- Radiografía de Tórax: Habitualmente se observa: cardiomegalia, derrame pleural, elevación del hemidiafragma, disminución de la vascularización pulmonar con aumento del tamaño de la arteria en el hilio.
- Dímero D: se caracteriza por su alta sensibilidad (98-100%) y su alto valor predictivo negativo (98-100%). Es muy útil para descartar el tromboembolismo pulmonar (TEP), pero no confirma el diagnóstico. Algunos estudios, teniendo en cuenta su alta sensibilidad y valor predictivo negativo concluyen que cuando los valores de dímero D sean inferiores a 500 μg/l, no es útil realizar más pruebas diagnósticas (4).
Las pruebas de imagen realizadas habitualmente son:
- Gammagrafía de perfusión: es útil como test de cribaje para descartar un tromboembolismo pulmonar (TEP).
- Eco-Doppler de miembros inferiores: un resultado normal no excluye el tromboembolismo pulmonar (TEP) si el nivel de sospecha es elevado.
- Ecocardiograma: ayuda en el diagnóstico diferencial pero no es una prueba diagnóstica.
- Angiografía pulmonar: Es la prueba de elección para el diagnóstico de tromboembolismo pulmonar (TEP).
- TAC con contraste: Prueba alternativa a la gammagrafía de ventilación- perfusión y a la angiografía. Presenta una sensibilidad del 75-100% para detección de émbolos en grandes arterias y arterias segmentarias pero no útil para detectar émbolos en arterias subsegmentarias, por lo tanto si la sospecha clínica es alta y el TAC es normal debe realizarse arteriografía dirigida a explorar el lecho vascular pulmonar distal.
- Angiorresonancia: permite ver la anatomía vascular pulmonar y la contractilidad del VD.
Un 10% de los pacientes diagnosticados de tromboembolismo pulmonar fallecen en las primeras horas a pesar del tratamiento, por lo tanto un diagnóstico preciso y un tratamiento adecuado son la clave del éxito. El objetivo principal es preservar un flujo sanguíneo adecuado evitando la extensión del coágulo y la recidiva de nuevos episodios mediante la administración inmediata de anticoagulantes (heparina).
Se administra Heparina Sódica por vía intravenosa (IV) mediante perfusión continua con bomba (4,8 mg/kg/24 horas), o intermitentemente (bolos de 1 mg/kg/4 horas).
Después del bolo inicial, suelen administrarse 1.000 U/h de heparina vía intravenosa (IV) ajustando la dosis de acuerdo con los resultados del TPT. Se consideran niveles terapéuticos las cifras 1,5 - 2 veces superiores a lo normal. La heparina se mantiene durante 7-10 días. La administración de anticoagulantes orales se inicia poco después que la de heparina, y se mantiene durante 3-6 meses (5).
El tratamiento trombolítico (urocinasa y estreptocinasa), se administra para disolver con rapidez el coágulo. Esta indicado en: Embolismo masivo, tromboembolismo pulmonar (TEP) severo con compromiso hemodinámico grave: síncope, hipotensión, hipoxemia o insuficiencia cardíaca y tromboembolismo pulmonar (TEP) reciente (primeras 24 horas de evolución).
La inserción de un filtro en la vena cava inferior está indicada si fuese necesario suspender el tratamiento anticoagulante o en el caso de presentar embolias recidivantes aún sometido a anticoagulación adecuada.
La embolectomía pulmonar está indicada en pacientes con inestabilidad hemodinámica.
CASO CLÍNICO
Mujer de 85 años de edad, sin alergias medicamentosas conocidas. Antecedentes médicos de hipertensión arterial (HTA) y enfermedad de Alzheimer avanzada.
Acude a urgencias por dolor en cadera derecha tras caída accidental. Tras las pruebas complementarias realizadas se objetiva fractura transcervical y trocantérea derecha.
Se decide tratamiento quirúrgico realizando una artroplastia de resección de cadera según procedimiento de Girldestone -Taylor, al no ser posible ningún tipo de osteosíntesis ni prótesis y teniendo en cuenta el estado previo de la paciente.
El postoperatorio curso sin incidencias y fue dada de alta con las siguientes recomendaciones:
- evitar encamamiento prolongado, mantener sedestación y bipedestación según tolerancia.
- realizar ejercicios de flexo-extensión de la extremidad intervenida lo antes posible.
- mantener la medicación habitual del paciente añadiendo tratamiento analgésico según grado de dolor.
- incorporar profilaxis antitrombótica mediante la administración de clexane 40 subcutánea/ 24 horas durante 10 días.
Tras 28 días de la intervención, la paciente acude a urgencias al presentar dificultad respiratoria con disnea de reposo.
En la exploración general se objetiva TA 180/90, frecuencia cardiaca rítmica 100l/m, saturación de oxigeno 90%, roncus y sibilantes aislados y extremidad derecha edematizada y empastada.
Las pruebas complementarias fueron las siguientes:
- analítica: hemograma y bioquímica sin alteraciones significativas.
- gasometría arterial: pH 7,49; pO2 62; pCO2 38.
- ECG: ritmo sinusal con imagen de BRDHH y patrón S1Q3T3.
- Rx Tórax: sin alteraciones de evolución aguda.
- Estudios de coagulación: Dímero D 15.994
- TAC Torácico: tromboembolismo pulmonar (TEP) submasivo.
Se traslada a la paciente a UCI con el diagnóstico de tromboembolismo pulmonar (TEP) masivo.�
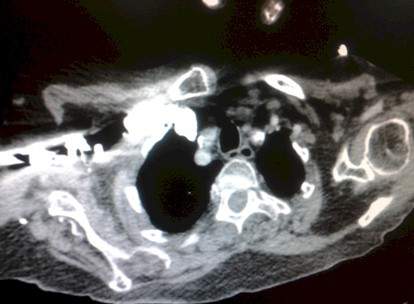
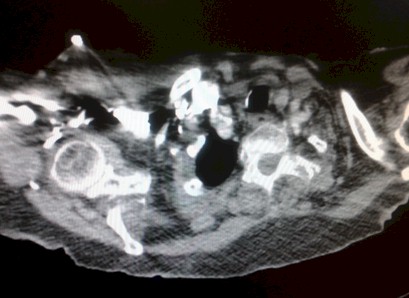
TAC Torácico
DISCUSIÓN
Se estima que durante los tres primeros meses tras una artroplastia de cadera existe el riesgo de desarrollar trombosis venosa profunda asintomática y posteriormente tromboembolismo pulmonar. El pico de mayor incidencia se produce entre el segundo y quinto día postoperatorio. Se ha descrito otro pico de incidencia alrededor de la segunda semana de la cirugía coincidiendo con el periodo de recuperación sin embargo está demostrado que los pacientes sometidos a un reemplazo total de cadera continúan estando en periodo de riesgo hasta 35 días después del acto quirúrgico (6).
Hasta un 80% de los pacientes pueden presentar trombosis venosa profunda tras una artroplastia de cadera siendo en la mayoría de los casos asintomáticos pero hasta un 20% pueden desarrollar tromboembolismo pulmonar. La tasa de mortalidad durante las primeras horas es aproximadamente del 70-90% (7).
Actualmente, existen medidas encaminadas a prevenir el desarrollo de estas complicaciones inherentes a la cirugía, pero hay que tener en cuenta que en determinados pacientes a pesar de llevar a cabo las medidas profilácticas adecuadas no están exentos de desarrollar estas complicaciones tal como acontece en el caso clínico descrito. La profilaxis se lleva a cabo mediante medidas físicas y tratamiento farmacológico.
Las medidas físicas van encaminadas a mejorar el flujo sanguíneo y favorecer la actividad fibrinolítica endógena. Una de las primeras medidas, es la movilización precoz del paciente encamado. Se utilizaran medias elásticas de compresión gradual u otros dispositivos similares como la compresión neumática intermitente (8). La compresión pasiva del paciente puede ser una alternativa pero no hay estudios que lo avalen.
Los métodos farmacológicos incluyen el uso de los siguientes fármacos:
- Heparina no fraccionada subcutánea (UFH): se suele utilizar a dosis bajas fijas vía subcutánea como profilaxis, sin embargo se ha demostrado mayor eficacia cuando se administra en dosis ajustada al peso, y ajustando la dosis al tiempo de tromboplastina parcial activada (TTPa), que debe ser entre uno y cinco segundos mayor que el control, lo que requiere un control más exhaustivo con varias inyecciones y control analítico diarios (9). Se utiliza a dosis bajas: 5.000 UI (de la sal sódica o de la cálcica) por vía s.c. cada 8 h (pacientes de riego elevado) o cada 12 h (para los de riesgo moderado). Se contraindica su uso en pacientes con antecedente de reacción alérgica, trombopenia o trombosis inducida por heparina, hemorragia activa y trastornos graves de la coagulación no corregidos (trombopenia, trombopatías y hemofilia). Sus principales efectos adversos son la hemorragia y la trombopenia.
- Heparina fraccionada de bajo peso molecular: se pautan por vía subcutánea cada 24 h. La primera dosis de heparina de bajo peso molecular puede iniciarse 12 h antes de la intervención y debe mantenerse durante al menos 7-10 días. Los pacientes de riesgo moderado reciben 20 mg al día en una inyección vía subcutánea (SC) única y los de riesgo elevado 40 mg al día en una inyección vía subcutánea (SC) única. Estas heparinas tienen las mismas contraindicaciones y efectos secundarios que la heparina no fraccionada. Existen medicamentos que potencian el efecto anticoagulante de las hepáticas de bajo peso molecular como los antiinflamatorios no esteroideos, el acido acetilsalicílico, corticoides y antagonistas de vitamina K (10).
- El uso de anticoagulantes orales solo se planteara en casos de hipersensibilidad a la heparina. La eficacia de los antiagregantes plaquetarios es inferior a la de la heparina y los anticoagulantes. Se usaran en caso de contraindicación de los anticoagulantes.
Tras muchos estudios, se ha concluido que la profilaxis únicamente intrahospitalaria es insuficiente. La duda se plantea sobre el tiempo que debe mantenerse la profilaxis tromboembólica. Lo más recomendable es mantener la profilaxis hasta la movilización activa del paciente, periodo tras lo cual desaparecen los factores desencadenantes del riesgo tromboembólico. En la actualidad, se tiende a mantener la profilaxis hasta cinco semanas después de la intervención. Sin embargo, el mantenimiento de la profilaxis dependerá de la situación personal del paciente (11).
BIBLIOGRAFÍA
1. Kakkar Ak. Prevention of venous thromboembolism in general surgery. In: Colman RW, Clowes AW, George JN, Goldhaber SZ, Marder VJ, eds. Hemostasis and Thrombosis: Basic Principles and Clinical Practice. 5th ed. Philadelphia, PA: Lippincott, Williams & Wilkins; 2006:1361-1367.
2. Kakkar VV, Howe CT, Flanc C, Clarke MB. Natural history of postoperative deep vein thrombosis. Lancet 1969; 2: 230-232.
3. Stein PD, Terrin ML, Hales CA, Palevsky HI, Saltzman HA, Thompson BT et al. Clinical, laboratory, roentgenographic and electrocardiographic findings in patients with acute pulmonary embolism and no pre-existing cardiac or pulmonary disease. Chest 1991; 100: 598-603.
4. Bounameaux H, De Moerloose P, Perrier A, Miron MJ. D-dimer testing in suspected venous tromboembolism: an update. QJM 1997; 90: 437-442.
5. Hirsh J. Hoak, j., Management of Deep Vein Thrombosis and Pulmonary Emboslism, Circulation, 1996: 93: 2212-2245.
6. Planes A, Vochelle N, Darmon JY, Fagola M, Bellaud M, Huet Y. Risk of deep-venous thrombosis after hospital discharge in patients having undergone total hip replacement: double-blind randomised comparison of enoxaparin versus placebo. Lancet. 1996;348(9022):224-228.
7. Carson JL, Kelley MA, Duff A, Weg JA, Fulkerson WJ, Palevsky HI et al. The
8. clinical course of pulmonary embolism. N Engl J Med 1992; 326: 1240-1245.
9. Best, A; Williams, S, y Gregg, PJ, et al: Graded compression stockings in lower limb arthroplasty. (Comunicación Congreso EFORT 1999, Bruselas). J Bone Joint Surg Br, 81-B(supp II): 210, 1999.
10. Leyvraz, PF; Richard, J; Bachmann, F; Van Melle, G; Treyvaud, JM; Livio, JJ, y Candardjis, G: Adjusted versus fixed-dose sub-cutaneous heparin in the prevention of deep-vein thrombosis after total hip replacement. N Engl J Med, 309: 954-958, 1983.
11. Geerts, WH; Jay, RM; Code, KI; Chen, E; Szalai, JP; Saibil, EA, y Hamilton, PA: A comparison of low-dose heparin with low-molecular-weight heparin as prophylaxis against venous thromboembolism after major trauma. N Engl J Med, 335: 701-707, 1996.
12. Dahl, OE; Andreassen, G; Aspelin, T; Muller, C; Mathiesen, P; Nyhus, S; Abdelnoor, M; Solhaug, JH, y Arnesen, H: Prolonged thromboprophylaxis following hip replacement surgery. Results of a double-blind, prospective, randomised, placebo-controlled study with Dalteparin (Fragmin). Thromb Haemost, 77: 26-31, 1997.