Estudio de sensibilidad in vitro de Pseudomonas aeruginosa frente a carbapenemes en pacientes oncológicos
El objetivo del estudio ha sido valorar la sensibilidad in vitro de Pseudomonas aeruginosa frente a imipenem, meropenem y doripenem en una serie de treinta y ocho pacientes oncológicos.
Study of in vitro susceptibility of Pseudomonas aeruginosa against carbapenems in cancer patients.
Tomás García Lozano (1), Eduardo Aznar Oroval (1), Pilar Pérez Ballestero (1), Marina Sánchez Yepes (1), Blanca Amparo Ortiz Muñoz (1)
(1) Servicio de Análisis Clínicos y Microbiología, Fundación Instituto Valenciano de Oncología (FIVO), Valencia, España
Palabras clave: Pseudomonas aeruginosa, carbapenemes, pacientes oncológicos
Key words: Pseudomonas aeruginosa, carbapenems, cancer patients
Resumen: Los carbapenemes son antibióticos ampliamente utilizados en multitud de infecciones. El aislamiento de Pseudomonas aeruginosa en el paciente oncológico tiene gran repercusión clínica. El objetivo del estudio ha sido valorar la sensibilidad in vitro de Pseudomonas aeruginosa frente a imipenem, meropenem y doripenem en una serie de treinta y ocho pacientes oncológicos.
En nuestra serie, se objetivan diferencias estadísticamente significativas (p<0.05), donde meropenem es superior in vitro a imipenem y doripenem en aislados de Pseudomonas aeruginosa.
Abstract: the carbapenems are antibiotics widely used in multitude of infections. The detection of Pseudomonas aeruginosa has a great clinical impact in the output of cancer patients. The aim of this study is evaluate the sensibility in vitro of Pseudomonas aeruginosa to imipenem, meropenem and doripenem in thirty-eight cancer patients.
We observed stadistical differences between meropenem, imipenem and doripenem in isolated of Pseudomonas aeruginosa.
Texto:
Los carbapenemes son antibióticos ampliamente utilizados en infecciones por bacilos gramnegativos, cocos grampositivos y enterobacterias multirresistentes. La decisión del uso de meropenem, imipenem o doripenem depende muchas veces del centro y/o de los protocolos aplicados en determinados cuadros clínicos.
La mayoría de los estudios han documentado que el tratamiento con carbapenemes reduce la mortalidad atribuible por infecciones (1,2,3).
El aislamiento de Pseudomonas aeruginosa en pacientes oncológicos tiene gran relevancia clínica y entre las múltiples razones, se debe principalmente a la resistencia intrínseca a determinados antibióticos y a la gran capacidad de adquisición de mecanismos de resistencia. La presencia de aislamientos por Pseudomonas aeruginosa productoras de metalo-beta-carbapenemasas (MBL) pueden suponer un serio problema en el paciente oncológico.
El uso masivo de determinados grupos de antimicrobianos induce a resistencias y generan, en determinados “microambientes” hospitalarios, serios problemas de endemicidad (4,5,6,7).
El objetivo de nuestro estudio ha sido valorar la sensibilidad in vitro, mediante la determinación de halos de inhibición, de Pseudomonas aeruginosa no productoras de carbapenemasas frente a imipenem, meropenem y doripenem en aislados procedentes de pacientes oncológicos desde diciembre de 2009 hasta mayo de 2010.
Realizamos un estudio prospectivo de 38 aislamientos por Pseudomonas aeruginosa de 38 pacientes distintos y de múltiples localizaciones (16 orinas, 9 esputos, 6 exudados de herida, 3 bronco-aspirados, 2 hemocultivos, 1 port-a-cath y 1 tubo endotraqueal), cuyo objetivo fue determinar los halos de inhibición en milímetros (mm) de imipenem, meropenem y doripenem (Oxoid,10 µg) mediante el método de difusión Kirby-Bauer con disco-placa en Mueller-Hinton (Becton Dickinson®) a 37º C y lectura a las 24 horas, según puntos de corte y recomendaciones de la CLSI (Clinical and Laboratory Standards Institute). No se estudiaron las cepas resistentes a carbapenemes o aquellas cepas con lecturas erróneas. El análisis estadístico se efectuó con el programa SPSS, versión 15. Se aplicaron test no paramétricos (Friedman y Wilcoxon) y los resultados se consideraron estadísticamente significativos con una p<0.05.
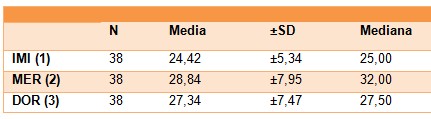
Tras medir los halos de inhibición de un total de 38 Pseudomonas aeruginosa (N=38, Sensibles a IMI ≥ 16 mm, MER ≥ 16 mm, DOR ≥ 17 mm, según las normas de la CLSI (Clinical and Laboratory Standards Institute)) se obtuvieron los siguientes datos expresados en los valores: media, desviación estándar y mediana (Tabla 1).
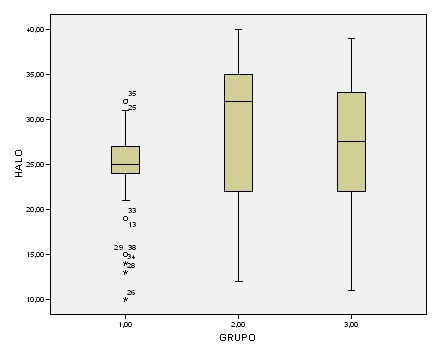
Al comparar los grupos entre sí, se encontraron diferencias estadísticamente significativas (p<0,0001, IC 95%, meropenem>imipenem/doripenem, test Friedman). También al comparar meropenem frente a imipenem (p<0,0001, IC 95%, meropenem>imipenem, test Wilcoxon) y meropenem frente a doripenem (p=0,001, IC 95%, meropenem>doripenem, test de Wilcoxon). Figura 1 (tablas blox-plot).
La mayoría de los estudios (COMPACT en Europa/España y TRUST en EEUU) objetivan superioridad de la actividad in vitro de doripenem con respecto a imipenem y meropenem en el tratamiento de infecciones por Pseudomonas aeruginosa y enterobacterias productoras de beta-lactamasas (BLEE y AmpC) (8,9).
Aunque nuestro estudio tiene ciertas limitaciones y admitiendo la comodidad de administración que doripenem ofrece, no parece aportar grandes ventajas con respecto a meropenem e imipenem en cuanto a inhibición del crecimiento bacteriano in vitro frente a Pseudomonas aeruginosa. Según nuestros resultados, meropenem es superior in vitro a imipenem y doripenem en aislados de Pseudomonas aeruginosa. Por ello meropenem sigue siendo una alternativa clara de tratamiento frente a enterobacterias y Pseudomonas aeruginosa.
Tabla 1. Estadísticos descriptivos. IMI (1) (imipenem), MER (2) (meropenem), DOR (3) (doripenem).
Figura 1: tables blox-plot.
1 (imipenem), 2 (meropenem) y 3 (doripenem)
Pruebas de normalidad
a Corrección de la significación de Lilliefors
Bibliografía
1- Kollef MH. Appropriate empiric antimicrobial therapy of nosocomial pneumonia: the role of the carbapenems. Respir Care. 2004;49:1530-41
2- Micek ST, Lloyd AE, Ritchie DJ, Reichley RM, Fraser VJ, Kollef MH. Pseudomonas aeruginosa bloodstream infection: importance of appropriate initial antimicrobial treatment. Antimicrob Agents Chemother. 2005; 45:1306-11.
3- van Delden C. Pseudomonas aeruginosa bloodstream infections: how should we treta them? Int J Antimicrob Agents 2007;30;S71-5.
4- García ramírez D, Nicola F, Arduino S, Relloso S, Amayevsky J. Fenotipos de resistencia a beta-lactámicos en aislamientos de Pseudomonas aeruginosa de pacientes internados. IX Congreso Argentino de la Sociedad Argentina de Infectología. 2009, Resumen 24838.
5- Hsueh P, Chen W, Luh K. relationships between antimicrobial use and antimicrobial resistance in Gram-negative bacteria causing nosocomial infections from 1991-2003 at a university hospital in Taiwan. Int J Antimicrob Agents. 2005 ;26 :463-72
6- Patzer JA, Dzierzanowska D. Increase of imipenem resistance among Pseudomonas aeruginosa isolates from a Polish paediatric hospital (1993-2002). Int J Antimicrob Agents. 2007 ;29 :153-8.
7- Zavascki AP, Cruz RP, Goldani LZ. Risk factors for imipenem-resistant Pseudomonas aeruginosa: a comparative análisis of two case-control studies in hospitalized patients. J Hosp Infect. 2005;59:96-101.
8- Nicola F, García Ramírez D, Arduino S, Di Chiara M, Smayevsky J. Actividad comparativa in vitro de doripenem y de otros carbapenemes frente a Pseudomonas aeruginosa. Rev Argent Microbiol. 2010 ;42 :193-198.
9- Gimeno C, Cantón R, García A, Gobernado M y Grupo Español de Estudio de Doripenem. Actividad comparativa de doripenem, meropenm e imipenem en asilados recientes obtenidos durante el estudio de vigilancia epidemiológica COMPACT-España. Rev Esp Quimioter. 2010 ;23 :144-152.