Bajo el término de TEP se incluye un amplio espectro de situaciones que van desde casos clínicos poco significativos hasta embolismos pulmonares masivos con muerte súbita. Es difícil conocer la incidencia real del TEP, debido en gran parte al problema de infradiagnóstico clínico; tan solo el 10-25% de las embolias demostradas por estudios anatomo-patológicos son correctamente diagnosticadas en vida.
Dr. Gerardo Álvarez Álvarez. Dr. Elvys Pérez Bada.
RESUMEN
Bajo el término de Tromboembolismo pulmonar se incluye un amplio espectro de situaciones que van desde casos clínicos poco significativos hasta embolismos pulmonares masivos con muerte súbita. Es difícil conocer la incidencia real del Tromboembolismo pulmonar, debido en gran parte al problema de infradiagnóstico clínico; tan solo el 10-25% de las embolias demostradas por estudios anatomo-patológicos son correctamente diagnosticadas en vida. La incidencia del Tromboembolismo pulmonar es mayor en varones, aumenta con la edad y es más frecuente en el ámbito hospitalario El tromboembolismo pulmonar es una complicación frecuente y se estima que el 4 % de todas las causas de muertes hospitalarias pueden atribuirse a la embolia pulmonar; que de no ser tratada puede alcanzar una mortalidad del 38 %. Se realizó un estudio observacional descriptivo mediante la revisión de los protocolos de necropsias de fallecidos por Tromboembolismo pulmonar del año 2006 y se centra en el estudio de las historias clínicas de 13 fallecidos por tromboembolismo pulmonar en el Servicio de Medicina Interna del Hospital provincial de Villa Clara Arnaldo Milian Castro. Se valoraron las variables edad, sexo, manifestaciones clínicas, ramas vasculares afectadas, enfermedades asociadas, diagnóstico.
Los anticoagulantes constituyen la piedra fundamental en el manejo de un grupo de enfermedades que tienen una elevada morbilidad y mortalidad en el paciente grave y cierto grupo de pacientes como aquellos con secuelas paralíticas de la enfermedad cerebro-vascular o con infarto agudo del miocardio, en quienes la incidencia de tromboembolismo venoso se estima entre 30% y 75%, se recomienda el uso de heparina profiláctica. Se revisan los esquemas de tratamiento anticoagulante, terapéuticos o profilácticos: bolo de entrada o dosis de ataque, modo de administración de la heparina, anticoagulación oral, días de tratamiento anticoagulante, exámenes de laboratorio y heparinas de bajo peso molecular. Se expone un esquema de tratamiento anticoagulante en el paciente grave conformado por la administración de heparina no fraccionada o convencional de inicio, y se mantiene entre 7 y 10 días, de acuerdo con la evolución del paciente. El seguimiento de laboratorio se realiza con el Tiempo Parcial de Tromboplastina activado. La administración de anticoagulantes orales se inicia entre el segundo y el tercer día del tratamiento, preferiblemente con warfarina: 10 miligramos, que adecuaríamos según los resultados del INR. Los niveles de anticoagulación se alcanzan alrededor del quinto día de tratamiento y permiten la reducción de la dosis de heparina no fraccionada. Con referencia a la profilaxis mediante el uso de anti coagulación se propone las heparinas de bajo peso molecular o la heparina no fraccionada a dosis de 5 000 Unidades cada 8 a 12 horas. TROMBOEMBOLISMO PULMONAR
INTRODUCCIÓN
La enfermedad tromboembólica venosa es una enfermedad frecuente, potencialmente mortal y en muchas ocasiones infradiagnosticada. Este término incluye tanto la trombosis venosa profunda (trombosis venosa profunda) como el tromboembolismo pulmonar entidades que están íntimamente relacionadas y deberían considerarse como parte de un mismo proceso patológico. Los estados de hipercoagulabilidad conducen a la formación de trombos en las venas de miembros inferiores y éstos pueden tener extensión proximal. Una vez formado el coágulo en el sistema venoso profundo de las extremidades inferiores, pelvis o miembros superiores, puede disgregarse y embolizar a los pulmones. El Tromboembolismo pulmonar consiste en la migración hacia un territorio vascular pulmonar de un trombo formado en el sistema venoso, con oclusión de las arterias pulmonares por un émbolo procedente, en la mayoría de los casos (95%), del sistema venoso profundo de las extremidades inferiores (grandes venas proximales) y en menor frecuencia de las pélvicas. Otros orígenes pueden ser: vena cava, cavidades cardíacas derechas, aurícula izquierda (fibrilación auricular), válvulas cardíacas (endocarditis), ventrículo derecho (necrosis) y miembros superiores. Son poco frecuentes los émbolos formados por tumores, aire, fibrina, líquido amniótico, medula ósea y cuerpos extraños.
Cada vez se tiende más a utilizar el término de enfermedad tromboembólica venosa (ETV), que engloba la trombosis venosa profunda y su consecuencia más grave el Tromboembolismo pulmonar. El Tromboembolismo pulmonar es un problema de salud muy importante ya que:
• Es la tercera causa de muerte en hospitales
• Tiene una incidencia de10 casos/100.000 habitantes y una prevalencia en hospitalizados del 1%
• Sin tratamiento tiene una mortalidad del 30%
• Es de difícil diagnóstico, sólo el 30% de los Tromboembolismo pulmonar con un mal desenlace se diagnostican en vida. Algunos autores indican que solo del 10-25%.
• La complicación más grave del Tromboembolismo pulmonar a largo plazo es la hipertensión pulmonar.
El 40% de los pacientes con trombosis venosa profunda sin síntomas clínicos sugestivos de embolia pulmonar presentan evidencia de Tromboembolismo pulmonar en las pruebas de imagen; por otra parte, pueden demostrarse alteraciones vasculares de miembros inferiores en el 30% de los pacientes con Tromboembolismo pulmonar.
Bajo el término de Tromboembolismo pulmonar se incluye un amplio espectro de situaciones que van desde casos clínicos poco significativos hasta embolismos pulmonares masivos con muerte súbita. Es difícil conocer la incidencia real del Tromboembolismo pulmonar, debido en gran parte al problema de infradiagnóstico clínico; tan solo el 10-25% de las embolias demostradas por estudios anatomo-patológicos son correctamente diagnosticadas en vida. La incidencia del Tromboembolismo pulmonar es mayor en varones, aumenta con la edad y es más frecuente en el ámbito hospitalario. En casos de trombosis venosa diagnosticada, la frecuencia de Tromboembolismo pulmonar oscila entre el 50 y el 79%, si se incluyen en el diagnóstico los casos de trombos microscópicos. Estudios recientes demuestran una mortalidad en torno al 15-20%. El conocimiento de la elevada frecuencia de embolismo pulmonar en pacientes con trombosis venosa profunda puede contribuir a mejorar el diagnóstico del Tromboembolismo pulmonar. Todos estos aspectos han sido recientemente revisados.
FACTORES DE RIESGO
El conocimiento de los factores de riesgo asociados con estados de hipercoagulabilidad es crucial tanto para la identificación y estratificación de los diferentes grupos de riesgo como en lo referente a las decisiones terapéuticas y la profilaxis antitrombótica. La formación del trombo está favorecida en presencia de la clásica triada de Virchow: éxtasis venoso, alteraciones de la pared vascular e hipercoagulabilidad. Los factores de riesgo más importantes son:
• Infarto de miocardio, insuficiencia cardíaca congestiva e insuficiencia venosa crónica.
• Lesión por traumatismo, sobre todo fractura de miembros inferiores y huesos largos.
• Anticonceptivos y terapia estrogénica.
• Edad > 40 años.
• Inmovilización prolongada > 4 días aproximadamente.
• Neoplasias con compresión del sistema venoso profundo y liberación de sustancias procoagulantes.
• Estados de hipercoagulabilidad primaria.
• Accidentes cerebrovasculares.
• Parto y puerperio.
• Antecedentes de Tromboembolismo pulmonar y trombosis venosa profunda.
• Cirugía ortopédica, abdominal y neurológica.
La coincidencia de diversos factores de riesgo incrementan la predisposición de embolia. El 40% de los Tromboembolismo pulmonar no tienen un factor de riesgo conocido, son de causa primaria.
Estudios recientes han confirmado la influencia de algunos de estos factores; así, los pacientes con neoplasias, debido en parte a la capacidad de las células neoplásicas de generar trombina y otras sustancias procoagulantes, presentan un riesgo de enfermedad tromboembólica recurrente y mortal tres veces superior al que presentan los pacientes con trombosis venosa profunda/Tromboembolismo pulmonar sin neoplasia subyacente 5. El tabaquismo y la obesidad han demostrado ser factores de riesgo independientes para el desarrollo de enfermedad tromboembólica 6. En un estudio reciente se ha sugerido que la incidencia de tromboembolismo venoso durante el embarazo es menor que lo que se ha descrito en trabajos previos, mostrando una mayor incidencia de trombosis venosa profunda en el periodo previo al parto, siendo los casos de Tromboembolismo pulmonar más frecuentes en el periodo posparto, especialmente en casos de cesárea 7. En cuanto a los tratamientos con anticonceptivos orales, se sabe que las fórmulas de segunda generación junto con estrógenos a dosis bajas aumentan el riesgo de trombosis venosa de 2 a 3 veces. En cualquier caso, el momento de mayor riesgo parece estar restringido al primer año de administración 10. Aunque tradicionalmente se ha considerado que la tromboflebitis superficial apenas plantea riesgo de embolización, un reciente estudio muestra que los pacientes con tromboflebitis superficial en las venas proximales de las extremidades inferiores presentan tasas de embolismo pulmonar inesperadamente elevadas, sugierendo que estos procesos no son tan benignos como se habían descrito previamente 8.
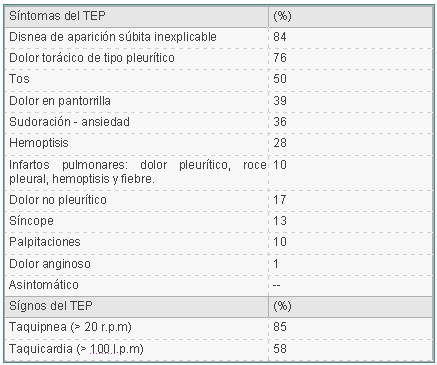
SINTOMAS Y SIGNOS
. Síntomas y signos clínicos Los síntomas son inespecíficos, su intensidad depende del grado de oclusión del lecho vascular pulmonar y de la reserva cardiorrespiratoria previa del paciente. El diagnóstico de la enfermedad se ve favorecido en la medida en la que se mantiene un nivel de sospecha. La hipotensión es el indicador pronóstico más importante.

DIAGNOSTICO
El diagnóstico y el tratamiento del embolismo pulmonar requiere un abordaje interdisciplinario, combinando aspectos médicos, quirúrgicos y radiológicos. La detección precisa del embolismo pulmonar continúa siendo difícil, y son numerosas las entidades con las que debe hacerse un diagnóstico diferencial. El sobre diagnóstico es un problema tan importante y frecuente como el infradiagnóstico, ya que el tratamiento antitrombótico no está exento de riesgos, por lo que es necesario realizar un diagnóstico lo más exacto posible. La estrategia diagnóstica más apropiada viene determinada por un estudio integrado que incluya una historia clínica y exploración física minuciosas, combinando las pruebas diagnósticas específicas cuando sea necesario. Es importante considerar el EP y la trombosis venosa profunda previa como una sola entidad clínica, y de esta forma, el diagnóstico de cualquiera de sus componentes establece la indicación terapéutica. Son numerosos los trabajos recientes que revisan la utilidad de las técnicas disponibles en la actualidad, así como su sensibilidad y especificidad, proporcionando algoritmos diagnósticos para los diferentes grupos de riesgo. Lo primero es tener una sospecha clínica, a partir de un cuadro clínico compatible, la presencia de factores de riesgo conocidos y las pruebas complementarias básicas. El primer paso es hace el cálculo de la probabilidad pretest, este cálculo se realizará con criterios explícitos que están disponibles en diferentes protocolos, a continuación se presenta el más conocido.

• Probabilidad clínica baja <2 puntos. Probabilidad de Tromboembolismo pulmonar de 10%, ocurre de 40% a 49% de pacientes.
• Probabilidad clínica moderada 2-6 puntos. Probabilidad de Tromboembolismo pulmonar de 20% a 40%, ocurre en el 50%
• Probabilidad clínica alta >6 puntos. Probalidad de Tromboembolismo pulmonar del 65%, ocurre en el 6% al 7%
• Probabilidad clínica baja con un resultado negativo de dímero D: permite excluir el Tromboembolismo pulmonar con un grado muy alto de fiabilidad (valor predictivo negativo: 99%).
• Probabilidad clínica intermedia o alta o el dímero D es positivo se hace TAC helicoidal o gammagrafía y se procederá como indica el algoritmo.
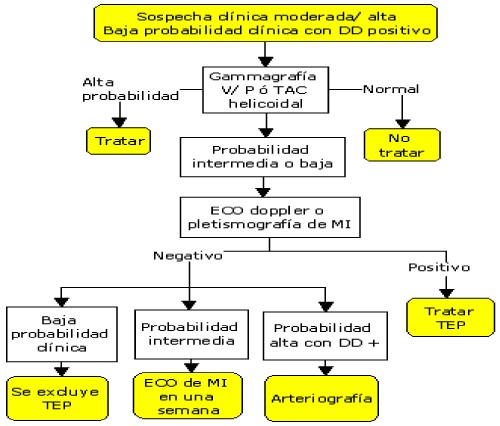
Algoritmo diagnóstico de Tromboembolismo pulmonar estableĀ
Ā
Algoritmo diagnóstico de Tromboembolismo pulmonar inestable
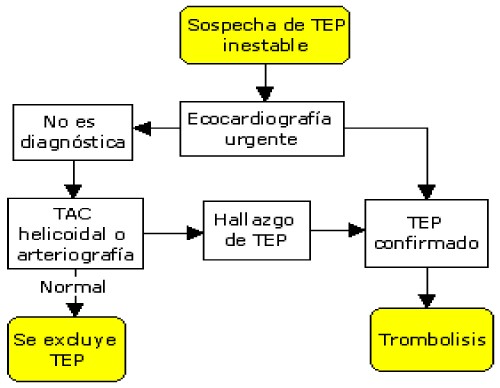
Las pruebas complementarias básicas: laboratorio, electrocardiograma y radiografía de tórax son útiles para descartar otros diagnósticos y valorar la gravedad del proceso.
1.- ECG. En el que podemos encontrar:
• Inversión de la onda T en derivaciones precordiales derechas.
• Taquicardia sinusal.
• Bloqueo de rama derecha.
• Arritmias supraventriculares.
• Trastornos de la conducción.
• Clásico patrón S1 Q3 T3 que es raro e indicativo de hipertensión pulmonar.
2.- Pruebas de laboratorio:
• Leucocitosis moderada con desviación a la izquierda.
• Aumento de productos de degradación del fibrinógeno.
• Aumento del dimero-D en plasma.
• Aumento de la LDH.
• Gasometría arterial: hipoxemia con hipocapnia y alcalosis respiratoria (30% de los casos la PO2 es normal). Aumento de la diferencia alveolo-arterial de O2.
El dímero-D se presenta en sangre tras la existencia de fibrinolisis, sirve como marcador de la presencia de trombos endovasculares.
3.- Radiografía de tórax.
Lo más frecuente en la embolia pulmonar es una radiografía de tórax normal. Las alteraciones radiológicas en el embolismo pulmonar se clasifican en:
• Embolismo sin infarto
o Signo de Westermark: son áreas de mayor claridad pulmonar que se deben a la oligohemia distal al vaso ocluido.
o Signo de Fleischer: es una dilatación de un segmento de la arteria pulmonar en el lugar dónde se enclava el émbolo con terminación brusca del vaso “signo de la salchicha” por vasoconstricción distal.
o Pérdida del volumen del pulmón con elevación del diafragma.
o Atelectasias laminares que aparecen en el 50% de los casos.
• Embolismo con infarto:
o Consolidación multifocal de predominio inferior, es visible entre las 12-24 horas de episodio embólico.
o Joroba de Hampton: opacidad triangular de base pleural y vértice hacia el hilio, es poco frecuente.
o Embolismo séptico: presenta muchas opacidades redondeadas o en cuña, periféricas y mal definidas.
o Embolismo graso: son infiltrados alveolares difusos y bilaterales similar a un edema agudo de pulmón que aparecen entre las 12-72 horas tras el traumatismo.
4.- Pruebas de confirmación.
• Gammagrafía pulmonar de perfusión:
o Tiene un gran valor en el diagnóstico de la embolia pulmonar
o Hasta ahora era la primera exploración no invasiva que debía hacerse ante la sospecha de Tromboembolismo pulmonar
o Inconvenientes: no está disponible en muchos centros y necesita el traslado del enfermo, no es diagnóstica en un 38% de los casos
o Una gammagrafía de perfusión normal, excluye Tromboembolismo pulmonar clínicamente significativo
o En caso de que sea anormal es necesario completar el estudio con una gammagrafía de ventilación Xe133
o Ventajas: es un método no invasivo, rápido, asequible, sencillo de realizar, con alta sensibilidad y útil para el diagnóstico de Tromboembolismo pulmonar
• TAC Helicoidal de tórax
o Ventajas: Elevada sensibilidad y especificidad para detectar trombos en las arterias centrales y segmentarias, no tiene riesgos.
o Inconvenientes: no es capaz de diagnosticar Tromboembolismo pulmonar periféricos y no está disponible en todos los hospitales.
o Puede ser que con el tiempo vaya desplazando a la gammagrafía.
Las imágenes se obtienen por gamma cámara en 6-8 proyecciones. La imagen normal es una distribución homogénea de la actividad radioactiva en todas la proyecciones, cuando hay una obstrucción de un vaso, no hay proyección distal de las micro partículas, lo que provoca una ausencia de radioactividad en todo el territorio prefundido por el mismo como se puede apreciar en ésta gammagrafía.
• Arteriografía
o Sensibilidad y especificidad del 99%.
o Es la prueba definitiva y de referencia.
o Es una técnica cruenta, con morbimortalidad, precisa de infraestructura compleja no siempre disponible.
o Se indica en los casos poco claros, en los que se necesita diagnóstico de certeza y en situaciones de extrema urgencia.
• Eco cardiografía
o No tiene riesgos y se puede hacer en la cabecera del enfermo.
o Exploración inicial de elección en Tromboembolismo pulmonar inestables.
o Inconvenientes: en Tromboembolismo pulmonar menores su sensibilidad es muy baja.
Tromboembolismo pulmonar inestables se hace Eco cardiografía aunque si hay signos de Tromboembolismo pulmonar y el enfermo está muy grave se puede hacer el tratamiento trombolítico sin hacer otras exploraciones.
¿Para qué sirve el dimero-D en el diagnóstico del Tromboembolismo pulmonar?:
• El dímero D es muy poco específico para diagnosticar el Tromboembolismo pulmonar porque también se puede elevar en otras enfermedades como son: IAM, ACVA, neoplasias, infecciones pulmonares, cirugía, hiperbilirrubinemia, traumatismos, edad avanzada, embarazo, hipertensión, raza negra y enfermedades inflamatorias.
• El dímero D tiene una gran sensibilidad y un alto valor predictivo negativo (tiene un gran valor para excluir el diagnóstico, aunque nunca de forma aislada, siempre debemos asociarlo a la sospecha clínica). Así si el valor del dímero-D es < 500 ng/ml y la sospecha clínica es baja nos permitiría excluir el diagnóstico de Tromboembolismo pulmonar y no sería necesario realizar otras pruebas complementarias.
• El dímero-D no se acepta aisladamente para excluir el Tromboembolismo pulmonar, siempre hay que relacionarlo con la sospecha clínica y otras pruebas diagnósticas.
Debemos hacer un diagnóstico diferencial de Tromboembolismo pulmonar con:
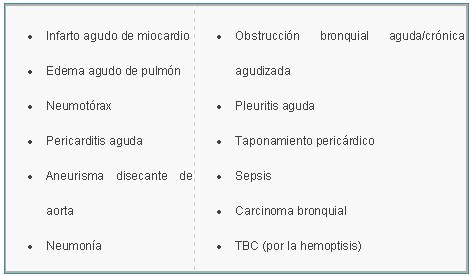
TRATAMIENTO
El objetivo principal del tratamiento del embolismo pulmonar es evitar la extensión y recidiva del proceso tromboembólico, así como reducir las consecuencias vasculares y hemodinámicas a largo plazo. El empleo de anticoagulantes junto a las medidas de soporte (reposo, oxigenoterapia, analgesia, control hemodinámico…) constituye la base del tratamiento del Tromboembolismo pulmonar . La rapidez de instauración del tratamiento es importante, sobre todo para evitar Tromboembolismo pulmonar de repetición, que son la causa fundamental de muerte en esta enfermedad. El 90% de las muertes por Tromboembolismo pulmonar se establecen en un periodo de 1-2 horas, antes de establecer el diagnóstico y el tratamiento.
Cuando hay una alta sospecha de Tromboembolismo pulmonar o está confirmado el diagnóstico, el tratamiento se comienza habitualmente con heparina no fraccionada i.v. a continuación se introducen anticoagulantes orales, superponiendo ambos tratamientos durante 4-5 días. Hay estudios recientes que demuestran que la tinzaparina subcutánea tiene la misma seguridad y eficacia que la heparina no fraccionada.
Medidas generales:
1. Toma de constantes (TA, frecuencia cardiaca y respiratoria, temperatura )
2. Canalizar una vía.
3. EKG y RX.
4. Oxigeno con Ventimask al 50%.
5. Analgesia: bolo de cloruro mórfico 10 mg i.v. que se puede repetir cada 4-6 horas (Se prepara diluyendo 1 ampolla en 9ml de suero fisiológico, razón de 2 ml/ minuto).
6. Tratamiento del shock obstructivo.
Medidas específicas
1. Heparina sódica I.V.: La heparina sódica no fraccionada intravenosa es la utilizada clásicamente en el tratamiento del Tromboembolismo pulmonar. Se recomienda en perfusión continua porque la intermitente (cada 4 horas) tiene mayor tendencia al sangrado y a la recurrencia del Tromboembolismo pulmonar.
Ante la sospecha de Tromboembolismo pulmonar el tratamiento con heparina debe iniciarse lo antes posible, si no hay contraindicación. Se da un bolo i.v de (5.000-10.000 U.I) seguido de perfusión continua a 15-25 U/KG de peso y hora, sin sobrepasar la dosis de 1,600 UI/H. Debemos hacer controles de coagulación midiendo el tiempo de tromboplastina parcial activada (TTPA), considerando el rango terapéutico cuando se encuentra 1,5-2,5 veces el valor basal de control.
La duración del tratamiento con heparina sódica es de 5-10 días pasando luego a anticoagulantes orales durante 3-6 meses, ambos tratamientos se deben superponer durante 4-5-días.
2. Heparinas de bajo peso molecular. Se están introduciendo como una nueva alternativa en el tratamiento del Tromboembolismo pulmonar. Su seguridad y eficacia están bien establecidas en el tratamiento de la trombosis venosa profunda con resultados iguales o mejores que la heparina fraccionada. Existen estudios que apoyan el inicio del tratamiento con heparinas de bajo peso molecular subcutáneas ajustadas al peso en pacientes con Tromboembolismo pulmonar hemodinámicamente estable. Este tratamiento comienza a ser la práctica habitual en algunos hospitales.
Recientemente se ha demostrado que la tinzaparina subcutánea es tan segura y eficaz como la heparina no fraccionada en casos de Tromboembolismo pulmonar, con similares tasas de recurrencia, complicaciones y mortalidad. Las ventajas de las Heparinas de bajo peso molecular sobre las heparinas no fraccionadas es que tienen una vida media más larga, no requieren control de TTPA, provocan menos hemorragias y la relación dosis respuesta es más predecible.
3. Anticoagulantes orales. El tratamiento con anticoagulantes orales debe iniciarse lo más pronto posible, si puede ser antes del 3║ día de iniciado el tratamiento con heparina. En la primera semana debemos hacer controles todos los días, ajustando la dosis según el INR, para que la anticoagulación sea optima el INR debe estar entre 2-3. La anticoagulación se prolongará en función de la aparición de recurrencias, la identificación de factores de riesgo y la etiología:
• Primer episodio se anticoagula durante 3 meses.
• Si factores de riesgo tratables se anticoagula 1mes.
• Tromboembolismo pulmonar idiopático o déficit de proteína C, anticoagulación 6 meses o más.
• Primera recurrencia, 1 año de tratamiento.
• Recurrencias sucesivas, anticoagulación de por vida.
4. Fibrinolisis. Se ha visto que disuelve el coágulo con más rapidez que la heparina, pero la mortalidad es la misma, el riesgo de hemorragia es mayor y el coste económico más elevado. Hay que valorar bien el riesgo coste-beneficio y tener un alto grado de certeza diagnóstica. Se indica en casos de Tromboembolismo pulmonar masivos y hemodinámicamente inestables. Su indicación debe basarse en una sospecha clínica más signos ecocardiográficos de disfunción del VD e hipertensión pulmonar. La fibrinolisis se debe realizar en las primeras 24 horas con estreptoquinasa, urocinasa y activador del plasminógeno tisular. Las pautas más frecuentes utilizadas en el tratamiento trombo lítico del Tromboembolismo pulmonar son por orden de eficacia:
o Pauta rt-PA: 100 mg puestos en 2 horas con un bolo inicial de 10 mg y 90 mg en 2 horas. El rt-PA se puede dar en forma de bolos: 0,6 mg/ kg hasta un máximo de 50 mg administrado en 2-3 minutos y se puede repetir la dosis a los 30 minutos si es preciso.
o Pauta UK. 2000 UI/ Kg en 15 minutos seguidas de 2000 UI/ Kg/ h durante 12-24 horas.
o Pauta SK: 250.000 UI en 20 minutos seguido de 100.000 UI/ hora durante 24 horas.
5. Filtro en vena cava inferior. Se coloca por debajo de las venas renales para interrumpir el flujo sanguíneo. Utiliza un mecanismo que funciona como filtro que impide el paso a la circulación de émbolos mayores de 3 mm. La mortalidad asociada a la implantación de un filtro de cava es del 0,2%. Indicaciones absolutas de filtro permanente en vena cava inferior:
• Tromboembolismo pulmonar recurrentes por fallo en la anticoagulación
• Cuando hay contraindicación absoluta de anticoagulantes.
• Cuando presentan hemorragias con los anticoagulantes.
• Tromboembolismo pulmonar masivos con gran repercusión hemodinámica y shock.
Las indicaciones de un filtro temporal en vena cava inferior no están bien establecidas aunque se aceptan como aconsejables:
• Embarazada joven con trombosis venosa profunda y Tromboembolismo pulmonar masivo.
• Trombosis de vena cava muy alta y no hay posibilidad de poner un filtro definitivo que nos garantice que no va a emigrar el trombo.
• trombosis venosa profunda amenazante y Tromboembolismo pulmonar severo con HTA pulmonar y que tiene tratamiento fibrinolítico.
• Joven con trombos amenazantes en VCI o en sector femoroilíaco y no hay contraindicación para usar tratamiento trombolítico
6. Embolectomía. Se hace con cirugía o con catéteres de succión. Es muy agresiva y se utiliza poco. Mortalidad peri operatoria 25%.
La interrupción de la vena cava inferior mediante la implantación de dispositivos intravasculares que impiden el paso de trombos mayores de 2 milímetros hacia las venas pulmonares debe valorarse en determinados casos: pacientes en los que existe contraindicación absoluta de anticogulación o aquellos que han presentado hemorragia grave como complicación del tratamiento anticoagulante, así como en casos con Tromboembolismo pulmonar recurrente a pesar de estar correctamente anticoagulados.
Los anticoagulantes constituyen la piedra fundamental en el manejo de un grupo de enfermedades que tienen una elevada morbilidad y mortalidad en el paciente grave. Patologías tales como: enfermedad tromboembólica venosa, el síndrome coronario agudo, el infarto cerebral aterotrombótico y otras, constituyen indicaciones básicas de los anticoagulantes en el paciente grave. Por otra parte los estados de hipercoagualabilidad, definidos por Almagro,1 como aquellos estados en que determinados trastornos tienden a desviar el balance hemostático hacia la deposición intravascular de fibrina constituyen también indicaciones de anticoagulación en el paciente grave.
Existen diferentes esquemas de anticoagulación, lo que no permite una estandarización de la terapéutica con el objetivo de lograr un uso mas eficaz de los anticoagulantes.
ESQUEMAS DE TRATAMIENTO ANTICOAGULANTE
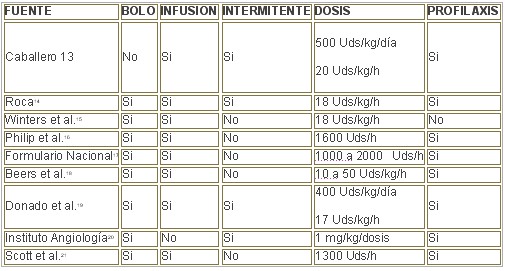
Tomando en consideración lo anterior, así como la experiencia acumulada en nuestras unidades de atención al grave y la necesidad de estandarizar la terapéutica anticoagulante como pauta imprescindible para la mejoría de la calidad de la atención al enfermo grave, proponemos el siguiente esquema de tratamiento, que estaría conformado por la administración de heparina no fraccionada o convencional con un bolo de entrada o dosis de ataque de 100 Unidades por kg de peso lo que representaría 7 000 Unidades para un paciente de 70 kg de peso y 10 000 unidades para el que tenga un peso de 100 kg; se continúa con una infusión de heparina a razón de 18 unidades por kg de peso por hora que podrá ser incrementarse según la gravedad del paciente y los resultados de las pruebas de laboratorio, hasta entre 20 y 25 Unidades por kg de peso por hora en situaciones como el tromboembolismo pulmonar con inestabilidad hemodinámica.
Este esquema lo mantenemos entre 7 y 10 días, de acuerdo con la evolución clínica del paciente, se realiza el seguimiento de laboratorio mediante el tiempo parcial de tromboplastina activado, que debe mantenerse entre 1.5 a 2.5 veces el control o entre 60 y 80 segundos. Iniciamos simultáneamente la administración de anticoagulantes orales, entre el segundo y tercer día de tratamiento anticoagulante, preferiblemente con warfarina: 10 miligramos de inicio que adecuamos según los resultados del INR. Con este esquema se alcanzan niveles de anticoagulación alrededor del quinto día de tratamiento que permite la reducción de la dosis de heparina no fraccionada.
Con referencia a la profilaxis de las complicaciones clínicas mediante el uso de anticoagulación, utilizamos heparinas de bajo peso molecular, de probada eficacia para este objetivo,2,3,16,21 o heparina no fraccionada: 5 000 unidades cada 8 ó 12 horas por vía subcutánea.
La heparina fraccionada o de bajo peso molecular representa una alternativa terapéutica por las ventajas que ofrece con respecto a la heparina no fraccionada. Se indica fundamentalmente para prevenir el tromboembolismo. Otros investigadores la aceptan como terapéutica alternativa en la enfermedad tromboembólica y de otros estados trombóticos. Al respecto, Sáenz22 en las Guías Prácticas de la Sociedad Española de Cardiología en Tromboembolismo Pulmonar e Hipertensión Pulmonar pone en duda el hecho de que las heparinas de bajo peso molecular constituyan una alternativa en el tratamiento del tromboembolismo pulmonar. Al respecto, Borla y Olivella23 están en contra de este criterio y concluyen que constituyen una buena alternativa en el tratamiento del tromboembolismo pulmonar. El consenso del American College of Chest Physicians24 informó que el tratamiento de la enfermedad tromboembólica venosa debería ser con heparinas de bajo peso molecular o heparina no fraccionada por vía intravenosa o subcutánea. Dahl25 emplea un régimen terapéutico a base de heparina de bajo peso molecular y warfarina en la prevención del tromboembolismo venoso. Nosotros hemos observado una respuesta clínica más rápida en los pacientes tratados con heparina no fraccionada en la enfermedad tromboembólica venosa y la preferimos en la prevención de la enfermedad tromboembólica venosa y no para su tratamiento.
PROFILAXIS
Ā
Las dificultades que plantea la detección del embolismo pulmonar y la elevada morbilidad y mortalidad a pesar de los avances en el diagnóstico y tratamiento de esta enfermedad hacen que la profilaxis adecuada de la trombosis venosa profunda pueda considerarse como la mejor arma terapéutica. La enfermedad tromobembólica constituye una causa de mortalidad potencialmente evitable, especialmente en el ámbito de los pacientes hospitalizados. Un conocimiento de los factores de riesgo para el desarrollo de trombosis permite una adecuada evaluación y estratificación de los pacientes de acuerdo a los grupos de riesgo de trombosis venosa profunda y EP con el fin de administrar una profilaxis adecuada.
La elevada incidencia de trombosis venosa profunda como complicación postoperatoria es bien conocida desde hace varias décadas, oscilando entre el 20-25% en intervenciones de cirugía general, y el 45-50% en cirugía ortopédica. La incidencia de Tromboembolismo pulmonar en estos casos es dificil de valorar, aunque se calcula que es de alrededor del 1% en pacientes mayores de 40 años sometidos a cirugía general y hasta el 3% en las intervenciones de cirugía ortopédica de cadera o rodilla.
Diversos estudios randomizados han demostrado que el riesgo de tromboembolismo venoso en pacientes sometidos a cirugía ortopédica, especialmente los de edad avanzada, puede reducirse en más de un 50% con el empleo de una profilaxis eficaz 39. Esto hace que las principales indicaciones de profilaxis antitrombótica sean la cirugía general, en especial pacientes con edad superior a 40 años, o en menores de esta edad con alguno de los factores de riesgo ya mencionados en apartados previos, y la cirugía ortopédica en adultos de cualquier edad y especialmente en obesos; los pacientes con fracturas en extremidades inferiores que requieran inmovilización en cama también deben recibir profilaxis. Aparte del ámbito quirúrgico, es recomendable el tratamiento profiláctico en pacientes ingresados que precisan reposo en cama con alguno de los siguientes diagnósticos: infarto agudo de miocardio, insuficiencia cardiaca congestiva, enfermedad pulmonar obstructiva crónica, neoplasias (en especial de páncreas, pulmón y próstata), sepsis, lesiones del sistema nervioso central que den lugar a hemiplejias o paraplejias, obesos, quemados (más del 40% de la superficie corporal), antecedentes de enfermedad tromboembólica venosa, mayores de 70 años, policitemia vera y poliglobulias secundarias, hemoglobinuria paroxística nocturna, síndrome nefrótico.
Entre los tratamientos profilácticos disponibles existen métodos de prevención de tipo mecánico y medidas farmacológicas. Los primeros tienen el objetivo de reducir el estasis venoso y entre ellos se encuentra la movilización precoz de los pacientes hospitalizados por enfermedades médicas o aquellos sometidos a intervenciones quirúrgicas, el drenaje postural con elevación de miembros inferiores, el empleo de medias elásticas de compresión o la compresión neumática intermitente. En cuanto a las medidas farmacológicas, el desarrollo de las heparinas de bajo peso molecular ha supuesto un gran impacto, no solo en el tratamiento de la trombosis venosa profunda, sino fundamentalmente en la prevención de la enfermedad tromboembólica. El tipo de método, la pauta, las dosis y la duración del tratamiento profiláctico debe establecerse de forma individualizada en relación con cada categoría de riesgo y con la duración del riesgo trombótico. Diferentes trabajos recientes revisan las recomendaciones profilácticas antitrombóticas actuales. En algunos estudios se relaciona la tendencia general a reducir las estancias hospitalarias en los pacientes de cirugía ortopédica con una posible reducción en la duración del tratamiento profiláctico, aunque recientes trabajos han sugerido que la profilaxis con HBPM durante 30 días en estoe grupo de pacientes parece ser más eficaz que una pauta de 7 días; es probable que existan otros factores que pueden afectar a la eficacia de la tromboprofilaxis, incluyendo el momento en que esta se inicia y la elección del fármaco.
BIBLIOGRAFÍA
1. Revista: N Engl J Med; 1999; 341: 793-800.Samama MM, Cohen AT, Darmon J et al.Uso de enoxaparina en la profilaxis de tromboembolismo venoso en pacientes con enfermedades médicas agudas.
2. Incidence of pulmonary embolism in venous thrombosis. Mostbeck A. Wien Med Wochenschr 1999;149(2-4):72-5
3. Incidence, clinical characteristics, and timing of objectively diagnosed venous thromboembolism during pregnancy. Gherman RB, Goodwin TM, Leung B, Byrne JD, Hethumumi R, Montoro M. Obstet Gynecol 1999; 94(5 Pt 1):730-4
4. Diagnosis of pulmonary embolism. Raskob GE, Hull RD. Curr Opin Hematol 1999 Sep;6(5):280-4
5. Treatment of pulmonary thromboembolism. Goldhaber SZ. Intern Med 1999; 38(8):620-5
6. Prevention of venous thromboembolism. Rosen SF, Clagett GP. Curr Opin Hematol 1999; 6(5):285-290
7. Atención Primaria en la red. Tromboembolismo pulmonar. http://www.Fisterra.com
8. Departamento de Cirugía (Prof. Gómez Alonso). Hospital Clínico Universitario. Facultad de Medicina. Salamanca (España)Complicaciones Hemorragicas De Los Anticoagulantes
http://www.angiologia.es/Web%5C3603%5C36030118.pdf
9. Rev. Doyma.Medicina Intensiva. Lunes 1 Agosto 2005. Volumen 29 - Número 06 p. 325 - 328 . www.db.doyma.es/cgi-bin/wdbcgiexe/doyma/home.home
10. Rev. Cubana Angiol Cir Vasc 2006;7.Hospital General Provincial Docente “Roberto Rodríguez Fernández”
Morón, Ciego de Ávila .Estudio de morbilidad y mortalidad en el tromboembolismopulmonar. http://bvs.sld.cu/revistas/ang/vol7_1_06/angsu106htmĀ
11. Trasylol.Indice Farmacéutico Medicohomepage.com
12. Boletin Escuela de Medicina.vol/28 N°3 1998 , Universidad Católica de chile.Factores Predisponentes y manejo de la trombosis venosa profunda; escuelamed.puc.cl
13. Rev Cubana Hematol Inmunol Hemoter 1997;13(2):90-108 Instituto de Hematología e Inmunología. Ciudad de La Habana, Cuba.Estados de hipercoagulabilidad. http://www. bvs.sld.cu/revistas/hih/vol13-2-97/hih03297htm.
14. Revista Cubana de Medicina Intensiva y Emergencias 2006;5(1) Hospital Provincial Docente: “Manuel Ascunce Domenech”. Unidad de Cuidados Intensivos.Camagüey. Esquemas de anticoagulación en el paciente grave http://bvs.sld.cu/revistas/mie/vol 5_1_06/mie 11506
15. An. Med. Interna (Madrid) v.22 n.4 Madrid abr. 2005
Tratamiento del tromboembolismo pulmonar agudo con heparina de bajo peso molecular subcutánea. Comparación con heparina no fracionada intravenosa . http://www.scielo.isciii.es/scielo.php/ing_es
16. En torno Medico. Diario electrónico de sanidad. http:// www.medynet.com./elmedico/biblio/index.htm#1
Autores:
Dr. Gerardo Álvarez Álvarez.
Master en Psicología Médica.
Especialista en 2do grado en Medicina Interna.
Profesor Auxiliar del Instituto Superior de Ciencias Médicas de Villa Clara.
J” de Cátedra clínica Medica Hospital Universitario Arnaldo Milian Castro.
Presidente Sociedad Cubana de Medicina Interna de Villa Clara.
J” del Grupo Provincial De HTA Villa Clara. Cuba.
Dr. Elvys Pérez Bada.
Especialista de 1er grado en Medicina Interna.
Profesor Instructor Instituto Superior de Ciencias Medicas Villa Clara.
Responsable de Residencia de Medicina Interna. Hospital Universitario Arnaldo Milian.
Asesor de Extensión Universitaria. Departamento Docencia.
J” Sala Medicina B. Hospital Arnaldo Milian Castro.