Durante los últimos 10 años, se han acumulado un significativo número de experiencias que implican a células y a moléculas relacionadas con la respuesta inmunológica en el proceso de la lesión vascular relacionada con la arteriosclerosis y la ateromatosis.
El papel que estas células, y moléculas de relación intercelular, desempeñan en la lesión vascular no es propiamente inmunitario, sino que es un ejemplo de las consecuencias fisiopatológicas de la cascada de eventos que relaciona la inmunidad con la inflamación. La aparición en plasma de diversas sustancias, puede emplearse en la actualidad, y mucho más en el futuro, como marcadores de riesgo y de lesión vascular latente.
Marcadores cardiacos. La proteína C reactiva. Recopilación de datos de revisiones bibliográficas y conclusiones.
R. Navarro Castelló, J. I. A. Soler Díaz, M. Garrido Fernández.
Comenzaremos, ubicando la Proteína C Reactiva (proteína C reactiva) dentro del Sistema Inmunitario Innato.
Todos los organismos multicelulares, entre ellos el ser humano, han desarrollado el uso de un número limitado de moléculas codificadas por líneas germinales que reconocen grandes grupos patógenos.
Dada la miríada de agentes que son patógenos para el ser humano, las moléculas del Sistema Inmunitario Innato humano deben reconocer las PAMP (del inglés: pathogen – associated molecular patterns), estructuras moleculares comunes compartidas por muchos patógenos.
Las PAMP deben ser estructuras conservadas, vitales para la virulencia y la supervivencia del patógeno, como las endotoxinas bacterianas, de modo que los patógenos no pueden mutar las moléculas de las PAMP para evadir las respuestas inmunitarias innatas humanas.
Además, un producto final importante de la Inmunidad Innata es la destrucción del patógeno invasor, de modo que es preciso que las PAMP reconocidas por las respuestas inmunitarias innatas sean completamente distintas de las moléculas propias.
Las PRR (del inglés: pattern recognition receptors) son proteínas del sistema inmunitario innato del huésped que reconocen las PAMP, y son moléculas humanas cuyos ancestros son primitivos.
De este modo, el reconocimiento de las moléculas patógenas por los tipos celulares hematopoyéticos y no hematopoyéticos conducen a la activación / producción de la cascada del complemento, las citocinas y los péptidos antimicrobianos como moléculas efectoras.
Las principales familias de proteínas PRR son las lecitinas del tipo C, las proteínas ricas en leucina, las proteínas del receptor barrendero (“scavenger”) de los macrófagos, las pentraxinas plasmáticas, las transferasas lipídicas y las integrinas.
Un grupo importante de glucoproteínas colágenas de PRR con dominios lecitina de tipo C recibe el nombre de colectinas, y entre ellas está la proteína sérica lecitina fijadora de la manosa.
Ésta y otras colectinas, así como otras dos familias de proteínas:
Las pentraxinas: como la Proteína C Reactiva y el componente amiloideo A del suero, y
Los receptores barredores de los macrófagos, tienen la propiedad de opsonizar (recubrir) a las bacterias para su fagocitosis por los macrófagos, y también pueden activar la cascada del complemento para destruir las bacterias.
La proteína C reactiva en el sistema cardiovascular.
Durante los últimos 10 años, se han acumulado un significativo número de experiencias que implican a células y a moléculas relacionadas con la respuesta inmunológica en el proceso de la lesión vascular relacionada con la arteriosclerosis y la ateromatosis.
El papel que estas células, y moléculas de relación intercelular, desempeñan en la lesión vascular no es propiamente inmunitario, sino que es un ejemplo de las consecuencias fisiopatológicas de la cascada de eventos que relaciona la inmunidad con la inflamación.
La aparición en plasma de diversas sustancias, puede emplearse en la actualidad, y mucho más en el futuro, como marcadores de riesgo y de lesión vascular latente.
Por consiguiente, su conocimiento será imprescindible en la Medicina Cardiovascular en los próximos años.
La historia de la relación, entre Enfermedad Cardiovascular e Inflamación, tiene uno de sus comienzos en el análisis del Múltiple Risk Factor Intervention Trial, en el que se encuentra una asociación de la Proteína C Reactiva (PCR) con el Infarto de Miocardio, con un odds ratio de 4.30 que persistía a pesar del ajuste por tabaquismo y otros factores de riesgo clásicos.
Así, como también, en el Cardiovascular Health Study and the Rural Health Promotion Project, en el que se sugería una asociación más estrecha de riesgo de Infarto con la proteína C reactiva para mujeres (OR: 4.50) que para hombres (OR: 1.75).
Poco después, en un subanálisis del Physicians’ Healt Study se comprobó su papel predictor en la enfermedad cardiovascular.
Se han intentado justificar estos mecanismos con Procesos Infecciosos que afecten a la pared arterial, y con mayor intensidad, se ha tratado de relacionar con la infección causada por Chlamydia pneumoniae, y sin embargo, nunca se ha llegado a afirmar con seguridad su relación con la enfermedad cardiovascular, siendo circunstanciales y muy escasas las relaciones epidemiológicas que puedan sugerirla en la actualidad.
La célula central en el proceso arteriosclerótico es el monocito – macrófago. Intervienen, además, diversos tejidos y órganos en la interacción celular que dan lugar al Proceso Inflamatorio: miocardio, endotelio, media arteriolar, tejido adiposo, hígado, etc.
Sin embargo, el desencadenante de la alteración estructural y funcional de la pared arterial, es la concentración de colesterol LDL (lipoproteínas de baja densidad) oxidada en el plasma y en la propia pared arterial.
A mayor concentración de lipoproteínas de baja densidad (LDL) oxidadas (densas y pequeñas: miden menos de 250 Å), mayor es la importancia del Riesgo Cardiovascular.
Es importante, en un Laboratorio, el medir la concentración de colesterol LDL y Apolipoproteína B en el plasma, de un modo seriado en el tiempo. Hemos de calcular el cociente: Colesterol LDL / Apolipoproteína B, para poder saber que tamaño tienen las lipoproteínas de baja densidad (LDL).
En esta revisión, tratamos de aclarar las relaciones que guardan entre sí los diversos factores celulares y moleculares que finalmente pueden condicionar la aparición de una Enfermedad Cardiovascular.
En primer lugar, veremos los mecanismos del Proceso Inflamatorio Arterial, y en segundo lugar se verán las Evidencias Epidemiológicas y Clínicas que relacionan el Proceso Inflamatorio con la Enfermedad Vascular.
En la Pared Arterial ocurre un proceso molecular y humoral que conlleva cambios estructurales y funcionales.
A continuación, se analizan las diferentes fases y mecanismos de la inflamación que intervienen en el proceso patológico relacionado con la Lesión Arteriosclerótica.
Disfunción endotelial.
Las lipoproteínas de baja densidad (LDL) oxidadas induce una alteración endotelial que consiste principalmente en la interrupción del proceso del óxido nítrico (ON) y en la muerte apoptósica (apoptosis: muerte programada) de las células endoteliales.
La producción normal de óxido nítrico por el endotelio como respuesta a factores neurohumorales y dependientes del flujo sanguíneo, implica la activación del óxido nítrico cintaza endotelial, y además de inducir vasodilatación, inhibe la activación y agregación plaquetaria, y refuerza la barrera como protectora de la pared vascular.
De este modo impediría la expresión de receptores de adhesividad celular en la superficie endotelial y dificultaría el paso de células inflamatorias circulantes a través del propio endotelio.
Cuando disminuye la producción de óxido nítrico: aumenta la adhesividad, la migración celular a través del endotelio y se facilita la aparición de “huecos” en la superficie interna vascular a causa de la apoptosis de las células endoteliales.
La adhesión de las plaquetas alrededor de la Lesión Endotelial libera el PDGF (factor de Crecimiento derivado de las Plaquetas).
Oxidación de las lipoproteínas.
Las lipoproteínas secuestradas dentro del espacio extracelular de la íntima, a salvo de los antioxidantes del plasma, podrían ser muy sensibles a la modificación oxidativa.
Las Lipoproteínas de baja densidad (LDL) oxidadas, no son homogéneas sino que, en realidad, forman una mezcla variable y mal definida.
Las moléculas lipídicas y proteicas de estas partículas podrían participar en procesos de oxidación.
Las modificaciones de los lípidos incluirían la formación de hidroperóxidos, lisofosfolípidos, oxiesteroles y productos aldehídicos de la degradación de los ácidos grasos.
Entre los productos recientemente descritos procedentes de la oxidación de los fosfolípidos se encuentran la palmitol – oxovaleroil – glicero – fosforil colina (POVPC), la palmitol – gloutaroil – glicero – fosforil colina (PGPC) y la epoxiisoprostano E2 – glucero – fosfocolina (PEIPC). Las modificaciones de la apoproteína, consisten en roturas del esquema peptídico y la derivación de algunos aminoácidos.
El grupo amino de la cadena lateral de la lisina podría condensarse con componentes de los lípidos oxidados (4 – hidroxinonenol o dialdehído malónico).
Una modificación reconocida recientemente, podría ser la producción local de ácido hipocloroso por las células inflamatorias de la placa, con la consiguiente aparición de radicales clorados, como las proteínas clotirosil.
En la actualidad, la investigación se dirige a caracterizar los componentes químicos específicos de las lipoproteínas oxidadas, de los que dependen sus efectos biológicos. Así ocurre, por ejemplo, con la oxovaleril – fosforil colina.
Se dispone de indicios, más que considerables, de que estas sustancias químicas están presentes en las lesiones ateroscleróticas.
Glucosilación no enzimática.
Es probable que, en los pacientes diabéticos con hiperglucemia mantenida, se produzca una glucosilación no enzimática de las apolipoproteínas y de otras proteínas arteriales, que alterarían su función y acelerarían la producción de aterogénesis. Numerosos trabajos experimentales indican que, tanto las lipoproteínas sometidas a modificación oxidativa como las glucosiladas, o sus componentes, podrían contribuir a muchos de los acontecimientos celulares posteriores en el desarrollo de la lesión.
Reclutamiento de leucocitos.
Tras la acumulación de lípidos extracelulares, el siguiente paso en la formación de la “estría grasa” es el reclutamiento de leucocitos. Los principales leucocitos hallados en un ateroma, en la fase de desarrollo, son las células de la estirpe mononuclear: monocitos y linfocitos. Posiblemente, en el reclutamiento de los leucocitos, hacia la estría grasa naciente, intervienen una serie de moléculas de adherencia o receptores para ellos, que se expresan en la superficie de las células del endotelio arterial.
El endotelio disfuncionante induce la aparición de moléculas de adhesión en su superficie. Las más “interesantes” son:
- la molécula de adherencia de la célula vascular 1 (VCAM-1) y,
- la molécula de adherencia intercelular 1 (ICAM-1)
miembros de la superfamilia de los genes de las inmunoglobulinas, así como las selectinas E y P (miembros de una familia diferente de receptores leucocitarios, conocida como selectina).
La lisofosfatidilcolina, un componente de las lipoproteínas de baja densidad (LDL) oxidadas, incrementa la expresión de la VCAM-1.
Algunas de estas moléculas pueden ser detectadas en plasma, y servir como marcador del Proceso Inflamatorio Vascular, como más adelante se verá.
Una vez adheridas a la superficie de la célula endotelial arterial, gracias a su interacción con un receptor del tipo VCAM-1, los monocitos y linfocitos penetran en la capa endotelial y establecen su residencia en la íntima.
Además de los componentes de las lipoproteínas modificadas, las citocinas (un grupo de mediadores proteicos de la Inflamación), también regulan la expresión de las moléculas de adherencia que intervienen en el reclutamiento de los leucocitos.
Además, el endotelio produce varias moléculas, cruciales para los fenómenos que ocurrirán posteriormente: MPC-1 (proteína quimiotáctica para monocitos), que atraerá más monocitos a la pared dañada; M-CSF (factor estimulante de las colonias de monocitos), que los dota funcionalmente; y NF-kB (factor nuclear kappa B), implicado en la transcripción de un importante número de genes funcionales en el Proceso Inflamatorio.
Producción de citocinas.
Como consecuencia de la presencia subendotelial de los monocitos convertidos en macrófagos, por la presencia, en el medio, de sustancias activadoras (M-CSF) y por otras moléculas estimuladoras de la transcripción (NF-kB) de genes implicados en la producción de sustancias proinflamatorias, se producen potentes citocinas en las paredes arteriales.
Entre ellas, está la interleucina 1 (IL-1) y el factor de necrosis tumoral (TNFa), que favorecen la producción local de factores de crecimiento, entre ellos el factor de crecimiento de origen plaquetario y el factor de crecimiento fibroblástico, junto con otros que podrían intervenir en la evolución y complicación de la placa. Otras citocinas, sobre todo el interferón (IFN) y derivado de las células T activadas (linfocitos T activados) del interior de la lesión, inhiben la proliferación del músculo liso y la síntesis de las formas intersticiales de colágeno.
Estas citocinas, amplían los fenómenos inflamatorios locales, activando a otras células, como los linfocitos T, que participan en la cascada inflamatoria con otras muchas interleucinas, como la IL-6. El efecto conjunto, es la estimulación de la RESPUESTA INMUNE LOCAL y la manifestación de efectos a distancia, como la producción de PROTEÍNAS de FASE AGUDA, en el hígado.
La TNFa, además, es un potente inductor de NF-kB (también lo son la IL-6 y la IL-1b), con lo que se cierran círculos en la lesión inflamatoria mantenida.
ESQUEMA. Producción de los principales Marcadores y Moléculas involucradas en la Fisiopatología del Proceso Inflamatorio Vascular.
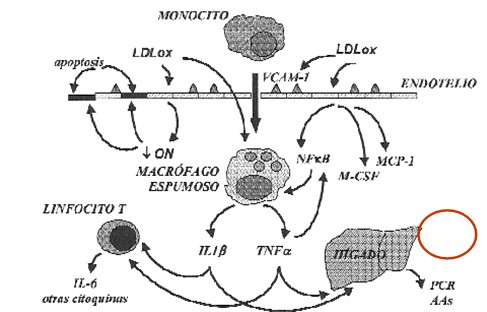
LDLox: LDL oxidada; ON: Oxido Nítrico; VCAM-1: molécula de superficie de adhesión celular (integrina); MCP-1: proteína quimiotáctica para monocitos; M-CSF: factor estimulador de colonias de monocitos; NF-kB: factor nuclear kappa B; IL-1: interleucina 1; TNFa: factor de necrosis celular; IL-6: interleucina-6; PCR: Proteína C Reactiva; Aas: amiloideo A sérico.
Los macrófagos activados producen, además, una serie de enzimas conocidos como metaloproteinasas (MMP), que destruyen la matriz extracelular del conectivo y, al disminuir la cantidad de colágeno, hacen a la placa de ateroma más frágil, por lo que la inflamación arterial, además, facilita la ROTURA de la Placa de Ateroma y, consiguientemente, la aparición de clínica isquémica.
Marcadores de inflamación.
Los marcadores de inflamación que se discuten con más intensidad, en la literatura, son las proteínas no relacionadas directamente con la lesión inflamatoria vascular. De hecho, se producen en el hígado como respuesta a las citocinas, específicamente TNFa y ILb, y por ello, son una respuesta inespecífica, ya que cualquier Proceso Inflamatorio eleva estos marcadores.
En la Patología Cardiovascular, se han encontrado relaciones con la Proteína C Reactiva (PCR), Amiloide a en el suero (AAs), y Fibrinógeno. A este último, no conviene “perderlo de vista”; sin embargo, la concentración sérica del fibrinógeno también puede afectarse, tanto por polimorfismos genéticos, como por factores metabólicos y ambientales, niveles de colesterol, triglicéridos, PAI-1 (inhibidor del activador del plasminógeno), antecedentes familiares, o por el consumo de cigarrillos.
Probablemente, es la determinación de los niveles séricos de proteína C reactiva la que ofrece un mejor reflejo del Proceso Inflamatorio subyacente, ya que se correlaciona con otros marcadores, como: los niveles séricos de ICAM-1, IL-6, Fibrinógeno, Activador tisular del Plasminógeno (tPA), PAI-1 y Factor VII.
Sin embargo, los niveles de esta proteína son realmente bajos en condiciones en los que no existe un Proceso Inflamatorio de relevancia clínica, por lo que se ha de recurrir a técnicas de determinación ultrasensibles (PCRus) para poder discriminar la relevancia clínica de los valores.
Aunque, efectivamente, la proteína C reactiva se puede encontrar en la pared arterial del vaso arteriosclerótico, no se le ha atribuido función alguna, hasta que recientemente se ha publicado que puede desempeñar un papel en la fagocitosis de las lipoproteínas de baja densidad (LDL) por el macrófago para formar la célula espumosa, a través de la opsonización (recubrimiento) de la partícula lipoproteica.
Relaciones de los parámetros de inflamación con los factores de riesgo cardiovascular clásicos.
La extensión de la enfermedad arteriosclerótica, se ha relacionado con la concentración plasmática de ciertas moléculas de adhesión celular (VCAM-1) que, como antes se ha descrito, intervienen en el proceso de transmigración monocitaria hacia el espacio subendotelial.
Esto podría ser un efecto aislado, sino se hubiera demostrado además, que la concentración de otras moléculas de adhesión en el suero (sICAM-1) tienen una estrecha relación con el hábito del tabaquismo, y también para el resto de factores de riesgo para la Enfermedad Vascular que coinciden en el mismo paciente (Riesgo Global).
Varios Factores de Riesgo bien conocidos, y especialmente, las cifras del Perfil Lipídico, se correlacionan con los niveles de proteína C reactiva circulantes.
ESQUEMA: Relaciones de la Proteína C Reactiva, con Parámetros Clínicos de relevancia en el Riesgo Cardiovascular.
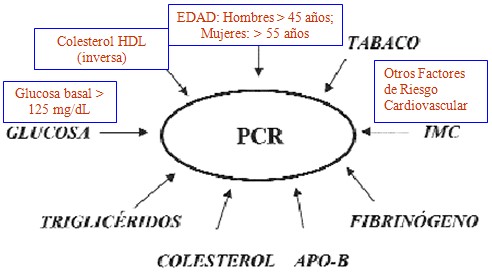
La IL-6, elevada en el curso de la Enfermedad Vascular, refleja la actividad inmune “en el sitio”. Esta citosina puede producirla: el endotelio vascular (estimulado por la hiperglucemia) y también el tejido adiposo.
Concentraciones de PCRus (ultrasensible) para la valoración del riesgo cardiovascular (según Dade-Behring Diagnóstica).
Tradicionalmente se ha utilizado la medición de la Proteína C Reactiva (PCR), en suero o plasma, como Reactante de Fase Aguda para el diagnóstico y monitorización de los Procesos Inflamatorios.
Los resultados de estudios recientes, sin embargo, indican que los niveles de proteína C reactiva tienen un Alto valor Diagnóstico para la Valoración del Riesgo Cardíaco. De hecho, como la inflamación parece jugar un importante papel en la patogénesis de la trombosis arterial, el grado de elevación de la proteína C reactiva (que puede reflejar una reacción inflamatoria de bajo grado atribuible a una inflamación crónica) puede predecir el riesgo de futuros problemas cardíacos e infartos.
Este nuevo ensayo ultrasensible, posibilita ahora, la medición de concentraciones extremadamente bajas de proteína C reactiva, como las que han sido relacionadas como evidentes en estudios recientes en conexión con la infección, inflamación y trombosis arterial.
Datos significativos:
Niveles de proteína C reactiva > 3 mg/L (0.3 mg/dL) en el momento de la admisión en el Centro Hospitalario, indican un pronóstico de riesgo en pacientes con Angina de pecho Inestable. Las elevaciones significativas de las concentraciones de proteína C reactiva están correlacionadas con el incremento de la gravedad de la Enfermedad Arterial Coronaria (CAD).
En pacientes que no muestran enfermedad arterial coronaria, por medio de angiografía coronaria, la media de concentraciones de proteína C reactiva era de 0.87 mg/L. En contraste, la concentración promedio era de 1.43 mg/L en pacientes con tres coronarias afectadas.
La infección crónica bacteriana como seropositiva a la Chlamydia pneumoniae o a la Helicobacter pylori está asociada con concentraciones de proteína C reactiva mayores que las consideradas como distribución normal de proteína C reactiva en la población general (intercuartil superior de concentración de proteína C reactiva: 3.95 mg/L).
La proteína C reactiva está también asociada con otros factores de riesgo establecidos, como elevaciones de Fibrinógeno, Colesterol Total, Apolipoproteína B, Glucosa y valores de Triglicéridos.
Las concentraciones de proteína C reactiva > 3.6 mg/L (4.13 veces el valor normal), en el estudio, predecían problemas coronarios en pacientes con Angina Inestable. Los pacientes con esos niveles de proteína C reactiva tenían el doble de riesgo de un problema coronario comparado con aquellos que tenían niveles < 3.6 mg/L.
En hombres, los niveles basales de proteína C reactiva predecían el riesgo de un futuro Infarto Cardíaco (IM) o ataque agudo. Concentraciones de proteína C reactiva > 2.1 mg/L están asociadas con el incremento 2.9 veces de riesgo desde el primer Infarto de Miocardio y un incremento 1.9 veces de riesgo de ataques.
Además, la capacidad del efecto protector de la aspirina para prevenir el primer Infarto Cardíaco estaba directamente relacionada con los incrementos del nivel de proteína C reactiva. Los pacientes con concentraciones de proteína C reactiva > 2.1 mg/L alcanzaron un efecto protector con la profilaxis de la aspirina, en donde aquellos con niveles < 0.55 mg/L no obtuvieron un beneficio significativo.
La reducción de problemas trombóticos asociados con el uso de la aspirina, incrementa la posibilidad de que los agentes antiinflamatorios como el ácido acetil salicílico (aspirina) puedan proporcionar un beneficio clínico en la prevención de la Enfermedad Cardiovascular.
Estos estudios proporcionan la evidencia de que la Enfermedad Cardiovascular se desarrolla debido a las lesiones arterioscleróticas y que está asociada con una Respuesta Inflamatoria subclínica de bajo grado que, a la vez, está reflejada por el nivel del incremento de proteína C reactiva. La utilización de la Proteína C Reactiva como marcador de la Inflamación Sistémica, da una estimulación global de la actividad fundamental de patomecanismos, y así parece ser una herramienta muy útil para la valoración del Riesgo Cardiovascular.
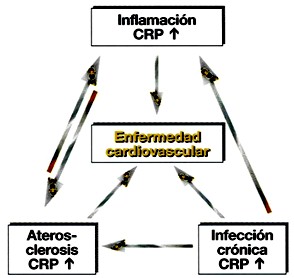
La proteína C reactiva en el síndrome coronario agudo y conclusiones.
Con las evidencias actuales, es imposible negar que los Marcadores de la Inflamación, entre los cuales destaca la Proteína C Reactiva, están asociados con eventos adversos en pacientes Coronarios Agudos y en aquellos sometidos a intervención percutánea.
Existen evidencias, que provienen de estudios prospectivos de cohortes, de que niveles elevados de este marcador (proteína C reactiva), en ausencia de otro mecanismo posible responsable de esta elevación en sangre, parecería correlacionarse con el riesgo de desarrollo y progresión de la enfermedad aterosclerótica coronaria y periférica.
Se necesitan nuevos ensayos y el uso de calibradores adicionales, para determinar sí los valores que se encuentran dentro de los rangos actuales de referencia, son útiles para predecir el riesgo de Enfermedad Cardiovascular y la estratificación de pacientes con Angina Inestable.
Necesitamos aprender a manejar la PCRus y “sacarle” todo el rendimiento posible, al igual que lo hemos hecho durante años con el perfil lipídico. Estos ensayos más sensibles, nos permitirán evaluar valores de proteína C reactiva como indicadores de respuesta inflamatoria, y establecer valores de corte para determinar el Riesgo Cardiovascular.
Así, es posible, que la proteína C reactiva se convierta en un marcador valioso para evaluar el Riesgo y la Extensión de la Enfermedad Cardiovascular. La proteína C reactiva podría constituirse en un método alterno, sencillo y “económico”, para poder definir, que pacientes con síndrome coronario agudo, pueden tener complicaciones y peor pronóstico.
Bibliografía:
Peter Libby. Principios de Medicina Interna. Harrison. (15Ş edición. Año 2001).