Pancreatitis en niño con Enfermedad de Crohn: a propósito de un caso
La azatioprina es uno de los medicamentos más eficaces en el tratamiento de la enfermedad de Crohn activa, que mantiene la remisión y reduce el uso de corticosteroides en estos pacientes. Sin embargo, tiene numerosos efectos adversos, entre los que se encuentra la pancreatitis, que obliga a la reducción de la dosis o la retirada del tratamiento.
Autores: Romera Santa Bárbara, Beatriz; Jiménez Lucas, Carlos; Verastegui Martinez, Cayetana; Martinez Andaluz, Carla
Palabras clave: pancreatitis, azatioprina, efectos secundarios, enfermedad de Crohn infantil
RESUMEN
Presentamos el caso clínico de un niño de 9 años, con diagnóstico de enfermedad de Crohn hacia 6 semanas, en tratamiento con nutrición enteral exclusiva y azatioprina desde hacía 4 semanas, que presenta episodio de dolor abdominal agudo epigástrico, no irradiado, que no cede con analgésicos habituales. Mejora con tramadol IV y reposo digestivo. A las 24h se inicia de nuevo nutrición enteral, presentando de nuevo episodio de dolor, de mayor intensidad que el dia previo; se realiza radiografía abdominal y ecografía abdominal, descartando perforación intestinal ni aire ectópico. Ante la sospecha de pancreatitis se solicita amilasa que sale muy elevada, confirmándose el diagnostico de pancreatitis por azatioprina.
Se suspendió la azatioprina y se sustituyó por terapia biológica, con muy buenos resultados, y con menos efectos adversos.
PALABRAS CLAVE
Pancreatitis, azatioprina, efectos secundarios, enfermedad de Crohn infantil
INTRODUCCIÓN
La enfermedad de Crohn es una enfermedad inflamatoria intestinal, que afecta a cualquier porción del tubo digestivo. El proceso inflamatorio suele ser excéntrico y segmentario, por lo general, de forma parcheada. Suele ser transmural, afectando a todo el espesor de la pared intestinal. La incidencia ha aumentado en los últimos años, y se encuentra en torno a 4,5/100,000 habitantes, con un pico de edad en la adolescencia. La afectación gástrica y duodenal puede producir vómitos e importante dolor epigástrico. Pueden formarse fistulas enteroentéricas o enterocolónicas. En cuanto a las manifestaciones extradigestivas, se encuentran las aftas orales, artritis periférica, eritema nodoso, epiescleritis, cálculos renales y colelitiasis.
En cuanto al tratamiento, en las formas moderadas-graves, además de la nutrición enteral exclusiva, se tiende a utilizar fármacos inmunomoduladores de entrada, para lograr la cicatrización de la mucosa o una remision profunda, disminuyendo así el uso de corticoides.
La azatioprina, que se administra a dosis de 2-2,5 mgr/kg/dia, puede ser eficaz en los brotes moderados-graves, en casos con fistulas, o si hay corticorresistencia o corticodependencia; entre sus efectos adversos aparece trastornos gastrointestinales, pancreatitis, hepatotoxicidad, neutropenia y trombocitopenia, dosis dependiente. Dichos efectos, pueden obligar a disminuir la dosis o a retirar el fármaco, según los casos.
CASO CLÍNICO
Se trata de un niño de 9 años, diagnosticado de enfermedad de Crohn hacía 6 semanas con un brote moderado, con presencia de úlceras a lo largo de esófago y en todo el colon, con afectación profunda y parcheada. Inicialmente se trata con nutrición enteral exclusiva, pero dado la falta de respuesta, con aparición de ulceras orales y perianales, a las 3 semanas se asocia tratamiento con azatioprina.
Un mes después, y tras haber iniciado algo de alimentación sólida durante 3 días, presenta episodio de dolor abdominal intenso, epigástrico, no irradiado, que no cede con analgésicos habituales, por lo que ingresa en nuestro hospital.
Exploración
A la exploración física presenta peso de 22,8 Kg, tala 128 cm, IMC 13,91 Kg/m2, Frec cardiaca 60 lpm, temperatura de 36,2ºC y saturación de oxigeno de 98% . Afectación del estado general por el dolor. Normohidratado. Palidez de piel, no de mucosas. Signos meníngeos negativos. Auscultación cardiopulmonar normal, sin alteraciones.
Abdomen blando y depresible, doloroso a la palpación en epigastrio. No signos de irritación peritoneal. Peristaltismo presente. Faringe sin hallazgos. Afta bucal. Otoscopia bilateral normal. Lesión aftosa en región perianal.
Pruebas complementarias
En el hemograma destacaba leucocitosis de 18800, con neutrofilia de 15000, hemoglobina de 10,5 mgr/dl, y 733000 plaquetas. La bioquímica era normal. PCR 4 mg/dl; PCT 0,21ng/ml. La coagulación también estaba sin alteraciones. Se colocó Mantoux que fue negativo en su lectura a las 72 horas.
Se realizó radiografía abdominal en bipedestación sin signos de perforación intestinal ni aire ectópico , y ecografía abdominal, observándose engrosamiento mural del colon ascendente, en relación con su enfermedad de base, pero sin otras alteraciones y sin liquido libre intraperitoneal.
Evolución
Se deja a dieta absoluta, iniciándose pauta de prednisona a 2 mgr/kg/dia y analgesia con tramadol IV a 1 mgr/kg/8h, con mejoría del dolor. Al reiniciar la nutrición enteral exclusiva, comienza de nuevo con dolor abdominal intenso que se trata con paracetamol y tramadol IV, sin respuesta, precisando fentanilo para responder. Se repite ecografía abdominal, sin observarse signos de perforación gástrica ni intestinal, y en la analítica, se objetiva una amilasa de 735 U/L.
En ese momento, se sospecha pancreatitis aguda, en relación con el tratamiento con azatioprina. De nuevo se mantiene a dieta absoluta durante 24 horas más, iniciándose progresivamente tolerancia a líquidos y después sólidos, y pudiendo ser dado de alta a los 6 días de ingreso.
Dado que presentó la reacción adversa a la azatioprina se decide suspender dicho tratamiento e iniciar pauta de terapia biológica con adalimumab.
Ha presentado buena respuesta, con remisión de la clínica, pudiendo retirar por completo los corticoides y con buena evolución ponderal y tolerancia a la alimentación. En la última revisión clínica presenta peso de 35,3 kg. Talla de 131,5 cm. IMC: 20 kg/m2, y se encuentra en tratamiento con adalimumab, omeprazol y vitamina D, y sin corticoides.
DISCUSIÓN
La enfermedad de Crohn es una enfermedad inflamatoria intestinal transmural, que se caracteriza por tener afectación parcheada y afectar a todo el intestino.
La mayoría de los casos de enfermedad inflamatoria intestinal pediátrica aparece en los años de la adolescencia (edad media de 12 años), un 20% antes de los 10 años y 4% antes de los 5 años. La enfermedad de Crohn es más frecuente en varones.
Puede afectar a todo el intestino, pero la afectación más frecuente en la edad pediátrica es en forma de ileocolitis, aunque también puede aparecer ileitis (30%) o afectación del tracto gastrointestinal superior: esofagitis, gastritis, duodenitis (30%) .
La afectación gástrica puede producir vómitos y dolor epigástrico. La obstrucción parcial del intestino delgado, por la inflamación o las estenosis, pueden producir clínica de dolor tipo cólico, o distensión abdominal. La enfermedad penetrante se demuestra mediante la aparición de fístulas entero entéricas, o enterocolónicas, que pueden contribuir a la malabsorción. Tiene muchas manifestaciones extra-intestinales bien conocidas y complicaciones.
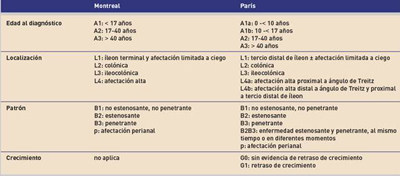
La clasificación de Montreal de la enfermedad inflamatoria intestinal (EII) de 2005 incluye criterios de edad pediátrica en un solo grupo por debajo de los 17 años, también tipo y extensión de la afectación. En la nueva clasificación de París de la enfermedad inflamatoria intestinal se han recogido aspectos peculiares de la enfermedad inflamatoria intestinal pediátrica, como la subdivisión de la edad pediátrica, ya que los menores de 10 años presentan características fenotípicas y pronósticas diferentes, la inclusión del retraso del crecimiento como un aspecto singular o la afectación diferenciada del intestino delgado según el tramo afectado. (Tabla 1).
En cuanto al tratamiento de dicha enfermedad, depende de la localización de la afectación, la gravedad de la inflamación, la edad del paciente y la presencia de complicaciones. Los pilares de tratamiento se basan en:
- Nutrición enteral exclusiva: los estudios pediátricos sugieren una eficacia similar al corticoide para la mejora de los síntomas clínicos, pero es incluso mejor para la recuperación completa de la mucosa.
- 5 aminosalicilatos: en el caso de enfermedad leve del íleon terminal o del colon. Se puede administrar mesalazina vía oral o rectal.
- Corticoides: siguen siendo un pilar de tratamiento, para disminuir la inflamación y mejorar la clínica. Dosis de 1-2 mgr/kg/día, máximo 40-60 mgr: se debe disminuir la dosis tan pronto como sea posible. No están indicados como tratamiento de mantenimiento.
- Inmunomoduladores, entre los que se encuentra la Azatioprina. Están indicados en casos de enfermedad de Crohn refractaria, fistulizante o dependiente de corticoides.
- Terapia biológica: los anticuerpos monoclonales frente a TNF-alfa (infliximab, adalimumab) han demostrado ser eficaces en la inducción, al mantenimiento de la remisión y a la curación de la mucosa en casos moderados-graves. Mejoran también la curación de las fístulas y disminuyen el uso de corticoides.
Refiriéndonos a la azatioprina, se ha demostrado que mantiene la remisión y reduce el uso de corticosteroides en pacientes con enfermedad de Crohn, sobre todo en los primeros 2 años de tratamiento. Está indicado en casos de enfermedad moderada- grave, corticodependiente o fistulizante. El efecto beneficioso de este fármaco puede retrasarse hasta 3-4 meses desde iniciado el tratamiento, por lo que no son útiles de forma aguda.
Los efectos adversos ocurren en un 15% de los pacientes en tratamiento, y entre dichos efectos se encuentran: trastornos gastrointestinales, hepatotoxicidad, mielotoxidad , con la aparición de leucopenia y trombopenia y pancreatitis.
La pancreatitis tiene una incidencia de un 7,5% del total de efectos adversos, aunque en la mayor parte de los pacientes suelen tener un curso leve ( 98% de los casos). Los niveles muy elevados de lipasa tienen peor factor pronóstico.
Diversos estudios demuestran que los pacientes con enfermedad de Crohn tienen mayor riesgo de desarrollar pancreatitis que los afectos de colitis ulcerosa, y este riesgo es cuatro veces superior al de la población general. En la población adulta, el tabaquismo es el principal factor de riesgo para el desarrollo de dicha patología, y en cuanto al sexo, existe mayor riesgo en mujeres que en varones. Así mismo, los pacientes con enfermedad de Crohn tienen mayor riesgo de desarrollar pancreatitis asociada a azatioprina.
Dado los posibles efectos secundarios de la azatioprina, en muchas ocasiones se requiere la interrupción o la reducción de la dosis de la terapia, pudiendo beneficiarse de la adición de terapia biológica o metotrexato.
Es importante pensar en los posibles efectos secundarios del tratamiento que siga el paciente, a la hora de realizar el diagnóstico diferencial con la clínica, ya que la pancreatitis puede confundirse con un dolor epigástrico por la inflamación gastrointestinal o con un absceso intraabdominal.
CONCLUSIÓN
En la enfermedad de Crohn, el tratamiento con azatioprina ha demostrado ser eficaz en el manejo de afectaciones moderadas-graves, disminuyendo la terapia con corticoides. Sin embargo, estos inmunomoduladores tienen importantes efectos secundarios que obligan a un seguimiento estrecho del paciente durante dicho tratamiento.
Entre los efectos secundarios de la azatioprina se encuentra la pancreatitis, que produce un dolor intenso epigástrico e intraabdominal, y que puede confundirse inicialmente, como sucedió en nuestro caso, con dolores asociados a la enfermedad de base o a otras complicaciones.
Aunque la mayoría de los casos son pancreatitis leves, debe ajustarse la dosis de tratamiento, e incluso valorar sustituirlo por otro grupo terapéutico, como el metotrexato o la terapia biológica.
Tabla 1.
BIBLIOGRAFÍA
1.- Hypersensitivity to azathioprine in a patient with Crohn’s disease: a case report.
Sousa M, Proença L, Carvalho J. Rev Esp Enferm Dig. 2017 Sep 18;109. doi: 10.17235/reed.2017.5031/2017.
2.- Safety of azathioprine and 6-mercaptopurine in pediatric patients with inflammatory bowel disease.
Kirschner BS. Gastroenterology. 1998 Oct;115(4):813-21.
3.- Adverse events associated with azathioprine treatment in korean pediatric inflammatory bowel disease patients. Chun JY, Kang B, Lee YM, Lee SY, Kim MJ, Choe YH. Pediatr Gastroenterol Hepatol Nutr. 2013 Sep;16(3):171-7. doi: 10.5223/pghn.2013.16.3.171. Epub 2013 Sep 30.
4.- Three hospital admissions in 9 days to diagnose azathioprine hypersensitivity in a patient with Crohn’s disease. Mookherjee S, Narayanan M, Uchiyama T, Wentworth KL. Am J Ther. 2015 Mar-Apr;22(2):e28-32. doi: 10.1097/MJT.0b013e318296f153. JOP. 2015 Mar 20;16(2):136-42. doi: 10.6092/1590-8577/2951.
5.- Crohn’s disease and acute pancreatitis. A review of literature. Jasdanwala S, Babyatsky M. JOP. 2015 Mar 20;16(2):136-42. doi: 10.6092/1590-8577/2951.
6.- Enfermedad inflamatoria intestinal (I): clasificación, etiología y clínica. Enrique Medina. An Pediatr Contin. 2013;11(2):59-67
7.-Levine A, Griffiths A, Markowitz J, Wilson DC, Turner D, Russell RK, et al. Pediatric modification of the Montreal classification for inflammatory bowel disease: the Paris classification. Inflamm Bowel Dis. 2011; 17: 1314-21.
8.- Azathioprine: an update on clinical efficacy and safety in inflammatory bowel disease. Lamers CB, Griffioen G, van Hogezand RA, Veenendaal RA. Scand J Gastroenterol Suppl. 1999;230:111-5. Review.
9.- Azathioprine-induced Acute Pancreatitis in Patients with Inflammatory Bowel Diseases–A Prospective Study on Incidence and Severity. Teich N, Mohl W, Bokemeyer B, Bündgens B, Büning J, Miehlke S, Hüppe D, Maaser C, Klugmann T, Kruis W, Siegmund B, Helwig U, Weismüller J, Drabik A, Stallmach A; German IBD Study Group. J Crohns Colitis. 2016 Jan;10(1):61-8. doi: 10.1093/ecco-jcc/jjv188. Epub 2015 Oct 13.
10.- Azathioprine toxicity in Crohn’s disease: incidence, approach and course. Colli MV, Amaro TA, Pinto AL, Gaburri PD, Chebli JM. Rev Assoc Med Bras (1992). 2008 Sep-Oct;54(5):415-21. Portuguese
11.- Adverse events of thiopurine immunomodulators in patients with inflammatory bowel disease. López-Martín C, Chaparro M, Espinosa L, Bejerano A, Maté J, Gisbert JP. Gastroenterol Hepatol. 2011 Jun-Jul;34(6):385-92. doi: 10.1016/j.gastrohep.2011.03.023. Epub 2011 May 25.
12.- Are pancreatic autoantibodies associated with azathioprine-induced pancreatitis in Crohn’s disease?
Weersma RK, Batstra MR, Kleibeuker JH, van Dullemen HM. JOP. 2008 May 8;9(3):283-9.