La enfermedad de Parkinson es una enfermedad degenerativa del sistema nervioso central producida por la degeneración celular de la sustancia negra del mesencéfalo y la disfunción de los circuitos neuronales relacionados con el control de los movimientos corporales.
Los síntomas más típicos de la enfermedad son la bradicinesia (lentitud de los movimientos voluntarios), acinesia (ausencia de movimiento), la rigidez muscular y el temblor, si bien suelen coexistir otros síntomas tanto sensitivos como vegetativos, cognitivos y †afectivos... Es un trastorno propio de personas de edad avanzada, aunque existen formas de inicio juvenil.
Nota científica. ¿Qué conocemos sobre la enfermedad de Parkinson?
Dr. Alberto Ochoa Govin*
†* Doctor en Medicina. Especialista en Neurocirugía. Neurocirujano. Servicios de Neurología, Neurocirugía y Terapia del Dolor. Fundación Medico Preventiva y de la Clínica Médico Quirúrgica de Cúcuta y El Centro Integral de Especialistas de Cúcuta.
La enfermedad de Parkinson es una enfermedad degenerativa del sistema nervioso central producida por la degeneración celular de la sustancia negra del mesencéfalo y la disfunción de los circuitos neuronales relacionados con el control de los movimientos corporales.
Los síntomas más típicos de la enfermedad son la bradicinesia (lentitud de los movimientos voluntarios), acinesia (ausencia de movimiento), la rigidez muscular y el temblor, si bien suelen coexistir otros síntomas tanto sensitivos como vegetativos, cognitivos y †afectivos... Es un trastorno propio de personas de edad avanzada, aunque existen formas de inicio juvenil.
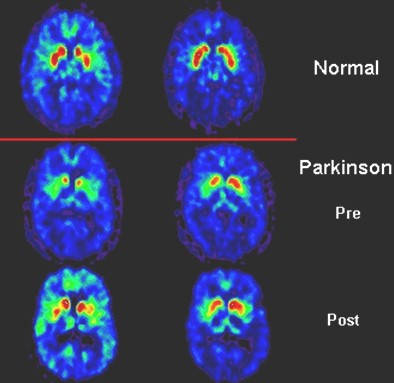
Pet Scan. Tomografía por emisión de positrones en un paciente normal y en un paciente con† enfermedad de Parkinson.
James Parkinson fue el que describió de forma detallada en 1817 los síntomas† de la enfermedad que† lleva su nombre. Si bien nuestros conceptos clínicos sobre la enfermedad se han modificado, la evolución asimétrica,† el curso de la enfermedad, la sintomatología temblorosa, la marcha festinante de aparición más tardía y el enlentecimiento motor fueron detallados de forma clara.
Parkinson también describió las alteraciones del lenguaje, la tendencia a las caídas y los trastornos del sueño, haciendo un preciso diagnóstico diferencial con otros tipos de temblor, en los que se puede reconocer el temblor fisiológico exagerado o el temblor esencial senil. Sus observaciones, basadas sorprendentemente en sólo 6 casos, sobre la historia natural de la enfermedad, fueron introducidas con disculpas por la falta de una interpretación patológica de la afectación de las funciones motoras que él había descrito. Concluyendo que la parálisis agitante era el resultado de una enfermedad de la médula espinal, extendiéndose hasta afectar al bulbo raquídeo. La ausencia de alteración del intelecto y el juicio indicaban que no había extensión al encéfalo.
Las contribuciones realizadas durante la primera mitad del siglo† aportaron muy pocas novedades a las descritas por Parkinson. Gracias a las contribuciones de los neurólogos franceses, especialmente Trousseau, Charcot y sus discípulos el cuadro cambio. Trousseau contribuyó a la descripción clínica de la enfermedad con su concepto de rigidez muscular; atribuyó la marcha festinante al trastorno postural, el cual causaba un desplazamiento del centro de gravedad, obligando al paciente a ir en su búsqueda; definió la bradicinesia como un enlentecimiento progresivo en los movimientos repetidos, y llamó la atención sobre el deterioro intelectual y la pérdida de memoria cuando la enfermedad avanzaba. Charcot amplió más tarde la descripción clínica, diferenciando el temblor parkinsoniano del temblor intencional. Ultimó que la impotencia motora era en parte debida a la rigidez muscular de cuello, cuerpo y extremidades, describiendo la postura característica, la tendencia a la propulsión y retropulsión, la pérdida del equilibrio y la micrografía del paciente parkinsoniano.
A principios de siglo los estudios neuropatológicos de la enfermedad de Parkinson se centraron esencialmente en las lesiones de los núcleos grises centrales y particularmente en el globo pálido. La participación crucial del locus niger en la patología de la enfermedad de Parkinson fue demostrada por Tretiakoff, aunque fue propuesta por primera vez por Brissaud. La lesión histológica más característica de la enfermedad de Parkinson, denominada cuerpos de Lewy, consiste en las inclusiones intracitoplasmáticas hialínicas y acidófilas que describió por primera vez Lewy.
La evidencia de un trastorno dopaminérgico en la enfermedad de Parkinson fue descrita por Ehringer y Hornykiewicz en 1960. Estos autores midieron las concentraciones de dopamina y noradrenalina en varias regiones del cerebro postmortem de dos pacientes con enfermedad de Parkinson y cuatro que habían presentado un parkinsonismo postencefalítico, y lo compararon con los resultados obtenidos en la corea de Huntington y otras alteraciones de los ganglios basales, y en 17 controles. Encontraron una disminución muy marcada en el estriado de los pacientes con parkinsonismo postencefalítico e idiopático, siendo estos resultados confirmados posteriormente en múltiples estudios.
En 1963 Carlsson y Linquist propusieron por primera vez la existencia de receptores dopaminérgicos en el cerebro. Spano et al en 1978 sugirieron que los receptores de la dopamina eran dos poblaciones diferentes en la que uno de ellos estaba directamente unido a la activación de la adenilciclasa, concepto que ha permanecido estable durante muchos años.
La enfermedad de Parkinson (EP) es un proceso degenerativo cerebral de etiología desconocida. Los cuerpos de Lewy se consideran su marcador morfológico, pero no existe un marcador biológico que permita su diagnóstico en vida del paciente. A pesar de que la semiología de la enfermedad es característica, en torno a cuatro de cada diez enfermos están sin diagnosticar, y no es extraño errar el diagnóstico; esto se debe a que su expresión clínica es variable y a que comparte con otros procesos muchas de sus manifestaciones. El diagnóstico de las enfermedades crónicas sin un marcador definitivo, como es la enfermedad de Parkinson, es una cuestión de probabilidades.
En general, se emplean unos criterios cuyo valor se establece en series con verificación necrópsica, ya que el diagnóstico certero es morfopatológico.
El diagnóstico clínico de enfermedad de Parkinson se basa en la existencia de tres datos universalmente considerados cardinales: bradicinesia, rigidez y temblor. La lentitud, torpeza y disminución, o incluso ausencia de movimientos espontáneos e inducidos, es generalmente el trastorno motor de mayor envergadura en la enfermedad de Parkinson. En sentido estricto, se entiende por acinesia la falta de movilidad o imposibilidad de realizar un movimiento. Se reconoce más fácilmente en la pobreza de movimientos automáticos, tales como el parpadeo, el braceo, las sinergias posturales, entre otros, pero también en otras actividades, como por ejemplo la reducción en la longitud de la zancada de la marcha, la micrografía o incluso la característica hipometría de los movimientos rápidos (balísticos). La rigidez consiste en un aumento del tono muscular tanto en músculos flexores como extensores. El aumento en la resistencia durante el movimiento articular (inducido por el explorador) es la característica más común asociada con la rigidez. Típicamente se hace más manifiesta cuando se mueve la articulación lentamente, suele acompañarse del fenómeno de la «rueda dentada» y se intensifica con los movimientos voluntarios de otras partes del cuerpo. El temblor parkinsoniano aparece típicamente en reposo y se inhibe durante el inicio de un movimiento voluntario. Consiste en una actividad rítmica alternante (4-6 Hz) entre grupos musculares agonistas y antagonistas que provoca el desplazamiento rítmico de una articulación.
En la enfermedad de Parkinson el temblor de reposo afecta preferentemente a las articulaciones distales, pero existe un temblor postural, de mayor frecuencia (7-12 Hz), que involucra también las articulaciones proximales, e incluso los músculos de la cara.
La marcha parkinsoniana tiene varias características. Antes de su inicio, durante la bipedestación estática, existe una postura flexora de cuello, tronco y rodillas, a la que se asocia usualmente una aducción de extremidades superiores («como pegadas») al tronco. El hecho clínico más impactante de la marcha en la enfermedad de Parkinson es la facilidad con que se bloquea, dando lugar a momentos de inmovilización motora. El enfermo parkinsoniano tiene otros muchos síntomas y signos, como seborrea, alteraciones autonómicas, entre otros, que no forman parte de los criterios diagnósticos.
La etiología y los mecanismos patogénicos de la enfermedad de Parkinson son, y posiblemente seguirán siéndolo durante muchos años, desconocidos. Se ha sugerido que la causa de la enfermedad de Parkinson sería multifactorial, interviniendo en ella factores genéticos y ambientales y el envejecimiento. Sin embargo, no existen datos suficientes que apoyen alguno de estos factores como único responsable, e incluso se ha sugerido la posibilidad de que con el término enfermedad de Parkinson se designen varias enfermedades diferentes. Los datos que se conocen en la actualidad apoyan la etiología multifactorial de la enfermedad de Parkinson, la cual podría ser el efecto de la interacción de los siguientes factores:
1.†††† El envejecimiento.
2.†††† Susceptibilidad genética.
3.†††† Factores ambientales.
El papel de las infecciones y traumatismos como factor de riesgo es muy improbable. Por otro lado, ningún tóxico ambiental ha sido demostrado como factor de riesgo en todos los estudios epidemiológicos realizados al respecto. La vida en el medio rural y el hábito de no fumar y de no beber (aunque es muy difícil que puedan interpretarse como factor protector) son las variables sugeridas como posibles factores de riesgo en la mayoría de estudios epidemiológicos.
La patogenia de la enfermedad de Parkinson es también desconocida, a pesar de los numerosos datos descritos y de los mecanismos propuestos. Probablemente debemos asumir, de acuerdo con Ben Shlomo, que aún estamos muy lejos de conocer la causa de la enfermedad de Parkinson.
Partiendo del conocido déficit dopaminérgico, secundario a la degeneración de la sustancia negra pars compacta (SNpc), se producen una serie de modificaciones en la fisiología de los ganglios basales y sus proyecciones que representan el sustrato anatomofuncional del síndrome parkinsoniano. En la enfermedad de Parkinson pueden distinguirse tres categorías de síntomas y signos:
1.†††† Las alteraciones motoras (rigidez, acinesia-bradicinesia, temblor, bloqueos y otras anomalías de la marcha, distonía, entre otras), que suponen el elemento esencial y cardinal del cuadro clínico.
2.†††† Trastornos emocionales (depresión, ansiedad, cambios de carácter y aislamiento, entre otros) y cognitivos (bradifrenia, trastornos de atención, percepción temporal, entre otros).
3.†††† Síntomas sensitivos (dolor, parestesias y disestesias, calambres) y manifestaciones autonómicas (rubor, sudoración, taquicardia, seborrea, estreñimiento, impotencia, entre otros).
La historia natural de la enfermedad de Parkinson (EP) se ha modificado notablemente desde la introducción de la levodopa (LD) hace casi 30 años. La levodopa, que continúa siendo uno de los† fármacos más potentes y eficaces en el tratamiento de la enfermedad de Parkinson, ha prolongado la supervivencia de los pacientes con enfermedad de Parkinson y ha mejorado su calidad de vida; sin embargo, ha dado lugar a una serie de problemas desconocidos antes de su utilización.
Poco tiempo después de las primeras descripciones de la eficacia terapéutica de la levodopa en la enfermedad de Parkinson, Cotzias et al y Barbeau observaron, en pacientes tratados con levodopa durante más de 2 años, el comienzo de modificaciones transitorias de su función motora. Los enfermos sufrían, a veces súbitamente, la reaparición de los signos parkinsonianos durante períodos variables de tiempo, sobre todo por las tardes. Estas fluctuaciones de la movilidad eran diferentes de las variaciones en la intensidad de los síntomas observadas en pacientes parkinsonianos que nunca habían sido tratados con levodopa, tales como episodios de «congelación», agravamiento del temblor con la tensión emocional, situaciones de cinesia paradójica habitualmente desencadenadas por emociones intensas, o la mejoría de los signos parkinsonianos que algunos pacientes experimentaban con el sueño. Las fluctuaciones motoras afectan al 40-50% de los pacientes tratados con levodopa durante 5 años y aproximada-mente al 80% de los enfermos tratados durante 10 años, por lo que la prevalencia acumulada anual de esta complicación motora, una vez iniciada la levodopaterapia† se aproxima al 10%.
La mayoría de los pacientes con fluctuaciones motoras sufren también la aparición de uno o varios tipos de discinesias, siendo ambas las principales complicaciones motoras del tratamiento crónico con levodopa.
Fluctuaciones motoras y discinesias pueden provocar una importante incapacidad funcional en los pacientes, y constituyen, en la actualidad, el más frecuente y difícil problema terapéutico de la enfermedad de Parkinson.
En la actualidad, se puede realizar el diagnóstico prácticamente en el ciento por ciento de las personas con esta dolencia, cuando hace apenas 20 años la imprecisión rondaba el 30%. También es posible establecer un tratamiento eficaz durante años y realizar la cirugía cuando es valorada como beneficiosa por los especialistas en este padecimiento.
El Parkinson es una enfermedad que origina la pérdida de neuronas de manera lenta y progresiva, principalmente en la zona del cerebro donde se fabrica la dopamina, una molécula encargada de controlar y facilitar las actividades motoras. Es como el diabético que le falta la insulina.
Por tanto, cuanto menos dopamina exista, habrá menos agilidad en los movimientos. Esa es la razón por la cual la marcha en estos pacientes se va haciendo cada vez más lenta, más difícil la escritura, parpadean menos y puede aparecer temblor o rigidez en los músculos.
Esta enfermedad, además de los desórdenes motores que produce, puede generar también trastornos emocionales y conductuales, en lo que se realiza actualmente un notable esfuerzo investigativo.
Las ciencias médicas están en capacidad de "reponer" con medicamentos la falta de dopamina. Atendiendo a que este padecimiento es de carácter progresivo, la pérdida de dopamina se va acentuando con el decursar del tiempo, lo que comporta que los efectos de los fármacos sean menos óptimos. "La eficacia terapéutica disminuye† porque no es posible modular el efecto de la dopamina, y es entonces cuando la cirugía desempeña un papel de importancia en el tratamiento".
En los años 1990 los investigadores del tema descubrieron que a menor existencia de dopamina, se producían más alteraciones en la actividad de las neuronas, comprometiendo también una zona del cerebro denominado "núcleo subtalámico" cuya función normal es ejercer el control de los movimientos (literalmente frenar), a fin de que no se originen movimientos indeseados. "Es como un policía que regula la velocidad del tránsito".
Hoy en día existen tres modalidades de tratamiento quirúrgico para la enfermedad de Parkinson: cirugía ablativa, estimulación cerebral profunda (ECP) y neurotrasplante (tratamiento restaurativo). Las dos primeras tienen un efecto más compensador que corrector del defecto bioquímico de la enfermedad. Sin embargo, la última modalidad intenta corregir éste defecto al reemplazar la pérdida de células dopaminérgicas o promover la sobrevida de las existentes.
En la aplicación y desarrollo de la cirugía ablativa y la estimulación cerebral profunda se han destacado dos estructuras nucleares consideradas como los blancos quirúrgicos de elección: tálamo motor, a nivel del núcleo ventralis intemedialis (Vim) y la región posteroventral del globo pálido interno (GPi). La talamotomía y la estimulación crónica del tálamo continúan siendo realizadas, fundamentalmente, para el control del temblor, mientras la palidotomía, proceder retomado por Laitinen resulta efectiva, al igual que la estimulación crónica del pálido interno, para mejorar muchos signos motores de la enfermedad.
Una de las cirugías más aceptadas en reconocidos centros neuroquirúrgicos del mundo y que se practica en la actualidad es la subtalamotomía dorso-lateral selectiva, que consiste en la eliminación de las zonas de esa estructura del cerebro que funcionan en exceso y generan una situación anormal del control de los movimientos.
El núcleo subtalámico (NST) es considerado por varios autores como un blanco preferido en la cirugía de la enfermedad de Parkinson (EP).
Los estudios experimentales con lesiones del núcleo subtalámico, han mostrado efectividad en mejorar todos los signos motores de la enfermedad de Parkinson en monos. MPTP (1-metil-4-fenil-1, 2, 3,6-tetrahidropiridina) y otros modelos. Igualmente fueron consideras efectivas las lesiones en la región subtalámica de pacientes con enfermedad de Parkinson realizadas en la década del sesenta, aunque muchas de ellas no eran verdaderas lesiones del núcleo subtalámico y se extendían en toda región subtalámica, incluyendo la zona incerta, sustancia negra pars reticulata (SNpr), campos de Forel-H2 y tálamo.
La subtalamotomía dorso-lateral selectiva, con lesiones solamente confinadas a la región sensoromotora del núcleo subtalámico se realizaron posteriormente en humanos.
Aunque la estimulación cerebral profunda† (ECP) del subtálamo en pacientes con enfermedad de Parkinson ha sido favorecida, la ablación del núcleo subtalámico cada vez es realizada por mayor número de investigadores en varios países. Aunque actualmente existen diferencias en los métodos descritos para la localización y lesión del núcleo subtalámico.
Por la forma, tamaño y posición espacial del núcleo subtalámico, su ablación requiere de una técnica quirúrgica particular para cada paciente y un método de evaluación clínica junto a la comprobación real de las lesiones que permita evaluar la seguridad y efectividad del procedimiento quirúrgico.
La "batalla pendiente" en el tratamiento del Parkinson, objetivo prioritario de las investigaciones en el campo de las neurociencias en los próximos años, es detener el proceso degenerativo de la enfermedad, impedir que avance y, a mediano plazo, incluso curarla. Esto constituye un reto y un problema a solucionar por la neurología y neurocirugía funcional moderna.