Así, cuando el factor IXa llega a la superficie plaquetaria forma el complejo tenasa junto al factor VIIIa. Este factor IXa proviene de 2 mecanismos:
1. Activación del FIX por FT/FVIIa sobre la célula portadora de FT y difusión del FIXa hacia la superficie plaquetaria (este factor no es inhibido por la antitrombina u otros inhibidores circulantes).
2. Activación del FIX por el FXIa, mediante dos vías: la primera sería la unión del FXI a las plaquetas y su activación por la trombina generando FIX y la segunda es la activación del FXI a través de la fase de contacto de la coagulación (vía intrínseca).
Una vez ensamblado el complejo FIX/VIIIa sobre la superficie plaquetaria, el FX es activado a FXa y junto a su cofactor FVa, forman el complejo “protrombinasa”, produciendo lo que se denomina “el estallido” de trombina, en cantidades suficientes para formar el coágulo de fibrina. El modelo celular presentado no considera la activación del sistema de coagulación a partir de la denominada “fase de contacto” (modelo tradicional de las vías extrínsecas y intrínsecas), sino que ocurre simultáneamente con la iniciada por el FT, pero a diferente velocidad.
Sistema de contacto de la hemostasia.
El sistema de contacto está formado por: FXII, precalicreína (PK), FXI y quininógeno de alto peso molecular (HMWK). La unión del factor XII plasmático a superficies cargadas negativamente induce su autoactivación que desencadena la activación del sistema de contacto. El factor XIIa adquiere actividad proteolítica, siendo sus sustratos principales el FXI y precalicreína, generando XIa y calicreína. El FXI y PK están en el plasma formando un complejo con el HMWK, que también tiene afinidad por superficies cargadas negativamente, por lo tanto actúa como cofactor y facilita la interacción de la enzima (FXIIa) con sus sustratos (FXI y PK).
La calicreína (K) generada puede activar más FXII y también hidrolizar al HMWK, liberando un fragmento denominado bradiquinina y dejando al resto de la molécula como un quininógeno activo de menor peso molecular, con mayor afinidad de unión a superficies con cargas negativas y por lo tanto mayor fijación de los sustratos para el FXIIa. La bradiquinina es un mediador vasoactivo y proinflamatorio, que induce la liberación de t-PA y prostaciclinas de la célula endotelial, por lo tanto, el FXI se activa por la trombina en un “feed-back” positivo y también por el sistema de contacto.
El FXIa convierte al FIX en IXa, el cual junto a su cofactor VIIIa, activa al FX a FXa. Esta última activación (FX a FXa) también se produce por acción del FT-FVIIa, pero la ejercida por el complejo FIXa-FVIIIa es de mayor eficacia. De aquí surge la importancia del déficit de FVIII y FIX, responsables de la hemofilia A y B respectivamente.
Se conocen deficiencias en las proteínas involucradas en el sistema de contacto (PK, HMWK, FXII) las cuales no están asociadas con episodios de sangrado. El sistema de contacto explica la coagulación de la sangre in vitro. Finalmente la trombina generada por el complejo protrombinasa, cliva los fibrinopéptidos A y B del fibrinógeno, generando una red de fibrina que inicialmente es soluble y por acción del FXIIIa (una transglutaminasa), y en presencia de Ca2+, se transforma en fibrina insoluble que es el coágulo estable (la misma trombina es la que activa al FXIII a FXIIIa).
La activación del sistema de coagulación debe estar regulada por otro sistema: el de los inhibidores fisiológicos. Los más importantes son: el TFPI (inhibe el complejo FT-VIIa y el FXa), la antitrombina (inhibe la trombina, FXa, FIXa, FXIa, FXIIa), el cofactor II de la heparina (inhibe la trombina), el C1-inhibidor (inhibe FXIIa, FXIa, calicreína), el sistema trombomodulina PC-PS (inhibe FV, FVa, FVIIIa). Ya una vez conformado el coágulo y localizado en el sitio de la lesión, el sistema plasminógeno-plasmina se encarga de la disolución del mismo, donde actúa como un sistema fibrinolítico y facilita la reparación del vaso.
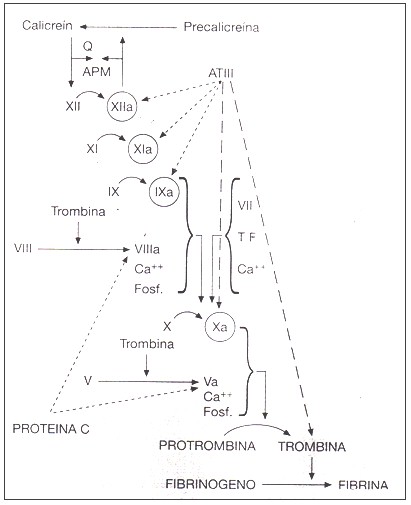
Fig. 2. Sistema de contacto de la coagulación
Sistema de micropartículas. Activación del sistema de coagulación
Por consenso internacional (2004) se define a las micropartículas como: partículas plasmáticas menores a 1 µ de diámetro, portadoras de antígenos de superficie de sus células de origen, es decir, sus características proteómicas y receptores de superficie. Son fragmentos celulares que se encuentran circulando y que se originan a partir de células endoteliales, plaquetas, eritrocitos y monocitos.
Cuando estas células son activadas por estímulos físicos o químicos (hipoxia, estrés, IL-6, TNFα) se produce una reorganización del citoesqueleto de membrana, con la consiguiente formación de vesículas y liberación de las micropartículas, es decir, durante su formación se modifica la bicapa lipídica de la membrana, exponiendo una superficie rica en fosfolípidos cargados negativamente (micropartículas), las cuales constituyen el soporte para la unión de los factores y complejos de la coagulación (función de las plaquetas).
Se ha demostrado que las micropartículas puede expresar factor tisular (actividad procoagulante), por lo tanto pueden iniciar y mantener la coagulación, ya no solo en el sitio de la injuria, sino donde se localizan estas micropartículas (endotelio, plaquetas, leucocitos).