En una sociedad donde han disminuido las epidemias y las pandemias, las causas de muerte han sido relegadas a otras patologías como, por ejemplo, la cardiopatía isquémica (CI). Esta es, sin lugar a dudas el problema de salud más difundido en el mundo de hoy.
Es la CI la verdadera pandemia del siglo XXI, y la primera causa de muerte, superando el 50% del total de fallecimientos. Produce un alto porcentaje de invalidez físico psíquica, así como enormes costos económicos, que superan los 140 000 millones de dólares al año en los Estados Unidos en gastos directos e indirectos.
INTRODUCCIÓN
En una sociedad donde han disminuido las epidemias y las pandemias, las causas de muerte han sido relegadas a otras patologías como, por ejemplo, la cardiopatía isquémica. Esta es, sin lugar a dudas el problema de salud más difundido en el mundo de hoy. 1-3
Es
Dentro de las diversas formas clínicas de presentación del Síndrome Coronario Agudo (SCA), es el Infarto del Miocardio, el que reviste la mayor mortalidad y letalidad. En los Estados Unidos cerca de 1.5 millones de personas sufren un Infarto Agudo del Miocardio cada año, con una mortalidad en el primer año de evolución que oscila entre un 10 y un 15%, siendo el riesgo de muerte por esta causa
En Cuba se han realizado estudios de mortalidad por infarto agudo del miocardio, los cuales han demostrado que la misma se mantiene elevada, en el año 2003 la incidencia de infarto agudo del miocardio en Cuba fue de 1.7 por mil habitantes mayores de 15 años,Ā con 8 720Ā fallecidos y una letalidad de 65.2%. En nuestra provincia la tasa por enfermedades cardiovasculares es de 215.26 por 100 000 habitantes. La tasa de infarto agudo del miocardio en Villa Clara es de 109.33 por 100 000 habitantes. La tasa estandarizada de cardiopatía isquémica es de 135.2 por 100 000 habitantes. El 28.2% de las muertes por infarto agudo del miocardio han ocurrido en el hogar, el 8.2% en camino al hospital, y el 14.5% en las unidades hospitalarias de urgencia (UHU) de los hospitales o policlínicos. Es decir que el 50.4% de las defunciones por infarto agudo del miocardio en la provincia de Villa Clara, han ocurrido antes de ingreso en las Unidades deĀ Cuidados Intensivos (UCI). La letalidad general en nuestra provincia oscila entre el 8% y el 14%.7
El manejo del infarto agudo del miocardio ha sufrido un cambio radical en los últimos años, lo cual se debe a una mejor comprensión de la fisiopatología del mismo, la relación con la disfunción microvascular, el rol de la inflamación en la enfermedad arterial coronaria así como la comprensión de la placa deĀ ateroma y la hemorragia intraplaca, conllevando de hecho al argumento de toda una serie de nuevas intervenciones terapéuticas, cuyo esencial objetivo es la restauración del flujo sanguíneo a las áreas musculares comprometidas. 8-12
Hace algún tiempo, se ha dirigido la atención cardiológica al perfeccionamiento de los procederes capaces de lograr la reperfusión del miocardio isquémico, dentro de los que se destacan por su eficacia en la recanalización de la arteria relacionada con el infarto y su bajo costo; la trombolisis coronaria, utilizándose agentes capaces de activar el sistema fibrinolítico del organismo y degradar el trombo oclusivo intracoronario. Esto incide de forma significativa sobre la evolución y complicaciones durante la fase aguda del evento coronario, contribuyendo de forma significativa a evitar los fenómenos de expansión y remodelado del área infartada, así como a la preservación de la función ventricular izquierda, la cual tiene especial valor como pronóstico predictivo de supervivencia a corto y largo plazo; de ahí que en la actualidad uno de los procederes más utilizados en el manejo del infarto agudo del miocardio sea el empleo de agentes fibrinolíticos. 13-20
El pronóstico del infarto agudo del miocardio ha mejorado mucho en los últimos años debido a la amplia utilización durante su fase aguda del tratamiento trombolítico, y de procederes intervencionistas como la angioplastia transluminal percutánea con balón (ACTP) y la cirugía coronaria revasculizadora de urgencia en un intento de reabrir la arteria relacionada con el infarto (ARI) y reducir el tamaño del mismo.5-6,21-25.
Se han diseñado múltiples aproximaciones terapéuticas para el tratamiento del infarto agudo del miocardio. A principios de los años 60 cuando comenzó a utilizarse, lo que su descubridor, Sodi PallarésĀ llamó «solución polarizante» y actualmente se conoce como solución GIK (Glucosa-Insulina-Potasio) el tratamiento del infarto agudo del miocardio era desalentador, pues apenas habían tratamientos específicos, se desconocía el efecto de los fibrinolíticos y muchos pacientes desarrollaban y fallecían por arritmias ventriculares malignas.26 Ā
Sodi Pallarés propugnó la utilización de una infusión de GIK en perfusión para el tratamiento de la fase aguda del infarto cardiaco, observando una disminución de la mortalidad, que él explicaba por varios mecanismos a saber: prevención de arritmias, aportes de nutrientes a las células hipóxicas, disminución del tamaño del infarto agudo del miocardio, etc.27
El tratamiento propugnado en aquella época consistía en una infusión de glucosa al 10% con 40 meq de cloruro de potasio y 20 unidades de insulina por cada litro de solución preparada, en administración intravenosa lenta (1.5 l/día). Tal tratamiento se administraba una, dos o tres veces a la semana o de forma continua durante dos o tres días, o incluso de una semana a un mes. Posteriormente Sodi PallarésĀ añadió al tratamiento la dieta baja en sodio y rica en agua, ante la posibilidad de que la perdida de sodio celular favoreciera la entrada de potasio. 26-27
No obstante a esto, los resultados no fueron concluyentes ni satisfactorios, en parte porque no se asociaban a la aplicación de métodos de reperfusión, y por otro lado los estudios realizados carecían de una muestra representativa y de la utilización de una metodología adecuada para avalar este proceder. Por este motivo se consideró posterior a estos primeros ensayos, que las soluciones de GIK no conseguirían un mayor descenso de la mortalidad, por lo que su uso se abandonó Āy quedó restringido a un pequeño número de centros; ante el empuje de nuevos tratamientos con demostrada eficacia como los betabloqueadores, antiagregantes plaquetarios y agentes trombolíticos.
Últimamente, sin embargo, se ha replanteado su utilidad y se han emprendido nuevos estudios que parecen confirmar las experiencias antiguas 27-28. Datos experimentales recientes apoyan que la infusión de GIK en el contexto del miocardio reperfundido/isquémico produce un impacto impresionante en la evolución del miocardio dañado pero viable, cuando es añadido temprano durante el periodo isquémico. Los resultados de las pruebas clínicas pilotos confirmaronĀ que una estrategia metabólica de modulación en las primeras horas de infarto agudo del miocardio con una infusión de GIK es factible, aplicable con efectos colaterales benignos. Un metanálisis de todas las pruebas de GIK realizadas al azar en el infarto agudo del miocardio que incluyó cerca de 2000 pacientes y 350 fallecidos, mostraronĀ una reducción consistente en la mortalidad del 28%.26-29
En cuanto al uso del Magnesio (Mg) en el infarto agudo del miocardio; algunos estudios epidemiológicos geosanitarios han demostrado que los índices deĀ mortalidad cardiaca son mayores en las áreas donde las concentraciones de Magnesio en el suelo y en el agua son menores.
Por otro lado, varios estudios preliminares han sugerido que el Mg podría ser capaz de limitar el tamaño del área infartada. La causa de este efecto beneficioso del Mg, se ha atribuido a que un descenso de la concentración extracelular de Mg, incrementa el tono arterial coronario y aumenta la sensibilidad a los vasoconstrictores. Por otro lado, poco después del comienzo de la isquemia miocárdica, el Mg podrá limitar la progresión patológica hacía el infarto y reducir el riesgo de arritmias inducidas por el incremento de los niveles de Mg, además limitar el daño miocárdico al inhibir la entrada de calcio en las células miocárdicas y/o al reducir la resistencia vascular periférica.30
En un estudio conjunto del Instituto Nacional de Salud (NIH), USA, y de
Los autores de este amplio metanálisis llegan a la conclusión de que la aplicación endovenosa de Mg, con alta probabilidad, tiene un efecto beneficioso en la mortalidad temprana cuando se sospecha de IMA. Ellos también hacen referencias a estudios muy amplios como elĀ ISIS 4, con los cuales se pretende aclarar si una infusión de Mg, en adición a un tratamiento con betabloqueadores a un tratamiento fibrinolítico y a un tratamiento oral con Aspirina, es terapéuticamente efectivo.31, 32
Atendiendo a estos resultados nuestras dos preguntas científicas serían:
1.- ¿Podrá la infusión intravenosa temprana de solución GIK reducir la mortalidad en el IMA sometido a tratamiento trombolítico?
2.- ¿Podrá la infusión intravenosa temprana de Mg reducir claramente la mortalidad cuando se sospecha de IMA?
OBJETIVOS
GENERAL
1-. Comparar los resultados de los tratamientos del Infarto Agudo del Miocardio trombolizado con el uso o no de infusión endovenosa de Glucosa-Insulina-Potasio (GIK) y en el infarto no trombolizado la terapéutica con infusión de Sulfato de magnesio.
ESPECIFICOS
1-. Identificar la influencia de algunas variables Epidemiológicas y Clínicas sobre los resultados de los tratamientos.
2-. Describir las reacciones adversas por el uso de trombolíticos, sulfato de Magnesio y solución de Glucosa- Insulina- Potasio.
3-. Diferenciar la letalidad en sus aspectos disfuncionales, así como las complicaciones presentadas.
Operacionalizacion de las variables:
Variables clínico epidemiológicas que fueron analizadas (Ver encuesta):
- Edad: se tomó como mínima la menor encontrada (28 años) y para mejor interpretación y comparación fueron agrupados: 28-39; 40-49; 50-59; 60-69; 70-79; 80 y más años.
- Sexo. Se considero en masculino y femenino.
- Tiempo entre el comienzo de los síntomas y el inicio del tratamiento: hasta 60 min.,entre 61y 120 min., entre 121y 180 min., entre 181 y 240 min., entre 241 y 300 min., entre 301 y 360 min., 361 min. Y 12 h y más de 12h.Ā
- Antecedentes de cardiopatía isquémica previa.
- Factores de riesgo coronario (FRC): Hábito de fumar, hipertensión arterial (HTA), stress, sedentarismo, diabetes mellitus (DM), hipercolesterolemia y obesidad. Los FRC fueron definidos según varios autores.
-Tipo de IMA: No Q y Q.
Complicaciones cardiovasculares, tuvimos en cuenta las siguientes:
a- Fallo de bomba clase Killip-Kimball.
Ausencia de estertores pulmonares o de tercer ruido.
Estertores pulmonares hasta un 50% o menos de los campos pulmonares o presencia de tercer ruido.
III.- Estertores pulmonares de más de un 50% de los campos pulmonares (edema agudo del pulmón).
IV.- Choque cardiogénico: Caída de la presión arterial sistólica hasta 90 mmHg o menos con oliguria (< 30 ml/h) y signos de sufrimiento tisular.
Āb- Trastornos del ritmo: Se incluyeron tanto las arritmias de reperfusión (aparecen en las primeras dos horas de aplicación del Trombolítico, son de corta duración y fácil manejo),Ā como las de no reperfusión (propias del IMA) que fueron diagnosticadas de acuerdo a criterios establecido
Āc- Re-infarto: Nuevo infarto que sucede posterior a un IMA previo, y que puede ocurrir en zonas adyacentes o lejanas en relación con la necrosis inicial, durante el ingreso y requiere de uno de los siguientes criterios:
1- Aparición de nuevas ondas Q patológicas con cambios evolutivos del segmento ST y de onda T durante el ingreso cuyo ECG aparentemente se había estabilizado.
2- Dolor torácico sugestivo de isquemia miocárdica, después de haber estado más de 24 horas sin dolor, con elevación de
d- BRIHH.
e- Angina post-IMA: Cuando aparece dolor anginoso típico después de las primeras 24 horas del IMA, acompañado de cambios transitorios en el ECG: elevación o depresión del segmento ST o de la onda T (inversión o positivización) durante el episodio doloroso.
f- Tromboembolismo pulmonar: Tuvimos en cuenta elementos clínicos, electrocar-diográficos, radiológicos y necrópsicos.
g- Insuficiencia cardiaca: Tuvimos en cuenta elementos clínicos,Ā electrocardiográficos, radiológicos y necrópsicos.
h- Bloqueo AV de III grado: hay disociación de los ritmos auricular y ventricular. Ningún estimulo generado en las aurículas puede pasar a los ventrículos y BAVĀ de ΙΙ grado.
Complicaciones no cardiovasculares, tuvimos en cuenta los siguientes:ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ
Bronconeumonía hipostática, íleo paralítico, sepsis urinaria y gastritis medicamentosa aguda.
Miocardio viable: Se entiende por miocardio lesionado pero viable aquel que manifiesta una mejoría funcional si se reperfunde de forma adecuada.
Efectividad: Es el efecto producido cuando el procedimiento es aplicado en condiciones medias, habituales, reales, es decir en la práctica habitual con los medios disponibles, en la práctica del día a día.
Eficacia: Es el efecto producido en la variable a evaluar cuando las intervenciones son aplicadas en condiciones ideales o de laboratorio, como en un ensayo clínico aleatorizado.
Utilidad: El resultado de la intervención es medido en términos de calidad de vida y su duración.
Beneficio: El resultado es medido en valor monetario.
Calidad de vida: Bienestar social, fisiológico, mental, intelectual y general de la persona.
Letalidad: Total de fallecidos por una causa entre total de enfermos por esa causa en un período de tiempo y un área determinada.
Fase aguda: Primeras 72 horas de iniciado el cuadro agudo.
Fase intrahospitalaria: Después de las 72 horas y hasta el egreso del paciente.
La hipercolesterolemia fue valorada por antecedentes referidos por el paciente de aumento de las cifras de colesterol previo al IMA.
Material y Método:
Se realizó un estudio analítico-comparativo transversal de 4 grupos de pacientes adultos ingresados en
1.- Pacientes con IMA tratados con betabloqueadores y Aspirina (todos ingresados desde 1988 hasta el 1║ de octubre de 1993, cuando comenzó la trombolisis con Heberkinasa cubana en nuestro hospital): IMA
2.- Pacientes con IMA tratados con trombolisis, betabloqueadores y Aspirina desde 1993 hasta el 2003: IMA-T
3.- Pacientes con IMA sin criterios de trombolisis, tratados con Sulfato de Mg, betabloqueadores y Aspirina desde 1993 hasta el 2003:IMA-Mg
4.- Pacientes con IMA tratados con trombolisis, solución GIK, betabloqueadores y Aspirina desde el 1║ de junio de 1998 hastaa el 31 de diciembre del 2003, los pacientes con IMA y criterios de trombolisis quedan divididos en 2 subgrupos; un primer subgrupo (los números pares) a los cuales se le realizó tratamiento con trombolisis, betabloquedores y Aspirina y un el otro subgrupo (los números impares) a los cuales conjuntamente con la aplicación de la terapia trombolítica, se les administró una infusión de GIK por vía endovenosa, betabloqueadores y Aspirina: IMA-T-GIK.
Posteriormente a la revisión documental sobre el tema, se localizaron los datos primarios en el libro de Registro de
Los criterios para el diagnóstico de IMA, fueron emitidos por
Infarto Miocárdico Agudo: Es la necrosis o muerte celular de un territorio determinado del corazón de forma aguda, debido a un déficit parcial o total de su irrigación sanguínea.
Lesión celular: Es la que ocurre cuando el grado de injuria sobrepasa la capacidad de adaptación de la célula y que puede llegar a ser irreversible.
IMA de onda Q: Aparecen ondas Q patológicas o QS con topografía manifiesta.
IMA no Q o ST-T: Hay cambios evolutivos del segmento ST y la onda T, sin aparición de ondas Q patológicas o QS en el ECG.
Supradesnivel del segmento ST: se considera cuando está presente en al menos dos derivaciones contiguas, siendo 0,1 mV en derivaciones frontales y 0,2 mV en derivaciones precordiales.
IMA transmural: Infarto que produce una necrosis que afecta toda la pared ventricular. Generalmente aparecen ondas Q en el ECG.ĀĀ
Criterios enzimáticos: a todos los pacientes se le realizó Transaminasa Glutámico Oxalacético (TGO) seriada, de poco valor al igual que
Criterios electrocardiográficos inequívocos de IMA:
ĀĀĀ Presencia de onda Q patológica o QS con topografía.
ĀĀĀ Supradesnivel evolutivo del segmento ST.
ĀĀ ĀBloqueo de rama izquierda del Haz de His (BRIHH) agudo.
Criterios equívocos de IMA:
ĀĀĀ Presencia de onda Q o QS en una sola derivación del ECG.
ĀĀĀ Supradesnivel no evolutivo del segmento ST.
ĀĀĀ Onda T invertida.
Criterios de inclusión para la administración del tratamiento trombolítico24
Dolor en la cara anterior del tórax, típico de Isquemia Miocárdica, de más de 30 minutos de duración, resistente a los nitritos de acción rápida por vía sublingual, con menos de 12 horas de evolución y en pacientes de cualquier edad y sexo.
Supradesnivel del segmento ST en el ECG, de más de 1mm en las derivaciones DI, DII, DIII, AVL y AVF, o de más de
Que no existan contraindicaciones para la aplicación del tratamiento trombolítico.
Criterios de exclusión para la administración del tratamiento trombolítico
Sangramiento interno activo.
Resucitación cardiopulmonar prolongada en los 7 días previos, excepto cuando solo se realice desfibrilación eléctrica.
Retinopatía diabética hemorrágica (grado III).
Neoplasia intracraneal conocida o trauma de cráneo menor de 2 semanas.
Cirugía mayor reciente (menos de 10 días).
Sospecha de disección aórtica.
Politraumatismo grave reciente.
Cirugía intracraneal, espinal y oftálmica en los dos meses precedentes.
Retinopatía hipertensiva hemorrágica (grado III), o hemorragia retineana de otras causas.
Hipertensión arterial severa (presión arterial sistólica mayor de 200mm Hg y/o diastólica mayor de 120mm Hg) que no desciende después del tratamiento con reposo, alivio del dolor o sedación.
Embarazo y puerperio de menos de 10 días.
Punción arterial o venosa profunda o biopsia en sitios no comprensibles en los últimos 7 días.
Historia de accidente cerebrovascular hemorrágico.
Presencia de alguna neoplasia o enfermedad sistémica con riesgo de sangramiento.
Presencia de sepsis severa o sospecha de endocarditis infecciosa.
Sospecha de pericarditis aguda.
Antecedentes de reacción alérgica al agente trombolítico.
Metodología para la administración del tratamiento trombolítico.
Fármaco utilizado: Estreptoquinasa Recombinante Cubana.
Dosis 1 500 000 uds.
Tiempo de administración: 30-60 minutos.
Vía de administración: EV.
Reacciones adversas por el fibrinolítico24: hipotensión, dolor lumbar, vómitos, rasch, fiebre, sangramientos, temblor ,escalofríos, etc.
Criterios de inclusión y exclusión para la administración de la terapia con GIK:
Criterios de inclusión
Clínica sugestiva de IMA.
Menos de 12 de horas de evolución.
Cambios electrocardiográficos sugestivos de IMA, incluyendo BRIHH agudo.
Criterios de exclusión
Diabetes Tipo I.
Hiperkaliemia (K mayor de 5 meq/L con o sin cambios en el ECG).
Embarazo.
Trastornos renales severos.ĀĀĀ
Protocolo para la administración de la terapia con GIK.
500 ml dextrosa 30%
30 uds de insulina simple.
40 meq de K.
Dosis: 1.5ml / Kg/ hora durante 24 horas.
La infusión de GIK debe ser administrada con bomba de infusión utilizando una vena periférica.
Antes de iniciar la infusión de GIK se debe obtener muestras de sangre para dosificar K y glucosa.
Se debe comenzar la infusión de GIK antes de obtener los resultados de laboratorio, asumiendo que el paciente no tiene hiperglucemia ni hiperkaliemia.
Después de comenzada la infusión de GIK la estrategia de reperfusión debe iniciarse inmediatamente. De no ser posible esto, la infusión de GIK se puede administrar al terminar la trombolisis.
Se tomarán nuevas muestras de glucosa y K a las 6 y 12 horas de la toma de muestra inicial.
Todas las muestras de sangre se deben tomar en el brazo opuesto a la infusión de GIK.
El ECG debe realizarse antes y a los 90 minutos de iniciada la reperfusión.
Debe monitorearse cuidadosamente el balance hídrico durante las primeras 24 horas con GIK, así como la diuresis.
Se puede utilizar insulina adicional en caso de hiperglucemia importante.
Se administrará además a todos los pacientes:
Atenolol o Propanolol por vía oral desde el ingreso hasta el egreso y luego ambulatoriamente en el seguimiento a menos que aparezcan reacciones adversas o contraindicaciones:
a. Atenolol 50 – 100 mg dia
b. Propanolol 60 – 120 mg dia
2. Aspirina por vía oral desde ingreso hasta el egreso, ambulatoriamente en el seguimiento a menos que aparezcan reacciones adversas: 250 mg al día.
ĀReacciones adversas por
Severas (producen un estado de colapso cardiovascular, con manifestaciones de hipoperfusión periférica importante, e incluye el shock anafiláctico como su máxima expresión)
ĀLigeras (se evidencian solo por irritación local o generalizada de piel y mucosa)
Criterios de inclusión y exclusión para la administración de la terapia con Mg. 21ˉ23,25ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ Ā
Los pacientes que fueron sometidos a tratamiento con infusión de sulfato de Mg,Ā cumplirán el siguiente criterio de inclusión: todo paciente con criterio de IMA excluido de tratamiento trombolítico con Estreptoquinasa Recombinante cubana.
Además se consideran los criterios de exclusión en el estudio:
Pacientes con shock.
Hipotensión severa persistente.
Bloqueo auriculoventricular completo, sin marcapasos.
Modo de administración.
Se administró tan pronto fue posible por vía endovenosa sulfato de Mg 2 gr. en 5 min. Se continuó inmediatamente con una infusión de Mg de 16 gr. en 900 ml de dextrosa al 5% en 24 horas.
Efectos secundarios o reacciones adversas. 22,23
Las dosis terapéuticas pueden producir enrojecimiento, sudoresis y sensación de calor. Ocasionalmente ocurren náuseas, vértigos y debilidad general. Las concentraciones elevadas pueden ocasionar hipotensión e insuficiencia respiratoria grave que se trata conĀ respiración artificial, administración intravenosa de 1g de Gluconato de calcio o Cloruro de calcio en 3 min. seguido de infusión de 15 mg/kg en 24 horas.
Contraindicaciones.
- Cardiopatías avanzadas.
Presentación.
Sulfato de Mg 10% ámpulas de 10 ml, 1 gr de Sulfato de Mg, 4-6 mmol.
Sulfato de Mg 20% ámpulas de 10 ml, 2 gr de Sulfato de Mg, 8-12 mmol.
Sulfato de Mg 30% ámpulas de 10 ml, 3 gr de Sulfato de Mg, 16-18 mmol.
Se administrará además a los pacientes:
Atenolol o Propanolol por la vía oral desde el ingreso, hasta el egreso y luego ambulatoriamente en el seguimiento a menos que aparezcan reacciones adversas o contraindicaciones.
Atenolol 50 – 100 mg al día.
PropanololĀ 60 – 120 mg al día.
Aspirina por la vía oral desde el ingreso hasta el egreso y luego ambulatoriamente en el seguimiento a menos que aparezcan reacciones adversas: 250 mg al día.
Se le realizó necropsia a todos los fallecidos para el 100%.
La información fue procesada manualmente el programa de SPSS para Windows y se presentó en tablas y gráficos estadísticos.
Para el análisis se utilizaron técnicas de distribución de frecuencia, porcentajes, diferencias absolutas y relativas y pruebas estadísticas de asociación y significación.
Se considera estadísticamente significativa:
- Probabilidades asociadas (p ≤ 0,05).
- Diferencias muy significativas (p ≤ 0,01).
- Diferencias altamente significativas (p ≤ 0,001).
Consideraciones éticas en relación con la investigación:
1-Se le explicó a los pacientes en que consiste el tratamiento, así como sus posibles complicaciones y la importancia de este para su evolución, obteniendo en todos los casos su consentimiento informado de forma verbal.
2-Cuando no fue posible la cooperación de los pacientes, se obtuvo el consentimiento informado de los familiares más cercanos, también de forma verbal, y previa una explicación detallada sobre el proceder.
3-Se creó un comité formado por especialistas en cardiología y medicina intensiva de
ĀĀ -Velar por la correcta marcha de la investigación, observando que se cumpla la metodología establecida en el diseño inicial, orientando de ser necesarios, cambios en la metodología o su interrupción si se observaran reacciones o efectos adversos indeseables.
Análisis y Discusión de los Resultados:
Ā TABLA 1: EDAD Y SEXO.
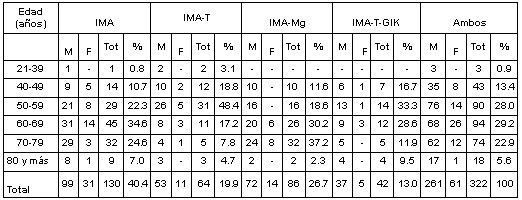
FUENTE: ENCUESTA.ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ TOTALES:
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀMasc vs fem en cada tipo de IMA y el total: Z = 20,2Ā p = 1
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ IMA vs. C/U de los demás: Z = 3,7Ā p<0,0001. femen. entre tipos IMA P>0,05ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ 50-79: dif. signific vs las demás, excepto entre ellas.Ā
En el período estudiado, desde el 1ro de Diciembre de 1988 hasta el 31 de Diciembre del 2005 fueron ingresados en
Pacientes con IMA tratados con Betabloqueadores y Aspirina (todos ingresados desde 1988 hasta el 1ro de Octubre de 1993): 130 enfermos para un 40.4% del total.
Pacientes con IMA tratados con Trombolisis, Betabloqueadores y Aspirina desde 1993 hasta el 2003: 64 infartados para un 19,9%.
Pacientes con IMA sin criterios de Trombolisis, tratados con Sulfato de Mg, Betabloqueadores y Aspirina desde 1993 hasta el 2003: 86Ā enfermos que representaron el 26,7 %.
Pacientes con IMA tratados con Trombolisis, Solución GIK, betabloqueadores y Aspirina desde 1ro de Junio de 1998 hasta el 31 deĀ DiciembreĀ delĀ 2003:Ā 42Ā infartados para un 13,0 %.
Existe un predominio significativo del sexo masculino con 261 pacientes, sobre el femenino con 61 infartados con una relación entre ambos sexos deĀ 4,3/1.
En las edadesĀ entreĀ 50-79 años, se localizaron el mayor de infartos con diferencias significativas con respecto a los demás grupos deĀ edades, excepto entre ellas (50 –59, 60 – 69 y 70-79 años).
El hallazgo del predominio del sexo masculino es aceptado en forma general en la literatura médica 15-27 y es considerado en ocasiones un factor de riesgo coronario. Hasta la edad de 55 años, el corazón sufre manifestaciones clínicas de isquemiaĀ miocárdica con una frecuencia de 4-6 vecesĀ mayor que la mujer.
EstaĀ diferenciaĀ tiende a desaparecer a partir de los 60 años y se plantea que depende de factores hormonales.
En el IPRAPNE 33Ā predominaron losĀ grupos de 50-59 y 60-69 años sumando un 47 %, coincidiendo con nosotros.
En nuestra serie la mayor cantidad de pacientes afectados se encuentra entre 60-69 años con 94Ā enfermosĀ (29,2Ā %),Ā leĀ sigueĀ enĀ formaĀ decreciente el de 50-59 (28,0 %),Ā 70-79 (22,9 %), 40-49 (13,4 %), 80 y más (5,6 %),Ā por último los de menos de 40 años con 3 infartados para el 0,9 %.
En todos los grupos es mayor la frecuencia de hombres que de mujeres.
La incidencia de IMA, en edades por debajo de los 50 años, se ha observado relativamente baja en varios estudios2-4, 7,8,13-16,29-33 en comparación con las edades más avanzadas de la vida siendo necesarioĀ destacar la frecuencia de IMA siete veces superior en este último grupo de pacientes.
La terapéutica fibrinolíticaĀ fue aplicada en nuestra serie, a un número no despreciable de infartos mayores de 60 años.
Los pacientes ancianos han sido privados de los beneficios delĀ tratamiento fibrinolítico durante muchos años y por muy diversas causas, fundamentalmente por temor a las complicaciones que se puedan presentar, incluyendo las hemorrágicas. La mayoría de los estudios iniciales que se realizaron para validar el tratamiento trombolítico en el IMA,Ā excluyeron a los enfermos de edad avanzada y otros hicieron una rigurosa evaluación de su inclusión, sin embargo se ha demostrado en otros trabajos que el beneficio del tratamientoĀ fibrinolítico aumenta con la edad. 5, 38,39ĀĀĀĀ
Los criterios para incluir a los ancianos en la terapia trombolítica en el IMA ha ido cambiando con el transcurso de los años y los nuevos conocimientos adquiridos a partir de los resultados de los grandes estudiosĀ realizados, los cuales han demostrado los beneficios que puede reportar a este grupo de pacientes con mayor incidenciaĀ deĀ IMA.
ĀĀ TABLA 2: TIEMPO ENTRE EL COMIENZO DE LOS SÍNTOMAS, EL INICIO DEL TRATAMIENTO Y
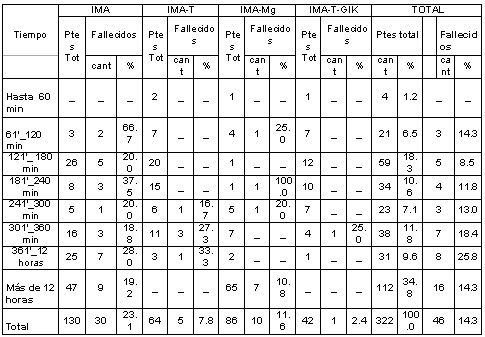
FUENTE: ENCUESTAĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀP> 0,05ĀĀ
El tiempo entre el comienzo de los síntomas, el inicio del tratamiento y la letalidadĀ en la fase aguda se estudian en la tabla 2.
De los 322 infartos tratados fallecieron 46(14,3 %), no hay una relación definida entre el tiempo transcurrido y letalidad. Debe obedecer a las pequeñas cantidades de pacientes en cada caso.
De los 46 fallecidos, 31 ocurrieron cuando la terapéutica fue aplicada a partir de las 6 horas del comienzo de los síntomas.
No seĀ reportaron fallecidos en losĀ IMA-T e IMA-T-GIK por debajo de 240 minutos y 300 minutos respectivamente, ocurriendo el mayor número de fallecidos entre 301-360 minutos para ambos grupos.
El mayor número de fallecidos de la serie se localizaron en los tiempos de más de 12 horas con 16 (14,3 % ) correspondiendo 9 al grupo IMA y 7 al grupo IMA-Mg.
La menor letalidadĀ en la fase aguda ocurrió en el grupo IMA-T-GIK (2,4 %) siguiéndole un orden creciente el IMA-T (7,8 %), IMA-Mg (11,6 %) y por último el IMA (23,1 %) coincidiendo por otrosĀ autores.21, 22,26-34,39 ĀĀ
HaĀ sido descrito en varios ensayos clínicos 9,10,18-20,25,42 que una vezĀ que sea ocluida una arteria coronaria importante, se extiende la necrosis de endocardio a epicardio, la que se completa en un intervaloĀ de tiempo que resulta variado, oscilando entre las 4 y 12 horas lo cual representa diferente grado de variación interindividual dependiendo de circunstancias como: El estado previo del músculo cardiaco, la presencia o no de miocardio precondicionado, la cuantía del consumo de oxígeno, la presencia y funcionamiento efectivo deĀ la red circulatoria colateral, el grado de reserva coronaria; así como la activación del sistema fibrinolítico endógeno capaz de producir episodios de desoclución intermitentes de la arteria relacionada con el infarto, o incluso lograr la total reapertura de la misma.
En la mayoría de los trabajos que se han revisado 5,15-20,23,25 sobre el tratamiento fibrinolítico en el IMA, se ha hecho referencia al beneficio que reporta su aplicación lo más precoz posible al comienzo clínico de los síntomas de oclusión de la arteria responsable del infarto (ARI) sobre todo en las primeras 4 horas (quedando evidenciado en nuestro trabajo) y muy especialmente en las primeras 2 horas, lo cual se hace evidente sobre la recanalización de dicho vaso y la reperfusión del territorio vascular previamente comprometido.
LasĀ medidas prehospitalarias aplicadas a los pacientes con sospecha de infarto agudo del miocardio son la piedra angular en su supervivencia. En Ciudad de
El estudio GISSI45 realizado en 1995, sobre la epidemiología de los retrasos evitables, evidenció que el tiempo paciente es el responsable de la mayor demora.
En el estudio GUSTO46 se aprecia como la trombolisisĀ precoz puede repermeabilizarĀ
Otras de las circunstancias que condicionan la no administración en tiempo delĀĀ trombolítico son los retrasos intrahospitalarios donde se destacan la presión asistencial en los servicios de urgencias, la necesidad de interconsulta con el intensivista, el traslado intrahospitalario hasta una unidad de vigilancia intensiva, la falta de camas libres en estas unidades y la suma de todas ellas implican un retraso para iniciar el tratamiento a veces inaceptable; es por ello que es necesario la trombolisis prehospitalaria. 47
Por último, los ensayos clínicos de agentes trombolíticos han demostrado la importante relación que existe entre el tiempo hasta el comienzo del tratamiento y la supervivencia en pacientes con IMA. En el trabajo publicado por el Grupo deĀ Ensayistas de Terapia Fibrinolítica (casi 69 000 pacientes) hubo una mortalidad del 1% más por hora de retraso hasta el momento del tratamiento.23, 25, 48,49
En los pacientes no trombolizados (IMA e IMA-Mg) hubo una disminución significativa de la letalidad en los tratados con infusión de Mg 11.6% contra 23,1%.
El beneficio de la aplicación endovenosa temprana de sales de Mg en caso de IMA, con disminución significativa de la mortalidad temprana y el número de arritmias severas con respecto al grupo que no utilizó Mg esĀ reportado por varios autores 32-34, coincidiendo con nuestros resultados.
TABLA 3.- FACTORES DE RIESGO CORONARIO Y ANTECEDENTES DE CARDIOPATIA ISQUEMICA DEL TOTAL DE INFARTADOS Y LOS FALLECIDOS EN
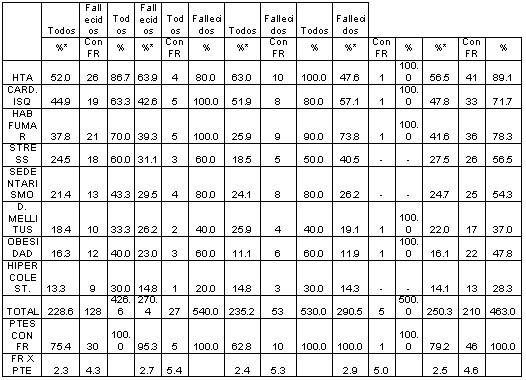
FUENTE: ENCUESTA
DelĀ total de pacientes con factores de riesgo coronario y antecedentes de cardiopatía isquémica previa, los fallecidos presentaron muchos más FRCA (4.6) que los del total de infartadosĀ (2.5); con igual comportamiento para cada grupo (tabla 7). El grupo IMA-T con 5.4 FRCA por paciente fallecido prevaleció en la serieĀ siguiéndoles: IMA-MgĀ con 5.3, IMA-T-GIK 5.0Ā yĀ porĀ último el IMA con 4.3.
Fallecieron 41 infartados conĀ HTAĀ (89.1%),Ā 36 con hábito de fumarĀ (78.3%), 33 con antecedentesĀ previo de cardiopatía isquémicaĀ (71.7 %),Ā 26 con stress (56.5%,),Ā 25 con sedentarismoĀ (54.3%),Ā 22 con obesidadĀ (47.8%), 17 con diabetesĀ mellitus (37.0%)Ā yĀ 13Ā conĀ hipercolesterolemiaĀ (28.3%).Ā
En diferentes estudios revisados 6,18-22,26-34,38-41,44-46,51 el número de factores de riesgoĀ coronario fue mayor en el grupo de los fallecidos.
TABLA 4 . COMPLICACIONES RELACIONADAS CON EL USO DE TROMBOLÍTICOS, TROMBOLÍTICOS – GIK Y LETALIDAD EN
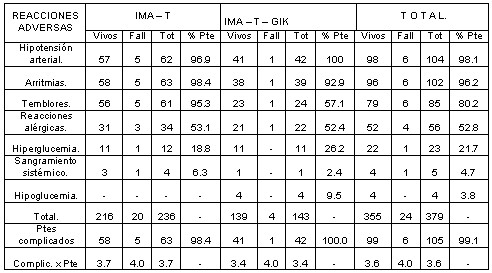
FUENTE: ENCUESTA.ĀĀĀĀĀĀĀĀĀĀĀĀĀHipotens. y Arritmias dif. signif p <0.05 vs. C/UĀ de las demásĀ en el total e IMA -ĀĀĀ T-GIK.
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀEnĀ IMA -T no dif. con temblores.
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀComplicaciones vivos vs fallecidos p > 0.05 entre IMA -T;Ā IMA -T -GIK y el total.
Las complicaciones relacionadas con el uso del trombolíticos,Ā soluciónĀ Glucosa-Insulina-Potasio y letalidad en la fase aguda se reflejan en la tabla 4.
El número de complicaciones en pacientes vivos y fallecidos no presentaron diferencias significativas. Se complicaron 105 infartados que representó un 99.1% del total. Los vivosĀ tuvieron 3.6 complicaciones por paciente y los fallecidos 4.0. En los IMA-T se complicaron el 98.4% de los enfermos, con 3.7 complicaciones en los vivos y 4.0 en los fallecidos, mientrasĀ que en el grupo IMA-T-GIK se complicaron el 100 % de los infartados con 3.4 complicaciones por enfermos vivos y 4.0 en los fallecidos.
Las complicaciones presentadas en orden de frecuencia fueron: la hipotensión arterial 98.1%, arritmias 96.2%, temblores 80.2 %, reaccionesĀ alérgicas 52.8 %, hiperglucemiaĀ 21.7 %, sangramientoĀ sistémicoĀ 4.7% eĀ hipoglucemiaĀ 3.8%.
La hipotensión arterial y las arritmiasĀ ofrecen diferencias significativas ( P< 0.05) con respecto a las demás complicaciones.
Salvo la hipoglucemiaĀ que se presentó en el grupo IMA-T-GIK en 4 infartos vivos, el resto de las complicacionesĀ presentaron para ambos grupos ( IMA-T e IMA-T-GIK)Ā distribuciones no significativas.
La hipotensión arterial ( HA) fue laĀ reacción adversa más frecuente en la serie coincidiendo con las mayorías de los reportes 5,22,23,25,27,33,43,47 que la sitúan en un rango que oscila entre el 50-80%.
La aparición de hipotensión arterial es de frecuenteĀĀ observación durante el tratamiento fibrinolítico, sobre todo cuando se emplea estreptoquinasa, ya sea en su forma natural o recombinante y el complejo Activador-Plaminógeno-Estreptoquinasa-Anisoilado (APSAC) lo cualĀ se encuentra en estrecha asociación con una activaciónĀ efectiva del sistema de la bradiquininaĀ tisular y plasmática, con reducción de la actividad del sistema del tromboxano A2 Āy de las prostaglandinas, produciendo diversos grados de vasodilatación a nivel de los vasos arteriales de mediano y pequeño calibre incluyendo las arteriolas 53.
Al comienzo de la era trombolítica y aún en la actualidad se teme a la aparición de HA severa, sobre todo aquellas que produce trastornos hemodinámicos, ya que puede comprometer la perfusión coronaria (por una reducción significativaĀ de la presión de perfusión y disminución de la resistenciaĀ de los vasos coronarios), ya queĀ se encuentra comprometida por el evento isquémico agudo. Esto puede tener como consecuencias negativas la extensión del área infartada si se empeora el flujo sanguíneo al territorio previamente comprometido, pero además puede producir isquemia a distancia en los territorios que presenten vasos con distintos grados de obstrucción (territorios en riesgo) llegando incluso a producir un sufrimiento sub-endocárdicoĀ de esas regiones, que en ocasionesĀ llevan a un IMA no transmural. Todo esto puede repercutirĀ en elĀ gastoĀ ventricular izquierdo (VI),Ā produciendo distintos grados de fallo VI. 5, 44,53
A pesar de la presente aparición de HA en el curso del tratamiento trombolítico en el IMA, esta se presenta en la mayoría de las ocasiones de forma benigna, casi nunca con severas manifestaciones, que pueden llevar a un estado de shock cardiocircultorio, lo cual se presenta casi exclusivamente cuando se asocia a estados de hipovolemia absoluta (pérdidas efectivas de volemia intravascular) o relativa como es el caso del IMAĀ de ventrículo derecho. 43-46
Otras de las manifestaciones adversas al tratamiento trombolítico, son las “reacciones alérgicas”, las cuales se pueden manifestar ya desde el inicio del tratamiento con una incidencia que oscila entre un 3-15 %, pero generalmente se descubren en las primeras 4 horas de iniciada la infusión; y que pueden ir desde reacciones ligeras por su comportamiento hasta severas, pudiendo llegar hasta el ominoso estado de shock anafiláctico. 53
Como proteína de origen bacteriano, la estreptoquinasa es antigénica y se han descrito comúnmente reacciones alérgicas relacionadas con su administración, por lo general limitadas a fiebre y urticaria, pues la anafilaxia es rara. También se pueden encontrar elevados niveles de anticuerpos antiestreptoquinasa, luego de la administración de este agente con fines terapéuticos, o post-infección estreptocócica, lo cual puede ser causa de inactivación y fracaso terapéutico, teniendo esto lugar en los pacientes donde se hace necesario repetir el tratamiento antes del año.
En nuestra serie se observaron reacciones alérgicas en más del 50 % de los casos tratados, fundamentalmente como episodios de urticaria, que se resolvieron con la administración de antihistamínicos por vía parenteral. No se presentaron reacciones alérgicas severas ni estados graves de shock anafiláctico.
Una de las reacciones más peligrosas, temidas y que en muchas ocasiones disuade la administración de la terapia trombolítica son los fenómenos hemorrágicos, los cuales ocurren a cualquier nivel de la economía y con distintos grados de severidad, que incluso puede llevar a la muerte de los pacientes. No se ha demostrado que exista una diferencia significativa entre los distintos fármacos trombolíticos en lo referente a la capacidad de producir sangrado sistémico. 53
En nuestro estudio la incidencia de sangrado sistémico fue escasa, haciéndose objetivo solo en 5 pacientes trombolizados, evidenciándose en el 100 % de los casos en las primeras 12 horas de administrado el tratamiento y el sitio de sangrado fue la vía urogenital, presentándose hematuria en todos los enfermos. Estos sangramientos se consideraron de ligera cuantía, al no afectar la cuantificación total de la hemoglobina, no comprometer la hemodinámica de los pacientes, ni necesitar la reposición de sangre o hemoderivados.
Los fenómenos hemorrágicos, a pesar de su pobre incidencia, constituyen la complicación más peligrosa asociada al tratamiento trombolítico en el IMA, sobre todo cuando el agente utilizado posee actividad sistémica y tiene la capacidad de inducir un estado lítico generalizado al activar no selectivamente al plasminógeno circulante, como es el caso de la estreptoquinasa recombinante cubana. 53
Diferentes estudios realizados han demostrado que gran parte de los pacientes con IMA presentan alteraciones del ritmo cardiaco durante la fase aguda del evento coronario. Se dice que la oclusión coronaria produce una serie de anomalías iónicas, metabólicas y neurohormonales, las cuales son en conjunto las responsables de estos trastornos. La reducción del flujo sanguíneo efectivo a los territorios cardiacos afectados conduce a un metabolismo predominantemente anaerobio con acumulación de los metabolitos tóxicos en el miocardio isquémico por ausencia de lavado venoso vascular. Esto produce un incremento del potasio y el calcio intracelular, depleción de fosfato de alta energía y aumento de las catecolaminas en el área isquémica y en la circulación general.
A punto de partida de estos fenómenos tienen lugar alteraciones de las propiedades electrofisiológicas y bioquímicas de tejido isquémico con la consiguiente aparición de arritmias ya sea por mecanismos de reentrada, actividad disparada, aumento del automatismo o por la aparición de pospotenciales precoces o tardíos. 43-47
El potasio activa la excitabilidad y la contractilidad del músculo cardiaco, variando el estado de polarización. En la zona central de un infarto la anoxia es grave y las células mueren. En la periferia del infarto, sin embargo, existen células que están anóxicas pero vivas. En estas, el gradiente iónico de potasio a través de la membrana está alterado y el potasio sale de la célula. 37 Esta pérdida contribuye a la reducción del potencial de membrana, generando así un foco eléctricamente inestable, capaz de producir arritmia. La GIK restaura las concentraciones de potasio extracelular y probablemente intracelular. También tiene capacidad de aumentar la recaptación de potasio por la célula, al estimular la bomba NA / K-ATP asa 53.
En este sentido se demostró la presencia de arritmias en 102 enfermos infartados (63 IMA-T, 39 IMA-T-GIK).
Las complicaciones inherentes al uso de GIK son poco frecuentes y en general de mínima gravedad; en nuestro estudio encontramos hiperglucemia en 11 enfermos e hipoglucemia en 4; no hubo fallecidos con estas complicaciones.
Lazar HL 38 encontró más frecuente la flebitis en la zona de punción venosa con un 15 %, seguido de la hiperglucemia, hipoglucemia y la hiperpotasemia, que no aparece si la función renal es normal. Marano 48 encontró en su estudio, como efecto adverso más frecuente la flebitis, seguida del malestar digestivo (en su estudio se administraba el potasio por vía oral) y la hipoglucemia (la glucosa también se administraba por vía oral)
TABLA 5. REACCIONES ADVERSAS AL MAGNESIO Y LETALIDAD EN LA FASE AGUDA.
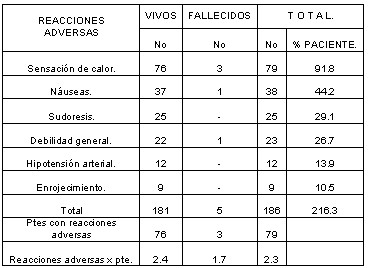
FUENTE: ENCUESTA.
Las reacciones adversas al Mg y letalidad en la fase aguda (Tabla 5) fueron: sensación de calor en 79 infartados (91.8 %), náuseas 44.2%, sudoresis 29.1%, debilidad general 26.7 %, hipotensión arterial 13.9 % y enrojecimiento 10.5 %.
Hubo 2.4 reacciones adversas por paciente en los egresados vivos y 1.7 en los fallecidos por lo que consideramos que las mismas no fueron protagonistas en las causas de muerte. Otros autores reportaron similares resultados. 30, 32,34
CONCLUSIONES
1-. En el grupo de pacientes estudiados predominó el sexo masculino, las edades de 60 a 69 años. La letalidad aumentó en correlación directa con la edad, no existiendo diferencias significativas entre ambos sexos. Los factores de riesgo coronario y antecedentes de interés con más frecuencia encontrados fueron: la Hipertensión Arterial, Cardiopatía Isquémica previa y hábito de fumar. Los fallecidos presentaron significativamente mayor número de factores de riesgos que los egresados vivos.
2-. La hipotensión arterial, las arritmias, los temblores y las reacciones alérgicas fueron las principales reacciones adversas que presentaron los pacientes tratados con fibrinolíticos con o sin Solución de Glucosa-Insulina-Potasio, encontrándose la hipoglucemia solo en el grupo IMA-T-GIK. Mientras que la sensación de calor, náuseas, sudoresis y debilidad general fueron mayoritarios en los enfermos tratados con Sulfato de Magnesio, no demostrándose relación causal con la letalidad.
3-. Hay un predominio de la letalidad y otras complicaciones cardiovasculares durante la fase aguda del infarto; en este sentido la terapia con Heberquinasa-GIK redujo la letalidad de la serie, siendo menor cuando fue administrada precozmente.
4-. En los pacientes tratados con magnesio fueron menos las complicaciones y la letalidad que el grupo de infartados sin tratamiento trombolítico
Recomendaciones
1-. Se recomienda el uso de Solución Glucosa-Insulina-Potasio asociado al tratamiento con Heberquinasa Recombinante Cubana en los pacientes con Infarto Agudo del Miocardio.
2-. En los pacientes con IMA sin criterio de trombolisis recomendamos el uso de Infusión de Sulfato de Magnesio.
BIBLIOGRAFIA
Arlatti S. Myocardial necrosis in ICV patients with acute non-cardiac disease: A prospective study. Intensive Care Med 2000 jan, 16(1): 31-7.
Cox JL, Melady MF, Chen E, Naylor CD. Lower improve coding of acute myocardial infarction in hospital discharge abstract: a pilot project. Can J Cardiol 1999 apr; 13: 351-8.
Reeder GS, Gersh BJ. Modern management of acute myocardial infarction. Curr Probl Cardiol 2000 sep; 21: 565-7.
Gilber WB, Kereiakes DJ, Dean En, Martín L., Anderson L. Prehospital diagnosis and treatment of acute myocardial infarction: A north-south perspective. The Cincinnati heart project and the Nashville prehospital TPA trial. Am Heart J 1999, 121: 1-110.
Keeley EC, Hillis D. Primary PCI for Myocardial Infarction with ST- Segment Elevation. N Engl J Med 2007; 356: 47-52.
De Winter RJ, Windhausen F, Cornel JH, et al . Early Invasive versus Selectively Invasive Management for Acute Coronary Síndromes . N Engl J Med 2005; 353: 1095-103.
Cuba. Ministerio de Salud Publica. Informe Estadístico año 2003 Ciudad de La Habana, 15 de Enero, 2004.
Liebson PR, Klein LW. The Non Q-wave myocardial infarction revisited: 10 years later. Prog Cardiovasc Dis 2000 mar-apr; 39: 399-444.
Camici PG, Crea F . Coronary Microvascular Dysfunction . N Engl J Med 2007; 356:830-8
Hansson GK. Inflammation , Atheroesclerosis, and Coronary Artery Disease. N Engl J Med 2005; 352: 1685-93.
Heistad DD. Unstable Coronary – Artery Plaques . N Engl J Med 2003; 349: 2285-7
Kolodgie FD, Gold HH. Burke AP, et al . Intraplaque Hemorrhage and Progression of Coronary Atheroma . N Engl J Med 2003; 349: 2316-24.
Ding W. Relationship between the site of coronary artery occlusion and degree of hemodynamic abnormality of right ventricular myocardial infarction. Chan Hua Neiko Tsachil 2001; 36(10): 676-9.
Lee KL; Woodlief JH, Topol EJ. Predictors of 30-day mortality in the era of reperfusion for acute myocardial infarction. Results from an international trial of 41 021 patients. Circulation 2000; 91: 1659-68.
Gosage JR. Acute myocardial infarction: Reperfusion strategies. Chest 1999; 106: 1851- 66.
Lee TH. Effective reperfusion for acute myocardial infarction begins with effective health policy. Ann Intern Med 2000 Apr 15; 126(8): 652-3.
Ohata H, Lemasler JJ, Trollerger D. Charges in shale and viability of culture adult rabbit cardiac myocites during ischaemia reperfusion injure. Res Mul Cummon Olpharmacol 2001; 86(3): 259-71.
White HD, Cross DB, Norris RM. Safety and efficacy of report a trombolitic treatment after acute myocardial infarction. Br Heart J 2000; 64: 174-81.
Barbach GI. A repeat infusion of recombinant tissue type plasminogen activators in patient with acute myocardial infarction and early recurrent in myocardial ischaemia. J Am Coll Cardiol 2000; 71: 524-8.
Simmons ML, Amount J, Vandre Braund. Reatreatment with altiplase of early signe of reoclusion after trombolisis. Am J Cardiol 2000; 16: 779-83.
Gaor; to perform safely percutaneous transluminal coronary angioplasty in acute myocardial infarction. Chung Hua Nei Ko Tsa Chich 2001; 36(9): 581-3.
Gosh BJ, Anderson JL. Trombolysis and myocardial salvage: Results of clinical trials and the animal paradigm- paradonic or predictable? Circulation 2000; 88: 296-306.
Hochman JS, Lamas GA, Buller CE , et al. Coronary Intervention for Persistent Occlusion after Myocardial Infarction . N Engl J Med 2006 ; 355: 2395-406.
Bradley EH, Herrin J, Wang Y, et al . Strategies for Reducing the Door-to Balloon Time in Acute Myocardial Infarction . N Engl J Med 2006; 355: 2308-19.
Hillis LD , Lange RA . Myocardial Infarction and the open- Artery Hypothesis . N Engl J Med 2005; 353: 1124-33.
Opie LH. Proof glucose-insulin-potassium provides metabolic protection of ischaemic myocardium? Lancet 1999; 353: 768-9.
Stanley AWH, Prather JW. Glucose-insulin-potassium, patient mortality and the acute myocardial infarction: results from a prospective randomized study [abstr]. Circulation 1999; 57 (Supl 2): 62.
Gradinac S, Coleman GM, Taegtmeyer H, Sweeney MS, Frazier OH. Improved cardiac function with glucose-insulin-potassium after aortocoronary bypass grafting. Ann thorac Surg 1999; 48: 484-9.
Marwick TH, Woodhouse SP. Severe hypophosphataemia induced by glucose-insulin-potassium therapy. A case report and pro-posa for altered protocol. Int J Cardiol 1999; 18: 327-30.
Raghu C. Peddeswara Rac D. Protective effect of intravenous magnesium in acute myocardial infarction following thrombolytic therapy. Int J Cardiol 1999 dec 1; 71(3): 209-15.
Shibata M. Ueshima K. Harada M. Nakamura M. Hiramari K. Effect of magnesium sulfate pretreatment and significance of matermetalloproteinesse-1 and interleukin-6 levels in coronary reperfusion therapy for patients with acute myocardial infarction. Angiology 1999 jul; 50(7):573-82.
32. Sánchez GC, Argüelles MT, Vázquez VL, Rosadón CY, Importancia del Tratamiento en Sulfato de Magnesio en pacientes con infarto agudo del miocardio. Estudio preliminar. Rev. Cubana Med 2003; 42(3).
33. Cuba. Ministerio de Salud Pública. Aplicación de la Estreptoquinasa Recombinante en el infarto Miocárdico Agudo. Extensión nacional. Informe final de ensayo clínico, Ciudad de la Habana, 29 de nov, 1995.
34. Woods KL. Fletcher S. Rffe C. Haider Y. Intravenous Magnesium Sulfate in suspected acute myocardial infarction: resulte of the Second Leicester Intravenous Magnesium Intervention Trial (LIMIT-2). Lancet. 1992; 339: 1553-8.
35. Wang K, Asinger RW, Marriot HJL . ST-Segment Elevation in Conditions Other than Acute Myocardial Infarction. N Engl J Med 2003; 349: 2128-34.
36. Zimetbaun PJ, Josephson ME . Use of the Electrocardiogram in Acute Myocardial Infarction . N Engl J Med 2003;348:933-40.
37. Wallach J. Interpretación Clinica de las pruebas de laboratorio. T1 . 4ta ed. Editorial Ciencias Médicas ; 2006.
38. Lazar HL Enhanced preservation of acutely ischemic myocardium and improved clinical outcomes using glucose-insulin-potassium (GIK) solutions. Am J Cardiol 1997; 80:90A-93A.
39. Lopaschuk GD. Fatty acid and glucose metabolism: a target for intervention In: Hearse DJ, ed Metabolic approaches to ischaemic heart disease and its management. London: Sience Press, 1998: 44-57.
40. Pfeffer MA, Mc Murray JJV, Velázquez EJ, et al .Valsartan, Captopril, or Both in Myocardial Infarction Complicated by Heart Failure, Left Ventricular Dysfunction, or Both N Engl J Med 2003; 349: 1893-903.
41.- Ioannidis JP, Salme D, Chew PW, Lam J. Accuracy and Clinical Effect of Out-04-Hospital Electrocardiography in the Diagnosis of Acute Cardiac Ischaemia: A Meta-Analysis. Ann Emerg Med 2001; 37: 461-70.
42. - Libby P, Theroux P .Pathophysiology af coronary artery disease circulation 2005; III: 3481-8.
43. Gómez PMV, Toledo Queseda A, Castellanos Dumois A, Herrera ML. Trombolisis en el infarto agudo del miocardio. Análisis de los Tiempos de demora. Rev Cubana Med. 2001; 40(2): 91-5.
44. Triolet Gálvez I A, Sánchez MJM Rabell PO, Pino Alvarez AA. Trombolisis en pacientes con Infarto Miocárdico Agudo ingresados en una Unidad de Cuidados Intensivos. Rev cubana Med Intens y Emerg. 2001;1(10): 172-203.
45. GISSI.Avoidable Delay Study Group: Epidemiology of avoidable delay in the care of patients whit acute myocardial infarction in Italy. Arch Intern Med. 1995; 155:1481.;
46 The GUSTO Argiographic Investigators: the effects of tissue plasminogen activator, Streptokinase or both on coronary-artery potency ventricular function, and survival after acute myocardial infarction. N Engl J Med 1993; 339:1650-2.
47. Valladares Carvajal FJ, Iraola Ferrer MD, Aicto Prendes Pr. Trombólisis Tardía. Rev Cubana Cardiol Cir Cardiovasc 2000; 14(2): 99-106.
48. Marano L, Bestetti A, Louinscio A, Tagliabue L , Castini D, Dario P. Effects of infusion of glucose-insulin-potasium on myocardial function after a recent myocardial infarction. Acta Cardiol 2000; 55(1): 9-14.
49. Conti R. Ischemic Heart disease. JACC 2000; 35 (5): 2-3.
50.- American Heart Association Cardiovascular disiase statisties , 2006. ( AC Cessed December 7, 2006, at http: // w w w . american heart org.)
51.- HeJ, GuD, WuX, et al. Major Causes of Death Among Men and Women in China. N Engl J Med .2005 ;353 ;1124-33.
52.- DzariK V, Barton JR, Kee C ,Teo KK, Ignaszewski A. Changing practice in the management of acute myocardial infarction complicated by cardiogenic Shock: elderly compared with Younger patients. Can J Cardiol. 1998 Jul; 14 (7 ): 923-30.
53 . Cué Brugneran M. Agentes Trombolíticos en el infarto agudo del miocardio. Rev. Cubana de farmacia, Julio-Dic, 1995: p1-12.
54 .Gan SC, Bearer SK, Houck PM, Male Hose RF. Lawson HW, Chan L. Treatment of acute myocardial infarction and 30 day mortality among women and men. N Engl J Med 2000: 343 (1):8-15.
55. Spencer B: Acute Myocardial Infarction Are diabetics different? JACC 2000; 35 (3): 1513-5.
56. Boletín de Información terapéutica para APS: Boletín No. 10. CDF 1999.
57. Benetos A, Zureik M, Marcet J, Thomas F, Bean K, Safar M. A decrease in diastolic blood pressure in associated in men, JACC 2000; 35 (3) :673-80.
58. Provo TA, Frascane RJ. 12-Leal Electrocardiograms during basic the life support care. Prehosp Emerg Care. 2004 Apr-Jun; 8 (12): 212-6.
59. Antman EM. ACC/AHA. Guidelines for the management ST elevation Myocardial infarction. Circulation 2004; 110: 588-636.
ENCUESTA
Nombres y apellidos: ___________________________ Edad: _______Sexo: _______
Historia Clínica: _________
Dirección: ________________________________________
Factores de riesgo: ________________________________________________________
___________________________________________________________________
Antecedentes de Cardiopatía Isquémica Previa: Si _____ No _____
Peso Inicial: _______ Peso Final: _________
Talla: ___________
Tiempo entre el comienzo de los síntomas y el inicio del tratamiento: ________
Confirmación del IMA: Eléctrico ______ Enzimático ______ Ambos _______
Grado de Killip __________
Reacciones adversas por el uso de Fribrinolítico:
___________________________________________________________________
Reacciones adversas por el uso del GIK:
___________________________________________________________________
Reacciones adversas por el uso de Mg: ___________________________________________
Cifras de Colesterol: ______________ Cifras de Glicemia: ______________________
Complicaciones en la fase aguda: ________________________________________________
Complicaciones en la fase intrahospitalaria:
___________________________________________________________________
Tratamiento utilizado________________________________________________
Causas de la no trombosis: __________________________________________________
Lugar donde se realizó el tratamiento: ___________________________________________
Fallecido por: Causa cardiaca _______________________
Causa no cardiaca ______________________
Resultados de la necropsia: ____________________________________________
__________________________________________________________________
Observaciones: _______________________________________________________
___________________________________________________________________
Autores:
Dr. Yasser A. González Sosa. 1
Dr. Calixto Orozco Muñoz.2
Dra. Llilian Rodríguez Pérez 3
Dra. Maria Esther García Enríquez 4
Dr. Mariano Seiglie Rebollar 5
1 Dr. en Medicina. Especialista de 1er grado en Medicina Interna. Profesor Instructor del Hospital General Docente de Remedios. Instituto Superior de Ciencias Medicas de Villa Clara. Cuba.
2 Dr. en Medicina. Especialista de2do grado en Medicina General Integral. Profesor Asistente. Instituto Superior de Ciencias Médicas de Villa Clara. Cuba.
3 Dr. en Medicina. Especialista de 1er grado en Pediatría. Instructor. Policlínico Universitario de Remedios. Instituto Superior de Ciencias Médicas de Villa Clara. Cuba.
4 Dr. en Medicina. Especialista de 1er grado en Medicina General Integral. Instructor. Sede Universitaria de Remedios. Instituto Superior de Ciencias Médicas de Villa Clara. Cuba.
5 Dr. en Medicina. Especialista de 1er grado en Medicina Interna. Profesor Asistente. Sede Universitaria de Remedios. Instituto Superior de Ciencias Médicas de Villa Clara. Cuba
6 Dr. en Medicina. Especialista de Primer grado en Bioestadística. Instructor. Sede Universitaria de Remedios. Instituto Superior de Ciencias Médicas de Villa Clara. Cuba
Instituto Superior de Ciencias Médicas de Villa Clara Dr. Serafín Ruiz de Zárate Ruiz. Santa Clara. Villa Clara. Cuba.