Clasificación, espectro antimicrobiano, mecanismo de acción, principales características farmacocinéticas, efectos indeseables más frecuentes y graves, usos, interacciones, contraindicaciones, preparados y vías de administración.
Guia para el estudio de los Aminoglucosidos y Macrolidos, para estudiantes de pre y postgrado de la carrera de Ciencias Médicas.
Material de apoyo complementario al tema 1: Medicamentos capaces de actuar sobre los organismos biológicos.
SUMARIO
Clasificación, espectro antimicrobiano, mecanismo de acción, principales características farmacocinéticas, efectos indeseables más frecuentes y graves, usos, interacciones, contraindicaciones, preparados y vías de administración.
OBJETIVOS.
Relacionar el uso de los antimicrobianos en la práctica médica a partir de su espectro de acción, su principal mecanismo de acción, características farmacocinéticas, efectos indeseables e interacciones medicamentosas y mencionar los preparados y vías de administración mas empleados.
Estructura Química de los Aminoglucósidos
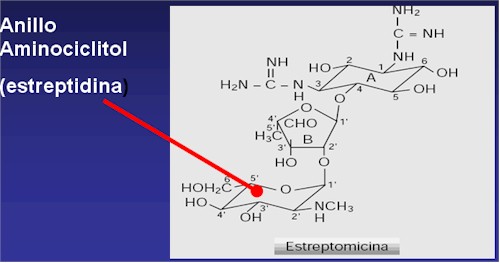
Los aminoglucósidos o aminociclitoles poseen dos o tres aminoazúcares ligados por puente glicosídico a un núcleo central de hexosa, aminociclitol. En el caso de la estreptomicina el núcleo es la estreptidina, el resto de los medicamentos de este grupo tiene un núcleo de 2-desoxiestreptamina. Al anillo aminociclitol se unen por enlaces glucosídicos dos o más azúcares con grupos amino o sin ellos.
Aunque la relación estructura-actividad de este familia no se conoce completamente, se sabe que cuando se modifican algunos grupos hidroxilo y amino unidos a los diferentes anillos, bien por procedimientos de síntesis química o por la acción de diferentes enzimas bacterianas, se produce la perdida de actividad antibacteriana.
Espectro Antimicrobiano
- Bacilos gram negativos aerobios y facultativos.
- Gram positivos.
- Micoplasmas,Legionellas, Neisserias ,y Micobacteria Tuberculosis
En la familia se distingue en primer lugar la estreptomicina. Otros derivados semisintéticos del streptomyces lo constituyen: Kanamicina que a través de modificaciones químicas que se hizo a su molécula se obtuvo
Derivados de las micromonosporas tenemos en primer lugar la: Gentamicina de la cual se obtuvo
De forma general a la hora de emplear un aminoglucósido, con el advenimiento de otros antibióticos con más amplio espectro y potencia y menor toxicidad, se deben valorar datos bacteriológicos y farmacológicos que contemplen las resistencias de este grupo.
Sus acciones se basan fundamentalmente frente a:
Bacilos gram negativos aerobios y facultativos: Enterobacter, Klebsiella, Pasteurella, Proteus, Yersinia, Salmonella, Shigella, Serratia, Brucella, Citrobacter, Aeromona, Alcaligenes, Acinetobacter, B.anthracis, E.coli, así como Pseudomonas.
Gram. Positivos: Su acción es limitada
Micoplasmas, Legionellas, Neisserias y Micobacteria tuberculosa.
Neomicina
Kanamicina
Paramomicina
PARENTERAL
Estreptomicina
Kanamicina
Gentamicina
Amikacina
Tobramicina
Sisomicina
Netilmicina
Espectinomicina
Dibekacina
Sagamicina
Mecanismo de Acción.
Los aminoglucósidos ejercen su acción bactericida inhibiendo la síntesis de proteínas a nivel del ribosoma específicamente en la unidad 30 S, en condiciones aerobias los aminoglucósidos ejercen una acción bactericida por un mecanismo de acción no conocido todavía completamente, pero en el que con seguridad participa la inhibición de la síntesis de proteínas.
Para ejercer su acción, los aminoglucósidos tienen que penetrar en el interior de las bacterias; por un proceso activo puesto que estos antibióticos son compuestos catiónicos, hidrófilos, que pasan con dificultad las membranas por simple difusión pasiva.
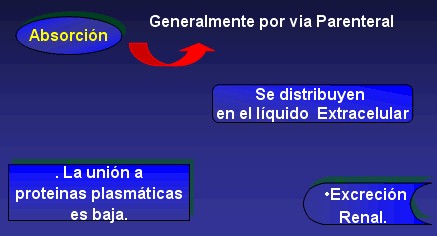
La absorción por el estomago e intestino delgado es casi nula debido a ser sustancias altamente básicas, sólo en pacientes con insuficiencia renal grave, la administración por vía oral puede llegar a producir concentraciones plasmáticas detectables por los procedimientos analíticos habituales, aunque no suelen ser suficientes para el tratamiento de infecciones sistémicas. La difusión tisular es escasa y limitada al liquido extracelular, excepto en la corteza renal, donde su concentración es mayor que en el suero. En general la concentración intracelular es más baja que la plasmática.
La administración parenteral es la de elección, alcanza el pico máximo a los 60 min. Cuando es administrado por vía IM y a los 30 min. cuando es administrado por vía IV.
La unión a proteínas plasmáticas es muy baja. Se distribuyen en el líquido extracelular.
La excreción es renal, a través del filtrado glomerular.
El tiempo de semivida de un aminoglucósido en personas con función renal normal es de aproximadamente de
Reacciones Adversas de Aminoglucósidos
Ototoxicidad: La toxicidad vestibular y acústica son efectos adversos demostrados tanto con el uso de la estreptomicina, gentamicina, tobramicina, así como el alto efecto cocleotóxico de la kanamicina, neomicina y amikacina. Clínicamente el paciente reporta zumbido de oídos, mareos, sensación de plenitud ótica y al realizar estudios pertinente estos pueden arrojar disminución o alteraciones en el audiograma.
Nefrotoxicidad: Siendo la vía renal la principal para la excreción de este grupo, se va a producir un cúmulo del medicamento a dicho nivel, lo cual puede provocar la muerte y llevar al paciente al fallo renal Aunque la elevación de la creatinina es el elemento más conocido para detectar la nefrotoxicidad existen signos como la aparición en orina de B2 micro globulina en las primeras 24 h de administrado el fármaco. El riesgo de nefrotoxicidad es mayor en personas de edad avanzada, en mujeres, en pacientes con insuficiencia renal previa, estados de depleción de agua y sodio o acidosis metabólica
Bloqueo neuromuscular. Ocurre sólo cuando se alcanzan concentraciones muy altas de aminoglucósidos en la placa motriz. Estas concentraciones se producen si el antibiótico se administra en inyección rápida IV o si la absorción es muy rápida, como ocurre cuando se administran concentraciones elevadas de aminoglucósidos en líquido pleural o peritoneal. Por ello se recomienda realizar la administración IV en forma de infusión de 20 - 30 min y, en caso de utilizar los espacios pleural o peritoneal, emplear concentraciones más bajas.

Los aminoglucósidos interactúan con varias penicilinas.
La nefrotoxicidad de los aminoglucósidos resulta aumentada si se asocian a otros fármacos potencialmente nefrotóxicos: Metoxifluorano, Anfotericina B, Vancomicina, Cisplatino, Ciclosporina y Cefaloridina. El riesgo de ototoxicidad aumenta con la asociación a Acido etacrínico, siendo más dudoso el peligro con otros diuréticos del asa. La acción en placa motriz puede ser potenciada por los bloqueantes musculares de diversa naturaleza.
Los aminoglucósidos interactúan con varias penicilinas (incluidas las antipseudomonas) mediante formación de enlace covalente. Para ello se requiere una alta concentración de penicilina y representa la pérdida de actividad de los aminoglucósidos. Esto sucede in vitro si se mezclan las soluciones en el mismo frasco de infusión, pero puede ocurrir también in vivo si el paciente padece insuficiencia renal.
La Neomicina
Aplicaciones Clínicas
- Sepsis intrabdominales y ginecológicas.
- Brucelosis, Peste, Tularemia, Carbunco.
- Endocarditis por estafiloco aureus.
- Fibrosis quística, otitis externa maligna del diabético y en las quemaduras infectadas.
Asociados a anaerobios como el Metronidazol, Clindamicina y Cefoxitina, se usan en las sepsis intrabdominales y ginecológicas
Junto a la vancomicina y rifampicina se usan en la endocarditis por estafiloco áureos y meticilina resistente. Antiseudomonicos junto a ureidopeniclinas, Ceftazidima y Quinolonas .En la fibrosis quistica, en la otitis externa maligna del diabético y en las quemaduras sépticas. En asociación con
Macrólidos
Estructura Química de los Macrólidos
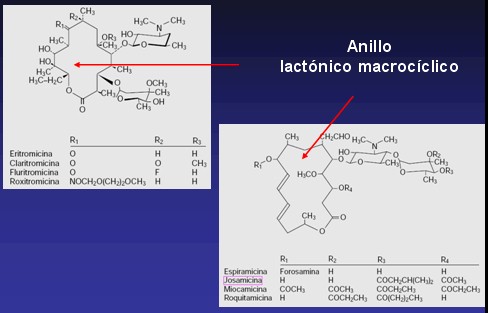
Bajo esta denominación se agrupa una serie de antibióticos que se caracterizan por la existencia de un anillo lactónico macrocíclico al que se unen diversos desoxiazúcares
El número de compuestos incluidos en este grupo ha experimentado un considerable aumento en los últimos años con el objetivo de:
a) mejorar la actividad antibacteriana de la eritromicina.
b) mejorar la absorción oral al obtener productos más estables en medio ácido.
c) prolongar la semivida y, por lo tanto, aumentar el intervalo entre dosis.
d) disminuir los efectos adversos especialmente de tipo gastrointestinal.
e) reducir el número y la importancia de las interacciones farmacológicas.
Espectro Antimicrobiano
Cocos Gram. Positivos: S.neumoniae, S.viridans,S. pyogenes,S galactiae ,S.aurues,
Cocos gram negativos: N.gonorrheae
Bacilos gram Positivos: Listeria, B.anthracis, Nocardia, Corynebacterium
Bacilos gram negativos: Haemophylus, Bordetella, Pateurella, Brucela
Espiroquetas: Leptospiras, T.pallidum, H.pylori, Campylobacter yeyuni
Germenes intracelulares: Mycoplasma , Clamydia, Legionella, Rickettsia, Urea plasma.
Ademas es efectivo en anaerobios exceptuando los bacteroides.
Desde un punto de vista químico pueden considerarse tres grupos de macrólidos:
a) los que poseen un anillo lactónico de 14 átomos: eritromicina, oleandomicina, roxitromicina, claritromicina, diritromicina y fluritromicina.
b) los que presentan un anillo lactónico de 15 átomos: azitromicina.
c) los que poseen un anillo de 16 átomos: espiramicina, josamicina, y rokitamicina
Los macrólidos poseen en general una potente actividad antibacteriana sobre la mayor parte de cocos grampositivos, muchas bacterias anaerobias, fundamentalmente las que constituyen la flora de la boca, y algunos bacilos grampositivos. Los bacilos gramnegativos, como se señaló en el apartado anterior, son intrínsecamente resistentes a los macrólidos.
La gran sensibilidad de los estreptococos (Streptococcus pneumoniae, S. pyogenes y S. agalactiae) a este grupo de antibióticos justifica su utilización como fármacos de primera elección en infecciones por estas bacterias en pacientes alérgicos a la penicilina.
Ningún macrólido es activo sobre estafilococos meticillín- resistentes ni sobre enterococos. Aproximadamente, el 80 % de las cepas de Staphylococcus aureus sensibles a meticilina son sensibles a los macrólidos, siendo la eritromicina el que presenta una mayor actividad.
Espiramicina, claritromicina y azitromicina poseen una actividad superior a los restantes macrólidos sobre Toxoplasma gondii.
Eritromicina
Roxitromicina
Claritromicina
Azitromicina
Carbomicina
Rosaramicina
Josamicina
Rokitamicina
Oleandomicina
Diritomicina
PARENTERAL
Eritromicina
Claritromicina
Azitromicina
Fluritromicina
Diritomicina
Mecanismo de Acción.
Efecto bactericida
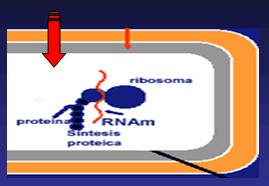
Los macrólidos inhiben la síntesis de proteínas a nivel de las subunidades 50s de los ribosomas bacterianos, bloqueando las enzimas que actúan en la translocación de la cadena proteica. Actualmente se acepta que los macrólidos del grupo de la eritromicina bloquean el proceso de traslocación del peptidil-ARNt en el ribosoma, mientras que los del grupo de la espiramicina inhiben la formación del enlace peptídico previo al proceso de traslocación.
Se destaca la propiedad importante de los macrólidos de penetrar en el interior de las células fagocitarias.
En un inicio se consideraban los macrólidos como bacteriostáticos, pero actualmente se sabe que llegan a tener efecto bactericida en dependencia fundamentalmente de la especie bacteriana, el tiempo de exposición, el tamaño del inóculo y la concentración que alcance el antibiótico en el lugar de la infección.
Características Farmacocinéticas
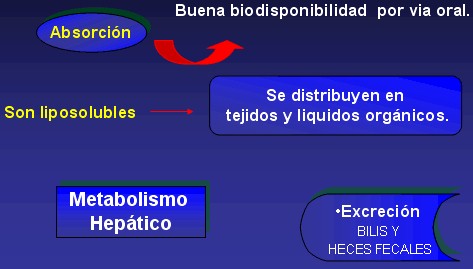
La eritromicina base es inactivada rápidamente en el medio ácido del estómago, por lo que se ha comercializado en forma de cápsulas con cubierta entérica. Además, para mejorar la biodisponibilidad oral de la eritromicina se han preparado diferentes sales (estolato, estearato, etilsuccinato o propionato) que son más estables en medio ácido. La vía IM es muy dolorosa, por lo que para administración parenteral sólo se utiliza la vía IV.
La absorción oral de los nuevos macrólidos es mejor que la de la eritromicina; la biodisponibilidad de la claritromicina es más del doble y la de azitromicina 1,5 veces mayor. La existencia de alimentos en el estómago influye de forma variable sobre la absorción de los macrólidos.
La distribución de los macrólidos es buena en todo el organismo.
Debido a su alta liposolubilidad, los macrólidos alcanzan concentraciones elevadas en la mayor parte de los tejidos y líquidos orgánicos.
Las concentraciones de azitromicina en la próstata, amígdalas, pulmón, riñón y mucosa gástrica son 10-100 veces superiores a las concentraciones plasmáticas y se mantiene durante días (t1/2: 2-4 días). También este antibiótico alcanza concentraciones superiores a las plasmáticas en los macrófagos alveolares, en la mucosa bronquial y en esputo.
El paso al LCR es escaso en general para los macrólidos en condiciones normales.
Los macrólidos son metabolizados por enzimas del sistema microsómico hepático citocromo P-450 (CYP3A4).
La excreción es básicamente por la bilis y las heces fecales.
Reacciones Adversas de los Macrólidos.
q Gastrointestinales
q Reacciones alérgicas
q Colestasis intrahepática
Este grupo de antibióticos se caracteriza por su escasa toxicidad, siendo uno de los más seguros de los que se utilizan en terapéutica
Las fundamentales reacciones son las gastrointestinales encontrándose entre ellas dolor abdominal acompañado de náuseas, vómitos, diarreas, meteorismo, epigastralgia.
Se han descrito reacciones alérgicas que cursan con erupción cutánea, fiebre y eosinofilia, que desaparecen al suspender el tratamiento.
Existe evidencia de coléstasis intrahepática con la oleandomicina y la eritromicina que es reversible al suspender el tratamiento. Se reportan casos excepcionales de estenosis hipertrófica del píloro en niños.
La tromboflebitis se ha reportado ante inyecciones intravenosas aunque son excepcionalmente raras.
En pacientes con antecedentes de arritmias o propensión a ellas se debe tener cuidado ya que este grupo puede inducir a prolongación del intervalo QT.
Se ha reportado en ancianos sordera que es reversible al suspender el tratamiento y toxicidad acústica.
Reducen el Metabolismo Hepático de otros fármacos METABOLIZADOS POR EL CIT-P50
EVITAR TRATAMIENTOS CONCOMITANTES
Interacciones farmacológicas. Los macrólidos pueden producir interacciones con otros fármacos por reducir su metabolismo hepático por enzimas del citocromo P-450
Debe evitarse el uso concomitante de fármacos metabolizados por enzimas del citocromo P-450
Aplicaciones Clínicas
• Alergias a las penicilinas.
• Neumonías.
• Sepsis por cocos Grampositivos del aparato respiratorio.
• Enfermedades obstructivas crónicas
Son ampliamente utilizados en pacientes alérgicos a las penicilinas. Constituyen primera elección en neumonía por Legionella pneumophila, micoplasma pneumoniae, tos ferina, difteria y afecciones gastrointestinales por Campylobacter yeyuni.
En la neumonía del anciano asociado a cefalosporinas, en la neumonía del adulto como monoterapia, en el acné, en la profilaxis de la cirugía colorrectal, la claritromicina ocupa especial lugar en la erradicación del helicobacter pylori.
En las sepsis por cocos Gram. positivos del aparato respiratorio o sea en sinusitis, otitis media, amigdalitis.
En las infecciones de la piel.
En cuanto a la azitromicina se ha comprobado su utilidad en la profilaxis de las enfermedades oportunistas en inmunodeprimidos, en las micobacteriosis atípicas, en la diarrea del viajero, el cólera, en
Además se ha comprobado su utilidad en las enfermedades obstructivas crónicas en la erradicación del germen y con efecto antinflamatorio evidente.
Ventajas de las monodosis: Menor efectos gastrointestinales, mayor adherencia al tratamiento, mayor resistencia a la degradación estomacal y ampliación de las propiedades terapéuticas.
Bibliografía
1-Malgor - Valsecia. Farmacología General.
2-Flores J. Farmacología Humana. 2004, Masson.
3-Goodman y Gilman. Las Bases Farmacológicas de la terapéutica,
Oncena Edición, 2006.
4-Rang HP, Dale. Pharmacology. 4ta edic, 1999.
5-Formulario OMS, 1994.
6-Morejón García Moisés. Actualización de Antimicrobianos Sistémicos.
Editorial Ciencias Médicas. 2005.
7- Formulario Nacional de Medicamentos. Editorial Ciencias Médicas.
2006
Autores:
1- Dr. Marco J. Albert Cabrera.
Master en Ciencias. Especialista de Primer y Segundo Grados en Medicina Interna Profesor Auxiliar del ISCM-Habana
2- Dra. Lina Martínez Acosta.
Especialista de 1er Grado en Medicina General Integral. Profesor Instructor del ISCMH.
3- Dra. Sirsi Guilarte Díaz
Especialista de 1er Grado en Medicina General Integral. Profesor Instructor del ISCMH.
4- Lic. Arelys Reyes Expósito.
Licenciada en Ciencias Farmacéuticas. Profesor Instructor del ISCMH.