Varios estudios han demostrado la existencia de anomalías moleculares, como la pérdida de la heterocigosidad en loci cerca de genes supresores de tumor y la sobre expresión de p53 en las células madres del limbo corneal así como también la inactivación de p53 ligada a la infección por papillomavirus humano (VPH) (5,6,7). Dentro de lo factores ambientales las personas expuestas a los rayos UVB, UVA, calor y polvo tienen una alta incidencia de desarrollar esta patología, al igual que existe mayor incidencia en aquellos países que se encuentran cerca del Ecuador (8).
Existen reportes que asocian la presencia de agentes virales en el desarrollo de pterigium como Herpes virus, VIH, y papillomavirus humano (VPH); no obstante sus implicaciones en la etiología de pterigium todavía permanece controversial (9) (10) (11). Otros estudios han detectado la presencia de papillomavirus humano (VPH)H en lesiones conjuntivales premaligna y malignas, como el carcinoma epidérmico de la conjuntiva, donde además se ha reportado que la carga viral de papillomavirus humano (VPH) es mayor en las lesiones premalignas (8) (9) (12). La neoplasia intraepitelial de conjuntiva y córnea (NIC) es el tumor maligno más frecuente de la superficie ocular, durante su evolución clínica la neoplasia intraepitelial de conjuntiva y córnea (NIC) progresa lenta y continuamente pudiéndose transformar en carcinoma escamoso (12).
El propósito del presente estudio fue evaluar las características clínicas de pacientes con pterigium provenientes de países latinoamericanos como: Ecuador, Guatemala, Perú y Venezuela, determinar su asociación con infección por virus papiloma humano, e identificar la población de mayor riesgo de presentar lesiones premalignas y malignas de la conjuntiva.
Materiales y métodos
Un total de 51 pacientes de Ecuador, Guatemala, Perú y Venezuela, incluidos en el Programa Misión Milagro, fueron evaluados bajo consentimiento informado en el hospital de los Samanes Venezuela. Se les realizó keratometría, toma de presión intraocular, biomicroscopía. Fue empleada la clasificación del pterigium de la Academia Norteamericana de Oftalmología (13), que lo divide en primario: que va a ser trasplantado por primera vez, recidivante, si ha recibido uno o más tratamientos quirúrgicos previos y de acuerdo a su extensión en grado I, II, III y IV, con respecto al crecimiento sobre la córnea y la distancia del eje pupilar. Las técnicas quirúrgicas empleadas en los pacientes fueron de acuerdo al grado y recurrencia del pterigium.
Un fragmento se colocó en buffer formol para el diagnóstico histopatológico, y otro fue congelado a -70oC para el diagnóstico molecular de VPH. Extracción del ADN: El sedimento celular de las muestras fue digerido en 100 µl buffer de lisis (0,1% sarcosina; 10 mM Tris HCl, pH 8) y 100 µl Proteinasa K (1mg/ml), incubando durante, al menos, 3 horas a 42ºC. El ADN fue extraído mediante separación v/v con cloroformo-fenol/isoamílico y precipitación con 2 ½ volúmenes de etanol absoluto frío; se resuspendió en agua libre de nucleasas y se determinó la concentración espectrofotométricamente. La detección del genoma de VPH se realizó mediante la reacción en cadena de la polimerasa (RCP) (14), empleando los iniciadores genéricos MY09 y MY11. Se utilizaron los iniciadores PC04/GH20 para amplificar simultáneamente un fragmento del gen humano de β-globina como control interno de la integridad y calidad del ADN y ausencia de inhibidores de la RCP, obteniéndose un producto de 268 pb.
Se incluyó, además, un control negativo (mezcla de reacción + ADN de individuo negativo). Aproximadamente 1 µg del ADN fue añadido a la mezcla de reacción [0,4 µl dntp´s (100 mM); 0,2 µl de cada primer (100 mM); 6 µl de buffer Taq 10X; 4 µl de MgCl2 (50 mM); 0,5 µl (2,5 U) de Taq DNA polimerasa (Invitrogen); H2O libre de nucleasas hasta un volumen final de 40 µl]. La amplificación se realizó en un termociclador “Mini cycler” MJResearch (Ciclos: 4 min. a 94 ºC, 40 por [15 seg. a 94 ºC, 30 seg. a 55 ºC, 45 seg. a 72 ºC] y una extensión final de 7 min. a 72 ºC). La tipificación se realizó con el kit MP-70078 “MPCR Kits for Human Papillomaviruses” (Maxim Biotch, Inc.) que permite tipificar los tipos 6 y 11 de bajo riesgo, y los tipos 16, 18 y 33 de alto riesgo oncogénico. Los amplificados fueron visualizados mediante electroforesis en gel de agarosa al 2%.
Se realizo la relación de dependencia de variables cruzadas utilizando la prueba de independencia de Chi2, programa Statxact ® versión 8.0.Los datos fueron presentados en tablas de contingencia para su análisis.
Resultados
De los 51 pacientes evaluados, el 49% (25/51) procedían del Ecuador, 23% (12/51) de Perú, 15% (8/51) fueron venezolanos y 11% (6/51) de Guatemala. 60.7% fueron masculino y 39.2% femenino. El tipo de pterigium que se observó con mayor frecuencia fue el primario 76,6% (39/51) mientras que el recidivante se presento en un 23,5% (12/51). La distribución de los casos de pterigium según su procedencia y grado de biometría se presenta en la Tabla 1.
Tabla 1
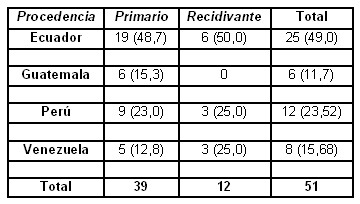
Frecuencia de casos de según procedencia y tipo de pterigium
Tabla 2
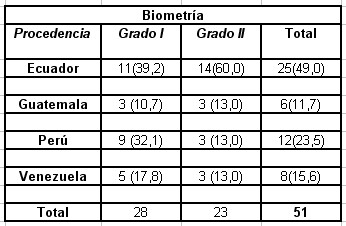
Frecuencia de casos de pterigium según procedencia del paciente y grado de biometría.
El mayor porcentaje de lesiones grado I, 39,2% (11/25) se observó en los pacientes de Ecuador seguido de 32,1% (9/12) de Perú y 17,8% (5/8) de Venezuela. El grado II se presentó mayormente en pacientes de Ecuador (60%) (14/25), mientras que valores iguales se observaron para Guatemala Perú y Venezuela (13%).
Tabla 3

Infección por papillomavirus humano (VPH) y riesgo oncogénico en pacientes con pterigium.
El diagnóstico molecular para detectar el genoma viral demostró que 47% (24/51) de las muestras presentaron infección por papillomavirus humano (VPH) y el 50,9% fueron negativas; una muestra resultó insuficiente para realizar la prueba. De los casos positivos para papillomavirus humano (VPH) el 70,83% (17/24) resultaron de bajo riesgo y 12,5% (3/24) de alto riesgo oncogénico, cuatro de las muestras positivas no se pudieron tipificar con la prueba utilizada en el estudio.