Hormona Somatostatina y Analogos Radiomarcados en Tratamiento de Tumores Neuroendocrinos.3
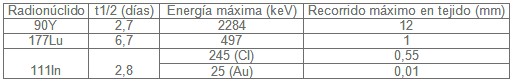
Por tanto, la selección del radionúclido se basa en el tiempo de vida media, tipo y energía de radiación emitida y distancia sobre la cual es depositada (recorrido máximo en tejido) (Tabla nº 2). Así, los radionúclidos emisores de partículas energéticas asociados a análogos de la somatostatina, pueden depositar dosis de radiación citotóxica con una alta transferencia de energía lineal (LET; parámetro relacionado con la probabilidad de eliminar células) selectivamente sobre tumores que expresen receptores de la somatostatina. 25
En cuanto al tiempo de vida media (t1/2; tiempo requerido para reducir el número inicial de átomos radioactivos a la mitad), éste se relaciona inversamente con la velocidad a la cual la dosis de radiación absorbida es depositada sobre la célula. Así, una mayor velocidad de deposición de la dosis (t1/2 corto) es mejor frente a tumores que se dividen rápidamente (rápido crecimiento). Mientras que un t1/2 largo puede ser más efectivo en tumores de crecimiento relativamente lento como la mayoría de los Tumores neuroendocrinos. 26
Si bien las propiedades físicas del radioisótopo son importantes, pues la heterogeneidad tumoral puede causar respuesta incompleta; el fuego cruzado, dosis radiacional proveniente del radionúclido localizado sobre las células tumorales positivas (expresan receptores de la somatostatina), puede eliminar las células tumorales negativas (no expresan receptores de la somatostatina) más cercanas. 26
La radiosensibilidad tumoral es de suma importancia en el éxito de la radioterapia dirigida. De ahí que, cuando dos tumores poseen similares niveles de receptores peptídicos, aquel que sea más radiosensible será un mejor candidato para la radioterapia metabólica. Sin embargo, aún no está claro, si un tumor radiosensible que usualmente tiene baja densidad de receptores de somatostatina sea un buen candidato para la radioterapia metabólica. 26
Otro aspecto importante a considerar es el denominado, efecto bystander, relacionado con las respuestas biológicas observadas en células, cuyas células vecinas son irradiadas sin recibir radiación las primeras. Estudios reportan tasa de mutación incrementada y tasa de sobrevida disminuida en estos casos. Estas observaciones han negado un criterio general en la radiobiología basado en que el daño celular es causado sólo por ionización directa o por radicales libres generados, como una consecuencia de la deposición de la energía en el interior del núcleo. No obstante, el rol del efecto bystander como promotor de la eficacia radioterapéutica está aún por ser determinada. 24
Otra ventaja de la radioterapia metabólica, es que la radiación puede ser depositada selectivamente no sólo en tumores primarios y metástasis grandes sino también en aquellos que son muy pequeños para ser visualizados e identificados por técnicas imagenológicas, para ser eliminados por cirugía o radioterapia externa. 26
Tabla.2 Propiedades físicas de los radioisótopos usados comúnmente en la radioterapia dirigida de los Tumores neuroendocrinos.
Dosimetría paciente específica
Debido a la alta variación individual entre pacientes, se requiere hacer cálculos dosimétricos paciente-específico antes de usar el agente radioterapéutico. Los métodos dosimétricos previos a la radioterapia metabólica, se emplean para confirmar el sitio del tumor primario y sus metástasis; evaluar la densidad de receptores en el tumor y estimar la dosis radiacional sobre órganos críticos (médula ósea y riñones) y tejidos tumorales. Tales datos permiten individualizar regímenes terapéuticos, identificar los pacientes que podrían beneficiarse con el tratamiento y excluir aquellos que no. 26,27
La Centelleografía de Receptores Peptídicos (CRP) con 111In-DTPA-octreotide (Octreoscan) o 177Lu-DOTA-octreotate, es una modalidad diagnóstica por imágenes muy sensible en la localización de Tumores neuroendocrinos primarios y metastáticos. Esta técnica puede ser empleada fácilmente en las estimaciones dosimétricas, corregidas por la medición del volumen preciso del órgano por Tomografía Axial Computarizada o Resonancia Magnética Nuclear, siempre y cuando sea necesario. 26
Criterios de inclusión
Los pacientes elegibles para la radioterapia metabólica, son aquellos con tumor inoperable, tumor metastático y con sobre-expresión de receptores para somatostatina en todos los sitios comprometidos; reserva medular; hemoglobina > 10 g/l, glóbulos blancos > 3.0*109 /l y plaquetas > 100*109 /l; urea <10 mmol/l; creatinina <160 mmol/l; velocidad de filtración glomerular > 40 ml/min; reserva hepática medida por perfil hematológico convencional; buen estado general y tiempo de recuperación de dos meses, si se ha utilizado quimioterapia previamente. 28
Las contraindicaciones son: embarazo, lactancia, mielosupresión, compromiso metastático extenso de la médula ósea, compromiso de la función renal e insuficiencia renal crónica, compromiso hepático extenso, haber alcanzado la dosis límite por dosimetría paciente específica y estado general deteriorado. 28
Agentes terapéuticos
A fines de los ochenta, se obtiene el 111In-DTPA-octreotide (Octreoscan),29 basado en el acoplamiento del análogo octreotide al agente quelante bifuncional ácido dietilendiaminotetraacético (DTPA), encargado de aportar los grupos reactivos necesarios para el acoplamiento del radiometal. El Octreoscan, es el radiofármaco peptídico más ampliamente usado en el diagnóstico de patologías malignas. Su utilidad para la radioterapia metabólica ha sido sugerida, pues el 111In emite electrones Au y electrones de CI con LET elevada, que puede ocasionar efectos radiotóxicos letales sobre la proliferación tumoral, siempre y cuando, este localizado a unos pocos nanómetros del ADN del núcleo. Sin embargo, tales partículas exhiben poca penetrabilidad tisular y en consecuencia, eficacia limitada en tumores grandes y pacientes en estadío terminal. 30
Además, el DTPA no es un agente quelante (BFCA) adecuado para acomplejar emisores beta, ya que exhibe disociación del metal in vivo. Como alternativa, se desarrolló un nuevo BFCA, el poliamino carboxilato macrocíclico ácido 1,4,7,10 tetraazaciclododecano-N,N’,N’’,N’’’-tetraacético (DOTA)31, capaz de formar complejos muy estables con diversos iones metálicos bajo condiciones fisiológicas. En la Fig.1 se representan los derivados de la somatostatina acoplados a DOTA más empleados: 90Y-DOTA0-Tyr3-octreotide (90Y-DOTATOC, 90Y-SMT-487), 90Y-DOTA-lanreotide (MAURITIUS) y 177Lu-DOTA-Tyr3-The8-octreotate (177Lu-DOTA-TATE).26
Fig.1 Radiofármacos basados en análogos de la somatostatina acoplados a DOTA, más empleados en la radioterapia metabólica de los Tumores neuroendocrinos.
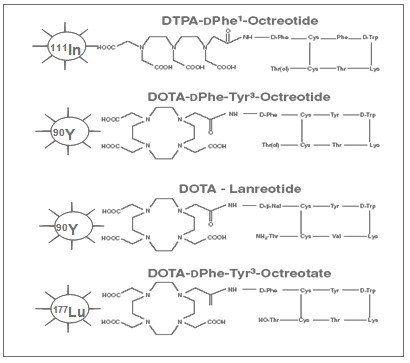
Estos difieren con respecto al perfil de afinidad por los receptores de la somatostatina. Si bien, el DTPA-OC enlaza con alta afinidad a sstr2, moderada a sstr3 y sstr5, y no reconoce a sstr1 y a sstr4. 32 El derivado DOTA-TATE posee un incremento de la afinidad por sstr2 en nueve veces con respecto al DOTA-TOC, incluso una vez que el mismo es marcado con 90Y mantiene una afinidad mayor en seis o siete veces. 33 Sin embargo, exhibe una reducción notable de su reconocimiento por el resto de los receptores de la somatostatina. Mientras que el DOTA-lanreotide tiene la menor afinidad por sstr2 pero muestra moderada afinidad por sstr3-sstr5.34 No obstante, tanto el DOTA-TOC como el DOTA-TATE exhiben mayor captación tumoral que el DOTA-lanreotide, siendo más difundidos los primeros en el tratamiento de los Tumores neuroendocrinos, ya que el sstr2 se encuentra altamente expresado en estas lesiones malignas. 35