Articulo de revision. Sustitutos plasmaticos en terapia intensiva.5
Atendiendo al peso molar (PM), tasa de sustitución molar (TSM), la relación C2/C6 y la concentración se caracterizan de la siguiente manera:
Peso molar:
Alto: 450 - 480
Medio: 130 - 200
Bajo: 40 – 70
Tasa de sustitución molar:
Elevada: 0,6% - 70%
Baja: 0,4 – 05%
Relación C2/C6:
Elevada > 8
Baja < 8
Concentración:
Elevada 10%
Baja 6%
El metabolismo varía entre las diferentes hidroxietilalmidones (HEA), para los de peso molecular alto la vida media plasmática es de 7,2 días, en hígado: 132 días y en bazo: 64 horas. Se excretan por riñón 74%, heces 11% y el 15% en reservas corporales. La molécula no es antigénica y guarda relación estructural con el glucógeno hepático.
Degradados por alfa-amilasas rompiendo los enlaces 1,4; los 1,6 no son hidrolizados (ramificación), y por maltasas e isomaltasas, la hidroxilación en C2 ofrece la mayor resistencia a la degradación de moléculas con TSM alta y C2/C6 elevada, se eliminan mayormente por el sistema retículo endotelial (SRE).
Se produce acumulación plasmática (cuanto más elevada la TSM y la relación C2/C6 mayor acumulación). La eliminación es renal en moléculas de peso molecular entre 50 – 70 kDa. La eliminación es rápida durante las primeras horas y luego hay una fase de eliminación lenta, se eliminan por riñón pero una semana después se puede encontrar en orina concentraciones bajas. (8,9)
En pacientes hipovolémicos el hidroxietilalmidón (HEA) 200/0,5 -10% eleva la volemia un 150% a los 60 minutos y mantiene un 124% a los 180 minutos. Por otra parte el hidroxietilalmidón (HEA) 200/0,6 - 6% eleva la volemia igualmente un 150% a los 60 minutos pero un 165% a los 180 minutos, un 130% a las 6 horas y un 50% a las 24 horas. La concentración ideal tiende a ser del 6% en vez del 10%. (25,26)
Se acumulan en tejidos, (hepático, renal y cutáneo), en células con intensa actividad macrofágica, dependiendo de la dosis, pudiendo persistir por varios meses a nivel muscular, intestinal y cutáneo. (27)
También puede producirse prurito, no observándose a bajas dosis, con localización en tronco, muslos y periné, pudiendo persistir por 8 – 9 semanas (posiblemente por depósito en la dermis de hidroxietilalmidones - HEA) no estando implicada la histamino-liberación. (28)
Modifican el: TTPa, TT, TS, activadores de los factores VIIIc, factor de la ristocetina (vWCo) y tiempo de lisis de las euglobulinas. El efecto sobre el complejo Willebrand se debe a la acumulación de grandes moléculas de HEA, el aumento de la presión coloide-oncótica (PCO) y del volumen plaquetario. Disminuyen la actividad endotelial y previenen la adhesión de neutrófilos. (29)
La perfusión está limitada a 20ml/kg de hidroxietilalmidones (HEA) 450 al 6% porque altera la polimerización de la fibrina. A 33 ml/kg para el hidroxietilalmidón de peso molecular medio y 20 ml/kg en días subsiguientes; dosis máxima total 80ml/kg. Los hidroxietilalmidones (HEA) 200/0,6 no se deben utilizar más de tres días, pueden producir hiperamilasemia (2– 4 veces) máxima a las 12 horas y desaparece entre las 24 a 72 horas. (27) Las características farmacológicas y clínicas principales de diferentes tipos de hidroxietilalmidón se muestran en la tabla 4.
La metabolización en polímeros de almidón y glucosa puede presentar riesgo de hiperglucemia, aunque cuando la molécula es degradada a peso molecular entre 40.000 – 50.000 Da es filtrada por el riñón.
Tabla 4. Características de los hidroxietilalmidones. (8,9)
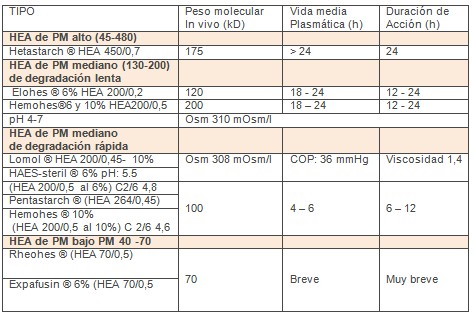
Dentro de las características que diferencian los diferentes grupos de sustitutos plasmáticos se encuentra la capacidad de retención de agua (H2O) que se comporta así:
Gelatina 40 ml/H2O x gramo (menos eficaz, duración corta del efecto)
Dextrán 35 – 40 ml/H2O x gramo.
HEA 200 30 ml/H2O x gramo.
En relación con la presión coloide-oncótica (PCO) el comportamiento es:
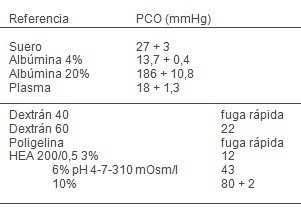
Los factores que condicionan la difusión (expansión) son la forma; globular o lineal, el tamaño (+ 35 Å de diámetro) y la carga eléctrica.
Es mejor que las soluciones macromoleculares estén diluidas en soluciones electrolíticas para mejorar la presión hidrostática intersticial y la circulación linfática. La duración de la expansión depende del estado dinámico de la permeabilidad de la membrana basal endotelial. (9,30,31)
La disminución de hematocrito, el aumento del flujo sanguíneo y la disminución de las presiones intravasculares, junto con la disminución de la viscosidad, constituyen las características que debe poseer el sustituto ideal, que debe mantener la presión coloide-oncótica (PCO), con baja viscosidad plasmática y sanguínea a baja velocidad de cizallamiento y con efecto de antiagregación de eritrocitos. (Efectos reológicos)