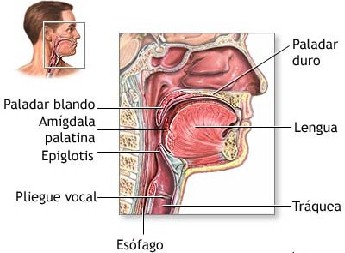
Otitis Media Secretora 6.
Comentario
Streptococcus pneumoniae (Spn) es un patógeno importante que coloniza la vía aérea superior; es el principal agente causal de las neumonías de la comunidad, otitis media, sinusitis y sepsis en los menores de 5 años. En los países que ya incorporaron la vacuna conjugada anti Haemóphilus influenzae tipo b con amplias coberturas, es el primer agente causal de meningitis en ausencia de brotes epidémicos de Neisseria meningitidis.
En los últimos años la aparición de cepas de Spnresistentes a penicilina y a otros antimicrobianos, ha complicado las estrategias terapéuticas para los tratamientos empíricos iniciales, especialmente en meningitis y otitis media aguda (OMA). Muchos de los Spn resistentes a penicilina, en particular los de alta resistencia, presentan CIMs aumentadas a cefalosporinas de 3° generación, lo que complica aún más el manejo terapéutico de las meningitis.
En un estudio multicéntrico de vigilancia epidemiológica organizado por la OPS que se desarrolla en el país y en otros países latinoamericanos, a través del grupo Sistema Regional de Vacunas (SIREVA), para el período 1993-1999, se registró sobre 1171 aislamientos una resistencia global del 31.4%, siendo de alto nivel 16.6% y de nivel intermedio 14.8%. La resistencia a cefotaxima fue del 29.6%, cefuroxime 28%, y cotrimoxazol 68%, lo que expresa la magnitud del problema especialmente en el tratamiento de las infecciones invasivas.
En el estudio SIREVA se detectaron los serotipos predominantes en el país siendo en orden decreciente el 14, 6A/6B, 5, 1, 23F, 19F, y 19A. Los serotipos más asociados a resistencia a penicilina fueron el 14 y 23F.
La problemática con las vacunas polisacáridas es que para ser efectivas en menores de 2 años requieren ser conjugadas es decir ligadas a una proteína que actúa como transportadora o “carrier”, permitiendo así que el sistema inmune responda al antígeno polisacárido. Esta conjugación con el antígeno proteico logra que el sistema inmune genere una respuesta T dependiente en los menores de 2 años.
La primera vacuna conjugada fue la anti Hib y con este modelo se continuó trabajando para lograr las actuales vacunas antineumocóccicas conjugadas que usan las mismas proteínas transportadoras que las vacunas anti Hib.
La actual vacuna aprobada por la FDA y el ACIP en Estados Unidos es una vacuna heptavalente (contiene 2 µg de los serotipos 4, 9V, 14, 18C, 19F y 23 F y 4 µg de 6B conjugada con una proteína transportadora CRM197 (mutante no tóxico de toxina diftérica). Estos serotipos son responsables del 83% de las enfermedades invasivas por Spn en menores de 4 años. en Estados Unidos.
La vacuna se recomienda a partir de los 2 meses de vida con un esquema semejante a las vacunas antiHib, 2, 4 y 6 meses de vida con un refuerzo entre los 12 y 15 meses de edad.
Según los datos disponibles a través del estudio SIREVA en Argentina (Centro Nacional de Referencia ANLISS Malbran), en el período 1993-99, los serotipos de la vacuna conjugada heptavalente actualmente aprobada en Estados Unidos, cubriría el 53.6 % de los serotipos aislados de infecciones invasivas por Spn. en menores de 5 años en la Argentina. Cuando se consideraron los serotipos con algún grado de resistencia a penicilina de los contenidos en la vacuna, estos representan el 64.1%.
Esta vacuna es sin embargo un importante avance en la prevención de las infecciones invasivas por Spn, y sería importante evaluar en el país los alcances de su uso.
Por otra parte sería de suma importancia conocer cuáles son los serotipos de Spn prevalentes en OMA a nivel nacional para poder evaluar los alcances de este nuevo conjugado en esta patología prevalente en la infancia.
CONCLUSIÓN
La vacuna heptavalente conjugada es segura y efectiva en prevenir la meningitis y neumonía por neumococo en niños. Es menos efectiva en la prevención de la otitis media. Se recomienda la vacunación de todos los niños menores de 2 años de edad y de los niños de alto riesgo entre los 2 y 5 años.
Med Letter 2000; 42 (1074):25-27
Como se menciona en el presente trabajo, en la mayoría de los casos la otitis media secretora (OMS) cursa de manera asintomatica, por lo que consideramos que se debería realizar un examen físico de rutina en lactantes y niños con el fin de detectar precozmente esta patología e instaurar el tratamiento adecuado.
Proponemos esta conducta en base a que la OMS persistente no es inocua, pudiendo llevar a la fibrosis irreversible de la membrana timpánica. Por otra parte conlleva una repercusión institucional en niños de mayor edad, ya que debido a la hipoacusia existe retraso en el aprendizaje, con bajo rendimiento escolar.
Bibliografia
1. DIAMANTE, Vicente Guillermo. “Otorrinolaringología y afecciones conexas” Editorial Promed.
2. http: www.orbita.starmedia.com.
3. http: MEDLINEplus Enciclopedia médica
4. http: www.otorrino.homestead.com.
5. http: cspt.es.)Universidad de Sabadelli)
6. http: elotorrino.com.
7. Angela Gentile
(Infectóloga pediatra, Jefe de Epidemiología del Hospital de Niños “Ricardo Gutierrez”)
8. Raúl O. Ruvinsky
(Infectólogo pediatra, Jefe del Departamento Materno-Infantil y coordinador del Grupo de Trabajo de Infectología, Hospital “Carlos G. Durand”)
9. http: www.OTL.org.ls
10. 1. SCHAPPERT SM. Office visits for otitis media: United States, 1975-90. Hyattsville, MD: United States Department of Health and Human Services, Public Health Service, Centers for Disease Control, (Advance data no. 214), 1992.
11. 2- Advance Data. Vital and Health Statistics of the Centers for Disease Control, National Center for Health Statistics. Office Visits for Otitis Media: United States,1995-1990. 214:20, 1992.
12. 3- HOWIE VM, PLOUSSARD JH, SLOYER J. - The “otitis prone”condition. Am J Dis Child 129:676, 1975.
13. 4- TEELE W.V., KLEIN J.O., ROSNER B. and the Greater Boston Otitis Media Study Group. Epidemiology of Otitis Media during the first seven years of life in children in greater Boston: a prospective study. J lnfect Dis. 160:83-91,1989.
14. 5- BLUESTONE C.D., STOOL S.E. & KENNA M.A.- Pediatric Otolaryngology, Vol 2. Pittsburgh. 3rd ed. W.B.Saunders. 22:388-582, 1996.
15. 12- SIH TM, Otite Média Secretora e Otite Média Recorrente. In: Sih TM, Manual de Otorrinolaringologia Pediátrica da Interamerican Association of Pediatric Otorhinolaryngology, Ed. Edusp,São Paulo, 217-227, 1997.
16. 13- BLUESTONE CD, STEPHENSON JS, MARTIN LM. Ten-year review of otitis media pathogens. Pediatr Infect Dis J. 11:S7-S11, 1992.
17. THE PNEUMOCOCCAL STUDY GROUP IN BRAZIL FOR THE SIREVA PROJECT. Prevalence of serotypes and antimicrobial resistance of Streptococcus pneumoniae strains isolated from Brazilian children with invasive infections. Microbial Drug Resist. 3:141-146, 1997.
18. DIAS CG, D'AZEVEDO P, KADER I, SUPERTI S, CARVALHO MG, FACKLAM RR, TEIXEIRA LM. Distribuição de sorotipos e susceptibilidade à penicilina entre amostras de Streptococcus pneumoniae isoladas em Porto Alegre, RS. Resumos do XIX Congresso Brasileiro de Microbiologia. 7;96, 1997.
19. 24-MENDES C, SADER H, DAINESI SM, DIAS CG, COSCINA A, ZOCCOLI C, SILVA JF, MAGALHÃES M, TEIXEIRA LM, SOUZA HHM, OPLUSTIL CP, ANDRADE MG, MIMIÇA L, MIMIÇA I. Evaluation of the antimicrobial activity of sparfloxacin, relative to other oral antibiotics against 1,125 bacterial isolates from 10 medical centers in Brazil. Braz J Infect. Dis. 2(1):18-24, 1998.
20. 25-TEIXEIRA LM, ANDRADE JRC, LOURENÇO NJ. Serotypes and antimicrobial susceptibility to Streptococcus pneumoniae isolates in Rio de Janeiro, Brazil Rev Microbiol. São Paulo. 19:93-94, 1998.
21. KOSKELA M, LEINONEN M, HÄIVÄ V-M, TIMONEN M, MÄKELÄ PH. First and second dose antibody responses to pneumococcal polysaccharide vaccine in infants. Pediatr Infect Dis. 5:45-50, 1986.
22. http://www.avera.org/adam/esp_ency/article/001336.htm