Modelo de estudio del choque directo radioactivo independiente del efecto peroxido .7
Obsérvese los cambios producidos por la inducción de sangre normal edetatada, cultivada en medio mínimo, con fluoruro de sodio, que es un inhibidor de diversos sistema enzimáticos y reduce la respiración celular y la glucólisis anaerobia. Al eliminar la respiración celular induce una cierta anaerobiosis, de modo que la célula debe metabolizar la glucosa en anaerobiosis pero encuentra bloqueada la ruta por acción del fluoruro. Se observan una paraforma inmadurativa de intensa regeneración (inferior) y un neutrófilo en apoptosis (inmediato superior).
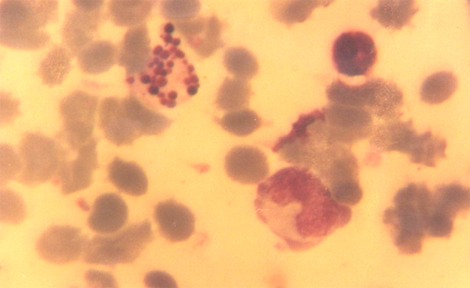
Idem anterior, con fluoruro de sodio. Nótese la involución de un neutrófilo a una paraforma semejante a un metamielocito neutrófilo, y la apoptosis completada del neutrófilo superior.
La acción del impacto directo radiactivo tendría lugar, primordialmente, en el núcleo, aunque también ataca la membrana citoplasmática y nuclear, y otras estructuras de membrana, abriendo cilindros de ionización.
Los radicales libres formados por la acción indirecta de la radiación sobre el agua celular, producirían la peroxidación de los lípidos de membrana instalando una lesión más generalizada a ese nivel que el choque directo, y podrían interferir en la cascada oxidativa de la fosforilación mitocondrial oxidando a los equivalentes reductores e instalando la microaerobiosis o la anaerobiosis. También pueden atacar el DNA nuclear en los mismos sitios que el impacto balístico de la radiación.
La existencia del aparato de Golgi no puede demostrarse cuando las células se tratan con solventes de las grasas, y es positivo a la reacción de Millon y de las enzimas proteolíticas, debido a lo cual se encuentra constituido por lipoproteínas. El bajo peso específico del Golgi sugiere que es muy rico en lípidos, entre los que se encuentran cefalina, lecitina y esfingomielina. Es por ello que el aparato de Golgi sería un blanco de elección del efecto peróxido radioactivo, y por su ubicación perinuclear tomaría cuenta de los radicales libres surgidos por las acción del bombardeo radioactivo sobre el agua del hipotético halo perinuclear, impidiendo que los mismos lleguen en cantidad apreciable al núcleo celular. Esta situación avalaría nuestra suposición de que los radicales libres surgidos de la ionización del agua nuclear por la acción radioactiva, serían los únicos radicales involucrados en la lesión del DNA nuclear, que se sumarían a las lesiones producidas por el impacto directo de la radiación sobre el ácido nucleico.
La alta densidad electrónica de los ribosomas los haría, como al núcleo celular, un blanco predilecto de la acción radioactiva; de modo tal que los RNA soportarían en sus moléculas lesiones indirectas copiadas de las lesiones producidas sobre el DNA por la radiación, y lesiones directas de clivaje por el efecto impacto o peróxido del radionucleido. El resultado final sería la síntesis de proteínas anómalas, o la inhibición de la síntesis de proteínas como en los linfocitos, en los cuales la radioactividad puede inhibir la producción de anticuerpos.
Veremos luego que los cambios o lesiones en las inducciones por agentes tanto químicos como radioactivos, hacen blanco fundamentalmente en la heterocromatina nuclear, produciendo el desenrollamiento de la misma y permitiendo la expresión de genes callados, que se inhibieron en el proceso de diferenciación celular. Tales genes codifican la información para la síntesis de proteínas metabólicas y estructurales de la célula indiferenciada, debido a lo cual sería de esperar que en células no especializadas en la síntesis de proteínas la acción radiocitológica induzca la blastogénesis celular.
A las 4 hs de incubación del cultivo inducido con el radioiodo, se observan LPMNn con filamentos interlobulillares prácticamente inexistentes y redistribución de la cromatina; estadio que llamaremos, en adelante, ESTADIO I de lesión. Otros LPMNn muestran un núcleo unificado, amorfo, con agrumación de cromatina hacia los bordes nucleares, que denominaremos ESTADIO II de lesión. También se observan ESTADIOS III, con aspecto de metamielocitos y ESTADIOS IV con aspecto morfológico de mielocitos; todos ellos paraformas o pseudoformas de las formas.
Tales hallazgos demuestran, al menos, la existencia de una pseudoinmaduración. Otra entidad de idéntica dirección pero de distinto sentido, la pseudomaduración degenerativa, ha sido descripta con anterioridad y analizada por otros autores.
La pseudomaduración degenerativa fue descubierta en pacientes con tratamiento monodroga por leucemia mieloide aguda (LMA) y tales elementos fueron designados como paraneutrófilos. Se observaron luego en sujetos no tratados de mielosis aguda y se los vinculó con alteraciones citoquímicas varias relacionadas con las peroxidasas y los lípidos. Rohr, en Alemania, definió al respecto la existencia de toda una progenie directa y anormal de elementos dismórficos. En 1963 el concepto fue extendido a la eritroleucemia por Catovsky y colaboradores, y confirmado por Etcheverry y Suarez en 1967. Finalmente Killmann incorporó el hallazgo de esos elementos a la displasia hematopoyética o estado preleucémico. (6)
Los caracteres morfológicos del neutrófilo de pseudomaduración degenerativa, consisten en un asincronismo morfoestructural de maduración, demostrado por lobulación del núcleo, cromatina inmadura para ese grado de lobulación y masa nuclear francamente aumentada respecto a la citoplasmática. (6)
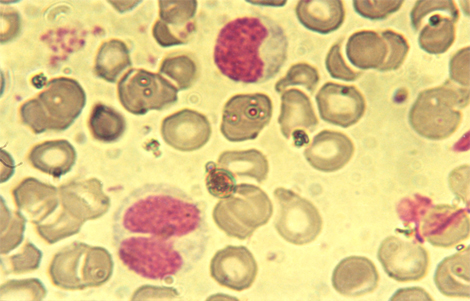
Sangre de Leucemia mieloide crónica en tratamiento monodroga. Nótese la presencia de un metamielocito en el borde superior (a las 12) y un paraneutrófilo de pseudomaduración o de intensa regeneración en el borde inferior (a las 7).
En el caso experimental que nos ocupa, se observa un asincronismo morfoestructural de inmaduración, demostrado por deslobulación del núcleo, núcleo único con una madurez de la cromatina que no condice con ese estado nuclear, pero masa nuclear grande que aumenta la relación núcleo-citoplasmática.
En algunos leucocitos polimorfonucleares involucionados a estadio IV, según observaremos en las microfotografías, se encuentra la aparición de vacuolas nucleares, de nucleolo en anillo o de cromosoma en anillo, engrosamiento de la membrana nuclear y frecuentes organitos citoplasmáticos.